
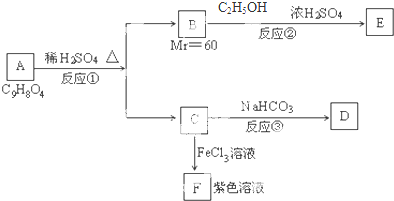
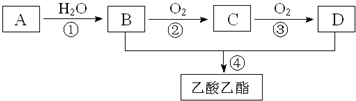
 �л���A�ɷ�������ת����
�л���A�ɷ�������ת����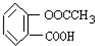 ��CΪ
��CΪ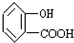 ��C�к��з��ǻ����Ȼ������ǻ���̼�����Ʋ���Ӧ���Ȼ���Ӧ����DΪ
��C�к��з��ǻ����Ȼ������ǻ���̼�����Ʋ���Ӧ���Ȼ���Ӧ����DΪ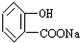 ��BΪCH3COOH����CH3CH2OH����������Ӧ���ɵ�EΪCH3COOCH2CH3���ݴ˿��ƣ�
��BΪCH3COOH����CH3CH2OH����������Ӧ���ɵ�EΪCH3COOCH2CH3���ݴ˿��ƣ�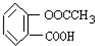 ��CΪ
��CΪ ��C�к��з��ǻ����Ȼ������ǻ���̼�����Ʋ���Ӧ���Ȼ���Ӧ����DΪ
��C�к��з��ǻ����Ȼ������ǻ���̼�����Ʋ���Ӧ���Ȼ���Ӧ����DΪ ��BΪCH3COOH����CH3CH2OH����������Ӧ���ɵ�EΪCH3COOCH2CH3��
��BΪCH3COOH����CH3CH2OH����������Ӧ���ɵ�EΪCH3COOCH2CH3��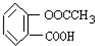 ���ʴ�Ϊ��
���ʴ�Ϊ��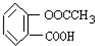 ��
��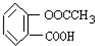 ��ˮ�ⷴӦ������������Ҵ�����������Ӧ���ʴ�Ϊ��ˮ�⣻������
��ˮ�ⷴӦ������������Ҵ�����������Ӧ���ʴ�Ϊ��ˮ�⣻������ ��C�к��з��ǻ����Ȼ������ǻ���̼�����Ʋ���Ӧ���Ȼ���Ӧ����DΪ
��C�к��з��ǻ����Ȼ������ǻ���̼�����Ʋ���Ӧ���Ȼ���Ӧ����DΪ ��C����D�ķ�ӦΪ
��C����D�ķ�ӦΪ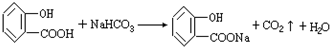 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��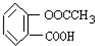 �����������Ȼ����������Ȼ����ܺ��������Ʒ�Ӧ��ˮ�����ɵķ��ǻ�Ҳ�ܺ��������Ʒ�Ӧ����A��NaOH��Һ���ȵĻ�ѧ����ʽ
�����������Ȼ����������Ȼ����ܺ��������Ʒ�Ӧ��ˮ�����ɵķ��ǻ�Ҳ�ܺ��������Ʒ�Ӧ����A��NaOH��Һ���ȵĻ�ѧ����ʽ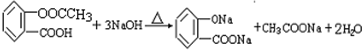 ������1mol A��Ӧ�����ĵ�NaOH���ʵ���Ϊ3mol���ʴ�Ϊ��3��
������1mol A��Ӧ�����ĵ�NaOH���ʵ���Ϊ3mol���ʴ�Ϊ��3��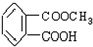 ��
�� ��
��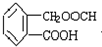 ��
��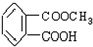 ��
�� ��
��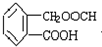 ��
��


 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����n=2ʱ������A��B��ת����֮��Ϊ1��2 | ||
B����ʼʱ�̺ʹﵽƽ��������е�ѹǿ��Ϊ��1+n������1+n-
| ||
| C����v��A����=2v��C����ʱ���ɶ϶���Ӧ�ﵽƽ�� | ||
| D������ʼʱ����3molA��3n molB����ﵽƽ��ʱ����3a mol��C |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��������̼������Һ�ķ�Ӧ |
| B�����������Ũ�ȵ�Ca��HCO3��2��NaOH��Һ���Ca2++2HCO3-+2OH-��CaCO3��+CO32-+2H20 |
| C������������ϡ�����У�FeS+2H+=Fe2++H2S�� |
| D�����۵⻯����Һ�ڿ����б���2I-+O2+H2O=I2+2OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
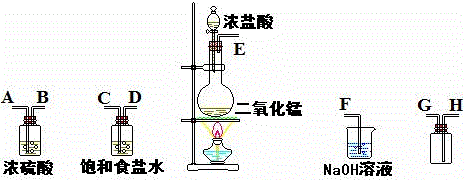
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
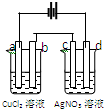 ��ͼ�ĵ����У�a��b��c��d����ʯī�缫��ͨ��һ��ʱ���a��b��c��d���缫�����������ʵ���֮���ǣ�������
��ͼ�ĵ����У�a��b��c��d����ʯī�缫��ͨ��һ��ʱ���a��b��c��d���缫�����������ʵ���֮���ǣ�������| A��2��2��4��1 |
| B��1��1��2��1 |
| C��2��4��4��1 |
| D��2��1��2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2S��Һ��ˮ�⣺S2-+2H2O?H2S+2OH- | |||
| B��NaHCO3��Һ�ĵ��룺HCO3-+H2O?CO32-+H3O+ | |||
| C��NH4Cl��Һ��ˮ�⣺NH4++H2O?NH3?H2O+H+ | |||
D��500�桢30MPa�£���0.5mol N2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
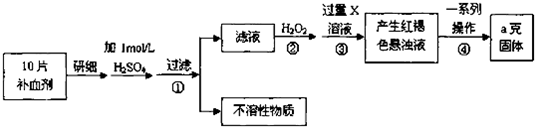
| ʵ�鷽�� | ʵ������ | ���� |
| ����Һ�м�KSCN��Һ | ������������FeCl3 | |
| ��KMnO4��Һ�м�����A��Һ | KMnO4��Һ��ɫ�����Ա仯 | ���������в��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com