
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如图所示关系,根据图示转化关系推测下列说法不正确的是 ( )
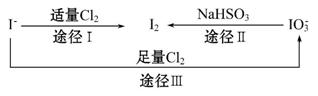
A.可用KI-淀粉试纸和食醋检验加碘盐中是否含有碘
B.足量Cl2能使湿润的KI-淀粉试纸变白的原因可能是5Cl2+I2+6H2O====2HIO3+
10HCl
C.由图可知氧化性的强弱顺序为Cl2>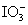 >I2
>I2
D.途径Ⅱ中若生成1 mol I2,反应中转移的电子数为10NA
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
据最近的美国《农业研究》杂志报道,美国的科学家发现半胱氨酸能增强艾滋病毒感染者的免疫力,对控制艾滋病毒的蔓延有奇效。已知半胱氨酸的结构简式为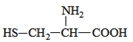 ,则下列说法错误的是
,则下列说法错误的是
A.两分子半胱氨酸脱水形成的二肽结构简式为:
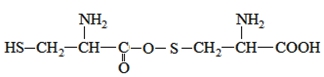
B.半胱氨酸是一种两性物质
C.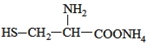 可与过量NaOH溶液反应放出氨气
可与过量NaOH溶液反应放出氨气
D.天然蛋白质水解产物均为α-氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于硅单质及其化合物的说法正确的是
①硅是构成一些岩石和矿物的基本元素 ②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维 ④陶瓷是人类应用很早的硅酸盐材料
A.①② B.②③ C.①④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学为了验证碳和硅两种元素非金属性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
 |
实验操作步骤:
Ⅰ. 打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ. A中看到白色沉淀时,…,关闭活塞a。
请回答:
(1)B中反应的离子方程式是________。
(2)通过步骤Ⅰ得知盐酸具有的性质是________(填字母)。
A.挥发性 B. 还原性 C. 氧化性 D. 酸性
(3)C装置的作用是________,X是________(写化学式)。
(4)为了验证碳的非金属性强于硅,步骤Ⅱ中未写的操作和现象是________,
D中反应的化学方程式是________。
(5)碳、硅的非金属性逐渐减弱的原因是________(从原子结构角度加以解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下硝酸铵受热分解的未配平化学方程式为NH4NO3——HNO3+N2+H2O,在反应中被氧化与被还原的氮原子数之比为( )
A.5∶3 B.5∶4
C.1∶1 D.3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
已知碳酸钙的分解①CaCO3(s)====CaO(s)+CO2(g)仅在高温下自发进行;氯酸钾的分解
②2KClO3(s)====2KCl(s)+3O2(g)在任何温度下都自发进行,下面有几组焓变数据,其中可能正确的是( )
A.ΔH1=-178.32 kJ·mol-1 ΔH2=-78.3 kJ·mol-1
B.ΔH1=+178.32 kJ·mol-1 ΔH2=-78.3 kJ·mol-1
C.ΔH1=-178.32 kJ·mol-1 ΔH2=+78.3 kJ·mol-1
D.ΔH1=+178.32 kJ·mol-1 ΔH2=+78.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c/(mol·L-1) | 0.8 | 1.24 | 1.24 |
下列说法正确的是( )
①平衡后升高温度,平衡常数>400
②平衡时,c(CH3OCH3)=1.6 mol·L-1
③平衡时,反应混合物的总能量减少20 kJ
④平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大
⑤此时刻反应达到平衡状态
⑥平衡时CH3OH的浓度为0.08 mol·L-1
A.①②④⑤ B.②⑥ C.②③④⑥ D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。
完成下列计算:
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠 g。
(2)钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
②计算并确定该钠-钾合金的化学式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com