
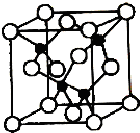
 X��Y��Z��U��W��ԭ���������������ǰ������Ԫ�أ�����Y��ԭ�Ӻ�����7���˶�״̬��ͬ�ĵ��ӣ�X��Z��δ�ɶԵ�������Ϊ2�� U�ǵ�������Ԫ���γɵļ������а뾶��С��Ԫ�أ�W���ڲ����ȫ�����������ֻ��1�����ӣ���ش��������⣺
X��Y��Z��U��W��ԭ���������������ǰ������Ԫ�أ�����Y��ԭ�Ӻ�����7���˶�״̬��ͬ�ĵ��ӣ�X��Z��δ�ɶԵ�������Ϊ2�� U�ǵ�������Ԫ���γɵļ������а뾶��С��Ԫ�أ�W���ڲ����ȫ�����������ֻ��1�����ӣ���ش��������⣺���� X��Y��Z��U��W��ԭ���������������ǰ������Ԫ�أ�����Y��ԭ�Ӻ�����7���˶�״̬��ͬ�ĵ��ӣ���YΪNԪ�أ�U�ǵ�������Ԫ���γɵļ������а뾶��С��Ԫ�أ���UΪAl��X��Z��δ�ɶԵ�������Ϊ2��X��ԭ������С��N����Z��ԭ����������N��Al֮�䣬X��Z�ĺ�������Ų��ֱ�Ϊ1s22s22p2��1s22s22p4����XΪCԪ�ء�ZΪOԪ�أ�W���ڲ����ȫ�����������ֻ��1�����ӣ�ԭ����������Al��ֻ�ܴ��ڵ������ڣ����������Ϊ2+8+18+1=29����WΪCuԪ�أ��Դ˽����⣮
��� �⣺X��Y��Z��U��W��ԭ���������������ǰ������Ԫ�أ�����Y��ԭ�Ӻ�����7���˶�״̬��ͬ�ĵ��ӣ���YΪNԪ�أ�U�ǵ�������Ԫ���γɵļ������а뾶��С��Ԫ�أ���UΪAl��X��Z��δ�ɶԵ�������Ϊ2��X��ԭ������С��N����Z��ԭ����������N��Al֮�䣬X��Z�ĺ�������Ų��ֱ�Ϊ1s22s22p2��1s22s22p4����XΪCԪ�ء�ZΪOԪ�أ�W���ڲ����ȫ�����������ֻ��1�����ӣ�ԭ����������Al��ֻ�ܴ��ڵ������ڣ����������Ϊ2+8+18+1=29����WΪCuԪ�أ�
��1��ͬ������ԭ����������һ�����ܳ��������ƣ���NԪ��2p�ܼ�Ϊ�����ȶ�״̬�������ϵͣ���һ�����ܸ���ͬ��������Ԫ�أ��ʵ�һ������N��O��C��
�ʴ�Ϊ��N��O��C��
��2��WΪCuԪ�أ��۵����Ų�ʽΪ3d104s1��Cuͬ���ڵ�Ԫ���У���Cuԭ��������������ȵ�Ԫ�ػ���K��Cr��
�ʴ�Ϊ��3d104s1��K��Cr��
��3�����ݵȵ�����ԭ������֪������CO��N2��Ϊ�ȵ����壬CO�Ľṹʽ��C��O��YZ2-��Y��N���γ�2���ļ�����1���µ��Ӷԣ�Ϊsp2�ӻ���VSEPRģ����ƽ�������Σ�
�ʴ�Ϊ��C��O��ƽ�������Σ�
��4��X��Y��Z������⻯��ֱ�ΪCH4��NH3��H2O��3���⻯�������ԭ�Ӽ۲���Ӷ�����Ϊ4��VSEPRģ�;�Ϊ���������Σ�������ԭ�ӵŵ��Ӷ������������¼��DZ�С���ʼ��ǣ�CH4��NH3��H2O��
�ʴ�Ϊ��CH4��NH3��H2O��3���⻯�������ԭ�Ӽ۲���Ӷ��پ�Ϊ4��VSEPRģ�;�Ϊ��������ṹ��������ԭ�ӵŵ��Ӷ����������ӣ����¼��DZ�С��
��5��������Nԭ����ĿΪ4��Alԭ����ĿΪ8��$\frac{1}{8}$+6��$\frac{1}{2}$=4���ʸû����ﻯѧʽΪAlN��Ϊԭ�Ӿ��壬Yԭ���γ�4�����ۼ�����Yԭ���ӻ���ʽΪsp3��
�ʴ�Ϊ��AlN��ԭ�ӣ�sp3��
��6���辧����Alԭ����ĿΪN��Al������N��Al����$\frac{27}{6.02��1{0}^{23}}$g=��405��10-10��3��2.70g/cm3�����N��Al��=4.00�������侧�����������������ܶѻ���
�ʴ�Ϊ�������������ܶѻ���
���� �����Ƕ����ʽṹ�����ʵĿ��飬Ϊ��Ƶ���㣬������ѧ���ķ��������������Ŀ��飬��Ŀ�漰��������Ų��������ܡ��ӻ���ʽ����������ȣ��Ƕ�ѧ���ۺ������Ŀ��飬�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
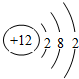 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
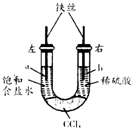 ������ͼװ�ý���ʵ�飬��ʼʱ����������Һ����ƽ���ܷ�ã�����һ��ʱ�䣮����˵����ȷ���ǣ�������
������ͼװ�ý���ʵ�飬��ʼʱ����������Һ����ƽ���ܷ�ã�����һ��ʱ�䣮����˵����ȷ���ǣ�������| A�� | �����O2�õ����ӣ��ҹ���H+�õ����� | |
| B�� | һ��ʱ������Һ������ҹ�Һ�� | |
| C�� | a��b����������ͬ�ĵ缫��Ӧʽ��Fe-3e-=Fe3+ | |
| D�� | a����Һ��pH����b����Һ��pH��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ζ�ʱ�����ֿ��Ƶζ��ܻ�������������ƿ���ߵα����۾�ע�ӵζ�����Һ�� | |
| B�� | ����ʱ��Ӧʹ�¶ȼ�ˮ����������ƿ֧�ܿڴ� | |
| C�� | ��Һʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ��� | |
| D�� | �����Ȼ�����Һʱ����һ�����Ȼ����ܽ��ڽ�Ũ�������У�����ˮϡ�͵�����Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 115mol/L | B�� | 1mol/L | C�� | 3mol/L | D�� | 2mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
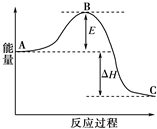 ��Ԫ�ص��⻯����������ڹ�ҵ�����ͷ������ж��й㷺��Ӧ�ã���ش��������⣺
��Ԫ�ص��⻯����������ڹ�ҵ�����ͷ������ж��й㷺��Ӧ�ã���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯī | B�� | ˮ�� | C�� | ����� | D�� | �մ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6ml | B�� | 12ml | C�� | 15ml | D�� | 18ml |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com