
【题目】工业废水中常含有一定量的Cr2O72-,易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将Cr2O72-转化为Cr3+,再将Cr3+转化为Cr(OH)3沉淀。
(1)利用硫酸工业废气中的SO2 可以处理酸性含铬废水,用离子方程式表示反应原理___________。
(2)已知Ksp[Cr(OH)3]=1×10-30。室温下,除去被SO2还原所得溶液中的Cr3+[使c(Cr3+)≤1×10-6mol·L-1],需调节溶液的pH至少为__________________。
(3)Cr(OH)3和Al(OH)3类似,也是两性氢氧化物,写出Cr(OH)3的酸式电离方程式__________。
(4)Cr3+在强碱中可被双氧水氧化为CrO42-,发生反应的离子方程式为_________________。控制其他条件不变,反应温度对Cr3+转化率的影响如下图所示。请分析温度超过70℃时,Cr3+转化率下降的原因是__________________。

【答案】Cr2O72-+3SO2+2H+=2Cr3++3SO42-+H2O 6 Cr(OH)3+H2O![]() H++[Cr(OH)4]-[或Cr(OH)3
H++[Cr(OH)4]-[或Cr(OH)3![]() H++CrO2-+H2O] 2Cr3++3H2O2+10OH-=2CrO42-+8H2O 双氧水在较高温度下发生分解,浓度降低
H++CrO2-+H2O] 2Cr3++3H2O2+10OH-=2CrO42-+8H2O 双氧水在较高温度下发生分解,浓度降低
【解析】
(1) SO2具有还原性,能将Cr2O72-转化为Cr3+,用硫酸工业废气中的SO2处理酸性含铬废水,离子方程式为:Cr2O72-+3SO2+2H+=2Cr3++3SO42-+H2O;(2)已知Ksp[Cr(OH)3]=1×10-30。室温下,除去被SO2还原所得溶液中的Cr3+[使c(Cr3+)≤1×10-6mol·L-1],Ksp[Cr(OH)3]=c(Cr)×c3(OH-)==1×10-6×c3(OH-)=1×10-30,c(OH-)=10-8 mol·L-1,需调节溶液的pH至少为6;(3)由于Cr(OH)3和Al(OH)3类似,也是两性氢氧化物,则Cr(OH)3的酸式电离方程式为:Cr(OH)3+H2O![]() H++[Cr(OH)4]-[或Cr(OH)3
H++[Cr(OH)4]-[或Cr(OH)3![]() H++CrO2-+H2O]; (4)Cr3+在强碱中可被双氧水氧化为CrO42-,发生反应的离子方程式为:2Cr3++3H2O2+10OH-=2CrO42-+8H2O ,双氧水在温度超过70℃时发生分解,浓度降低,氧化能力降低,Cr3+转化率下降。
H++CrO2-+H2O]; (4)Cr3+在强碱中可被双氧水氧化为CrO42-,发生反应的离子方程式为:2Cr3++3H2O2+10OH-=2CrO42-+8H2O ,双氧水在温度超过70℃时发生分解,浓度降低,氧化能力降低,Cr3+转化率下降。


科目:高中化学 来源: 题型:
【题目】某研究小组设计了如下实验,探究常温下催化剂对过氧化氢分解反应的影响。
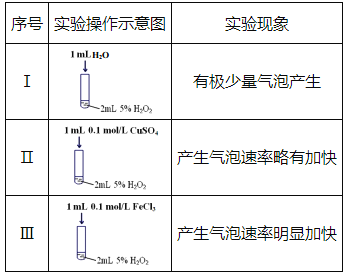
(1)实验I的作用是_________。
(2)实验III中反应的化学方程式为_________。
(3)根据实验I~III中现象的不同,可以得出的结论是:
①使用合适的催化剂,可提高双氧水分解的反应速率;
②___________________________。
(4)在一定温度下,10mL0.40mol/LH2O2溶液发生催化分解,6min后H2O2的浓度减小到0.10mol/L,以H2O2的浓度变化表示的反应速率为v(H2O2)=_________mol/(L·min)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水溶液中Fe3+和I-存在可逆反应:2Fe3++2I-![]() 2Fe2++I2,平衡常数为K。已知氢氧化铁和氢氧化亚铁的溶度积如下:Ksp[Fe(OH)2]=4.87×10-17,Ksp[Fe(OH)3]=2.64×10-39。下列判断不正确的是
2Fe2++I2,平衡常数为K。已知氢氧化铁和氢氧化亚铁的溶度积如下:Ksp[Fe(OH)2]=4.87×10-17,Ksp[Fe(OH)3]=2.64×10-39。下列判断不正确的是
A. 反应的平衡常数K=![]()
B. 该可逆反应只能在酸性条件下存在
C. 加入AgNO3,平衡右移,溶液黄色变浅
D. 加入CCl4,平衡右移,水溶液层黄色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体,图1表示各物质浓度随时间的变化,图2表示速率随时间的变化。t2、t3、t4、t5时刻后各改变一种条件,且改变条件均不同。若t4时刻改变条件是压强,则下列说法错误的是
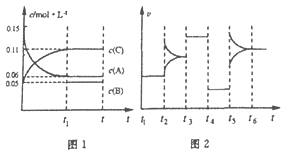
A. 若t1=15s,则前15s的平均反应速率v(C)=0.004mol·L-1·s-1
B. 该反应的化学方程式为:3A(g) ![]() B(g)+2C(g)
B(g)+2C(g)
C. t2、t3、t5时刻改变的条件分别是升高温度、加入催化剂、增大反应物浓度
D. B的起始物质的量为0.04mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。
(1)连二次硝酸中氮元素的化合价为________。
(2)常温下,用0.01 mol·L-1的NaOH溶液滴定10 mL 0.01 mol·L-1H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
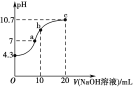
①写出H2N2O2在水溶液中的电离方程式:____________________________。
②c点时溶液中各离子浓度由大到小的顺序为_______________________________。
③b点时溶液中c(H2N2O2)________(填“>”“<”或“=”,下同)c(N2O![]() )。
)。
④a点时溶液中c(Na+)________c(HN2O)+c(N2O![]() )。
)。
(3)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中![]() =________。[已知Ksp(Ag2N2O2)=4.2×10-9,Ksp(Ag2SO4)=1.4×10-5]
=________。[已知Ksp(Ag2N2O2)=4.2×10-9,Ksp(Ag2SO4)=1.4×10-5]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1 NaOH溶液和下图所示装置进行测定中和热的实验,得到表中的数据:

实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH溶液 | ||
1 | 20.2 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 24.9 |
试完成下列问题:
(1)实验时用环形玻璃棒搅拌溶液的方法是____________________。
不能用铜丝搅拌棒代替环形玻璃棒的理由是_____________________。
(2)经数据处理,t2—t1=3.4 ℃。则该实验测得的中和热ΔH=________[盐酸和NaOH溶液的密度按1 g·cm-3计算,反应后混合溶液的比热容(c)按4.18 J·(g·℃)-1计算]。
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为ΔH1,则ΔH1与ΔH的关系为:ΔH1__________ΔH(填“<”、“>”或“=”),理由是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列产品或材料属于复合材料的是( )
①玻璃钢 ②采用碳纤维增强复合材料制的钓鱼竿 ③航天飞机机身 ④航天飞机隔热陶瓷瓦 ⑤纳米高分子复合材料
A. ①⑤ B. ①②③④⑤ C. ②⑤ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种短周期元素的原子半径及主要化合价如下表: (请用化学用语答题)
元素代号 | X | Y | Z | M | R |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(1) M在元素周期表中的位置为_____________。
(2)X与Y按原子个数比1∶1构成的物质的电子式为____;所含化学键类型______
(3)X+、 Y2-、M2-、R3+离子半径大小顺序为__________。
(4) 写出Z元素气态氢化物的形成过程___________。
(5)将YM2通入FeCl3溶液中的离子方程式:______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com