
【题目】在常温条件下,下列对醋酸的叙述中,不正确的是
A.pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-)
B.将pH=a的醋酸稀释为pH=a+1的过程中,c(CH3COOH)/c(H+)变小
C.浓度均为0.1 mol·L-1的CH3COOH和CH3COONa溶液等体积混合后:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]
D.等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,存在a+b=14
【答案】D
【解析】
A.pH=5.6的CH3COOH与CH3COONa混合溶液中,电荷守恒为c(Na+)+c(H+)=c(OH-)+c(CH3COO-),pH=5.6,则c(H+>(OH-),所以c(Na+)<c(CH3COO-),A正确;
B.加水稀释促进电离,则氢离子的物质的量增大,醋酸的物质的量减小,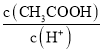 =
= 变小,B正确;
变小,B正确;
C.物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合,溶液显酸性,电荷守恒为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),物料守恒为c(CH3COO-)+c(CH3COOH)=0.1mol/L=2c(Na+),由上述两个式子可得c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)],C正确;
D.pH=a的醋酸与pH=b的NaOH溶液恰好中和,醋酸和氢氧化钠的物质的量相等,醋酸为弱酸,醋酸部分电离,醋酸的浓度大于氢离子的浓度,即c(CH3COOH)>10-amol/L,氢氧化钠的浓度等氢氧根离子的浓度,即c(NaOH)=10b-14mol/L,c(CH3COOH)=c(NaOH)=10b-14mol/L>10-amol,则a+b>14,D错误;
故选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图是元素M的价类二维图。其中A是一种盐,E的相对分子质量比D的相对分子质量大16,A和B是含最低价M元素的两种化合物,当x为一种强碱时,有如下转化关系。下列说法不正确的是( )
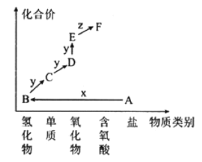
A.物质B遇少量的氯气会产生白烟
B.F的浓溶液可以用铁制容器盛放
C.E与水反应可生成F
D.物质D能够被x完全吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据所给图形回答下列问题:
⑴图表示容器中气体粒子的示意图,图中“![]() ”和“
”和“![]() ”分别代表不同元素的原子,它们的结合体代表分子,则图中可表示氮气的是______,可表示氯化氢(HCl)分子的是______,可表示一氧化碳和氧气的混合气体的是______(填序号)。
”分别代表不同元素的原子,它们的结合体代表分子,则图中可表示氮气的是______,可表示氯化氢(HCl)分子的是______,可表示一氧化碳和氧气的混合气体的是______(填序号)。
|
|
|
|
A | B | C | D |
⑵如图是水分子在一定条件下分解的示意图,从中获得的信息不正确的是______(填序号)。
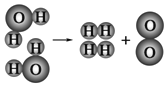
A 生成1mol O2需断开4mol H—O共价键
B 水分解后生成氢气和氧气的分子数比为2:1
C 水分解过程中,分子的种类不变
D 水分解过程中,原子的数目不变
⑶表各图中的小球代表原子序数从1—18元素的原子实![]() 原子实是原子除最外层电子后剩余的部分
原子实是原子除最外层电子后剩余的部分![]() ,小黑点代表未用于形成共价键的最外层电子,短线代表共价键.下列各图表示的结构与化学式一定不相符的是______(填序号)。
,小黑点代表未用于形成共价键的最外层电子,短线代表共价键.下列各图表示的结构与化学式一定不相符的是______(填序号)。
A | B | C |
|
|
|
NH3 | CO2 | CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家正在研究温室气体CH4和CO2的转化和利用。
(1)CH4和CO2所含的三种元素中电负性最大的为_________(填元素符号)。
(2)下列关于CH4和CO2的说法不正确的是_________(填序号)。
a.固态CO2属于分子晶体
b.CH4分子中含有极性共价键,是非极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp2
(3)在Ni基催化剂作用下,CH4和CO2反应可获得化工原料CO和H2。
①基态Ni原子的核外电子排布式为_______,Ni元素位于元素周期表的第_________族。
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1molNi(CO)4中含有_________molσ键。
③某镍白铜合金的立方晶胞结构如图所示。
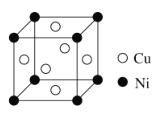
该晶体中距离Ni原子最近的Cu原子有_________个,若合金的密度为dg/cm3,阿伏加德罗常数的数值为NA,晶胞边长a=_________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PPG是一种可降解的聚酷类高分子材料,在材料的生物相容性方面有很好的应用前景。PPG的一种合成路线如下:
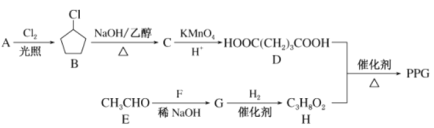
已知:R1CHO+R2CH2CHO![]()
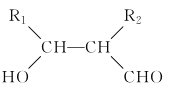
回答下列问题:
(1)G的结构简式为_________,B中含有官能团的名称为 _________。
(2)由B生成C的化学方程式为_________。
(3)H的化学名称为_________。
(4)由D和H生成PPG的化学方程式为_________。
(5)写出D的同分异构体中能同时满足下列条件的有机物结构简式:_________。
①能与饱和NaHCO3溶液反应产生气体
②既能发生银镜反应,又能发生水解反应
③核磁共振氢谱显示为3组峰,且峰面积比为6:1:1
(6)D的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是_________(填标号)
a.质谱仪 b.红外光谱仪c.元素分析仪d.核磁共振仪
(7)以E为起始原料合成![]() 选用必要的无机试剂,写出合成路线流程图:_________。合成路线流程图示例:H2C=CH2
选用必要的无机试剂,写出合成路线流程图:_________。合成路线流程图示例:H2C=CH2![]() CH3CH2OH
CH3CH2OH![]() CH3CH2Br。
CH3CH2Br。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组在某温度下测定溶液的pH时发现0.01mol/L 的NaOH溶液中,由水电离出的c(H+)c(OH-)=10-22,该探究小组将pH=x的H2SO4溶液与pH=y的NaOH溶液按体积比1:10混合,混合后所得溶液恰好呈中性,若x=![]() y,则x为( )
y,则x为( )
A.2B.3C.4D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中将CO2与含少量CO的H2混合生成甲醇,反应为:CO2(g)+3H2(g)CH3OH(g)+H2O(g),下图表示按![]() 分别为①1:4和②1:6两种投料比时,CO2的平衡经随温度变化的曲线。
分别为①1:4和②1:6两种投料比时,CO2的平衡经随温度变化的曲线。
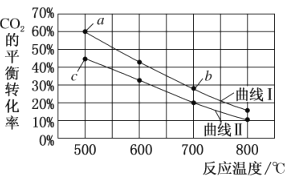
设①②两种投料比时CO2投料的物质的量浓度相等。下列有关说法正确的是
A.按投料比①时,CO2的平衡转化率随温度变化的曲线对应的是图中的曲线l
B.图中a点对应的H2的转化率为30%
C.图中b点对应的平衡常数K的值大于c点
D.![]() 的数值,a点比c点小
的数值,a点比c点小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫脲(![]() )是一种白色而有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
)是一种白色而有光泽的晶体,味苦,可用于制造树脂,也用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
(1)硫脲中硫的化合价为_______;与硫脲互为同分异构且能与FeCl3溶液发生显色反应的化合物的化学式为_______
(2)可用H2NCN(氨基腈)与C2H5SH (乙硫醇)反应制备硫脲。氨基腈的电子式为_____
(3)制取氨基腈的传统工艺流程如下:
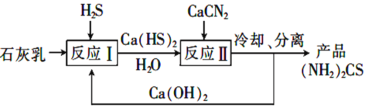
①反应Ⅱ的化学方程式为______
②测定硫脲含量的方法如下:
步骤1 :准确称取a g产品,经溶解等步骤最后在500 mL容量瓶中定容。
步骤2:准确量取20.00 mL配制好的溶液注入碘量瓶中,加入V1 mL c1 mol/L I2的标
准溶液及适量的NaOH溶液,于暗处放置10 min(2NaOH+I2=NaIO+NaI+H2O,
4NaIO+(NH2)2CS+H2O =(NH2)2CO+4NaI+H2SO2)。
步骤3:加水及适量的盐酸,摇匀。
步骤4:用c2 mol/L标准Na2S2O2溶液滴定剩余的I2( I2+2Na2S2O2=2NaI+Na2S4O6) ,加入淀粉溶液,滴定至终点时消耗Na2S2O2溶液V2mL。
“步骤3”加入盐酸的目的_________(用离子方程式说明)。
“步骤4”滴定至终点时的颜色变化是________。
③产品中(NH2)2CS的质量分数为_______ (列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.1molCH3COONa和0.05molHCl溶于水配成1L溶液(pH<7)。
(1)用离子方程式表示该溶液中存在的三个平衡体系___、___、__。
(2)溶液中各离子的物质的量浓度由大到小顺序为___。
(3)溶液中粒子中浓度为0.1mol/L的是___,浓度为0.05mol/L的是__。
(4)物质的量之和为0.lmol的两种粒子是___与___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com