
工业上用甲和乙通过化合反应制备丙,如图是三种分子的模型图,根据微观示意图得出的结论错误的是
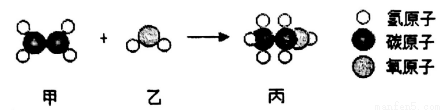
A.甲的化学式为C2H4
B.保持乙化学性质的最小微粒是水分子
C.化学反应前后分子的种类都发生了改变
D.乙和丙都属于氧化物
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年山东省泰安市高一下学期期末考试化学试卷(解析版) 题型:选择题
向甲、乙、丙、丁四个容积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小的顺序排列正确的是( )
甲.在500℃时,10 mol SO2和5 mol O2反应
乙.在500℃时,用V2O5做催化剂,10 mol SO2和5 mol O2反应
丙.在450℃时,8 mol SO2和5 mol O2反应
丁.在500℃时,8 mol SO2和5 mol O2反应
A.甲、乙、丙、丁
B.乙、甲、丙、丁
C.乙、甲、丁、丙
D.丁、丙、乙、甲
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆一中高一下期末化学试卷(解析版) 题型:实验题
回归、改进、拓展教材实验,是高考化学实验考查的常见形式。
I.甲组同学在进行《必修二》实验2-5“Fe3+离子在H2O2溶液分解实验中的催化作用”时,进行了以下探究。基于目前学过的元素周期表的相关知识,该小组推测了同为第四周期第VIII族的Fe、Co、Ni可能有相似的催化机理。
【查阅资料】:钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。其中CoxNi(1-x)Fe2O4(其中Co、Ni均为+2价)也可用作H2O2分解的催化剂,具有较高的活性。
(1)写出H2O2溶液在Fe3+催化下分解的化学方程式__________________________________。
(2)①该催化剂中铁元素的化合价为 。
②下图表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线。由图中信息可知: 法制取得到的催化剂活性更高,由此推测Co2+、Ni2+两种离子中催化效果更好的是 。

II.乙组同学在进行《选修四》实验2-2“草酸溶液浓度对酸性高锰酸钾溶液褪色时间的影响”时,发现溶液褪色总是先慢后快,该小组设计了如下过程探究其原因:
【查阅资料】KMnO4溶液氧化H2C2O4的反应历程为(流程中“III”等为Mn的价态):
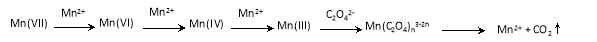
【提出假设】假设1:该反应为放热反应
假设2:反应生成的Mn2+ 对该反应有催化作用
假设3:K+ 对该反应有催化作用
【设计、完成实验】
(3)称取 g草酸晶体(H2C2O4·2H2O),配制500 mL 0.10 mol/L H2C2O4溶液。在上述过程中必须用到的2种定量仪器是托盘天平和
(4)完成探究,记录数据
实验 编号 | 烧杯中所加试剂及用量(mL) | 控制条件 | 溶液褪色时间(s) | |||
0.10 mol/L H2C2O4溶液 | 等浓度 KMnO4溶液 | H2O | 0.50 mol/L 稀硫酸 | |||
1 | 30 | 20 | 30 | 20 | 18 | |
2 | 30 | 20 | 30 | 20 | 水浴控制温度65 ℃ | 15 |
3 | 30 | 20 | 30 | 20 | 加入少量MnSO4固体 | 3.6 |
4 | 30 | 20 | x | 20 | 加入5 mL 0.10 mol/L K2SO4溶液 | 18 |
仔细阅读分析表中数据,回答问题:
x = mL,假设__________成立(填“1” 、“2”或“3”)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆一中高一下期末化学试卷(解析版) 题型:选择题
某无色溶液中含有大量的H+和SO42-,则此溶液还能大量存在的离子组是
A.Na+、Fe2+、NO3-
B.Na+、Mg2+、NO3-
C.Cr2O72-、Ba2+、Cl-
D.K+、Na+、S2O32-
查看答案和解析>>
科目:高中化学 来源:2016届浙江省杭州市高一入学测试化学试卷(解析版) 题型:简答题
归纳总结是学习化学的一种方法。

(1)甲同学发现A、B、C三种物质有如图l所示的相互反应关系,“—”表示能反应(部分反应物、生成物以及反应条件省略,下同)。己知A是常见金属,人体缺乏组成A的元素易患贫血症;B胃酸的主要成分;B与C反应产生不溶于稀硝酸的白色沉淀,则A是____(填化学式,下同,C是_______。请写出下列反应的化学方程式:A与B________________;B与C____________________。
(2)乙同学发现X、Y、Z三种物质有如图2所示的循环转化关系“→”表示能转化。
①若X、Y、Z均为含钙化合物,X是一种常用干燥剂,Y俗称熟石灰。则X的化学式为______;请写出Y→Z的反应化学方程式________________。
②若X是碳单质,Y、Z是含有碳元素的氧化物,X、Y、Z的相对分子质量依次增大,则Y的相对分子质量为 ;Z→X可通过以下反应实现:___________________;该反应的基本反应类型是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海省高一下期末化学试卷(解析版) 题型:选择题
下列关于碱金属的叙述正确的是 ( )
A. 随着核电荷数增加,它们的密度逐渐减小
B. 随着核电荷数增加,单质的熔点、沸点升高
C. 随着核电荷数的增加,单质与水反应的剧烈程度增大
D. 随着核电荷数增加,离子的氧化性逐渐增强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西西藏民族学院附中高一下期末化学试卷(解析版) 题型:填空题
氧硫化碳(COS)可替代磷化氢而被用作熏蒸剂。
(1)组成氧硫化碳和磷化氢的各原子中,原子半径最大的元素在周期表中的位置是_______________.
(2)下列事实可用于比较C与P两种元素非金属性相对强弱的是_____(填字母)
A.最高正化合价:P>C
B.同温同浓度的两溶液的酸性:H3PO4>H2CO3
C.沸点:PH3>CH4
(3)氧硫化碳水解及部分应用流程如下(部分产物已略去);
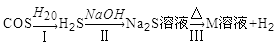
①已知:常温下,反应Ⅱ中每吸收1.7g H2S气体,反应放出热烈4.76kJ,则该反应的热化学方程式为_______________________________。
②已知M溶液中硫元素的主要存在形式为S2O32—,则反应Ⅲ中生成S2O32—的离子方程式为_______________.
③如图是反应Ⅲ中,在不同反应温度下,反应时间与H2产量的关系(Na2S初始含量为3mmol)。由图像分析可知,a点时M溶液中除S2O32—外,还有______________(填含硫微粒的离子符号)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com