
【题目】Na2S2O3·5H2O可作为高效脱氯剂,工业上用硫铁矿(FeS2)为原料制备该物质的流程如下。
硫铁矿
![]()
![]()
![]()
![]()
![]()
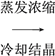 Na2S2O3·5H2O
Na2S2O3·5H2O
已知:Ⅰ.气体A可以使品红溶液褪色,与硫化氢(H2S)混合能获得单质硫。
Ⅱ.pH约为11的条件下,单质硫与亚硫酸盐可以共热生成硫代硫酸盐。
回答下列问题:
(1)沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,其目的是_______________________________。
(2)吸收塔中的原料B可以选用________(填字母序号)。
a.NaCl溶液 b.Na2CO3溶液 c.Na2SO4溶液
(3)某小组同学用下图装置模拟制备Na2S2O3的过程(加热装置已略去)。

①使用70%的硫酸比用98%的浓硫酸反应速率快,其原因是____________________。装置B的作用是______________________。
②C中制备Na2S2O3发生的连续反应的化学方程式有Na2S+H2O+SO2===Na2SO3+H2S、2H2S+SO2===3S↓+2H2O (或)2H2S+H2SO3===3S↓+3H2O和___________________________________。
(4)工程师设计了从硫铁矿获得单质硫的工艺,将粉碎的硫铁矿用过量的稀盐酸浸取,得到单质硫和硫化氢气体,该反应的化学方程式为__________。
【答案】 使固体与气体充分接触,加快反应速率 b 该反应的实质是H+与SO![]() 反应,70%的硫酸中含水较多,c(H+)和c(SO
反应,70%的硫酸中含水较多,c(H+)和c(SO![]() )都较大,生成SO2速率更快 防止倒吸 Na2SO3+S=Na2S2O3 FeS2+2HCl===FeCl2+H2S↑+S↓
)都较大,生成SO2速率更快 防止倒吸 Na2SO3+S=Na2S2O3 FeS2+2HCl===FeCl2+H2S↑+S↓
【解析】硫铁矿在沸腾炉中燃烧生成氧化铁与二氧化硫,气体A为二氧化硫,溶液D蒸发浓缩、冷却结晶得到硫代硫酸钠晶体,故D为Na2S2O3,单质单质硫与亚硫酸盐可以共热生成硫代硫酸盐,则溶液C为Na2SO3,故原料B为可以为碳酸钠溶液或氢氧化钠溶液。则
(1)沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,其目的是:使固体与气体充分接触,加快反应速率;(2)碳酸钠可以与二氧化硫反应生成亚硫酸钠与二氧化碳,而NaCl、硫酸钠不与二氧化硫反应,答案选b;(3)A为制备二氧化硫,二氧化硫在C中与硫化钠溶液反应得到硫化氢,硫化氢与二氧化硫反应得到S单质,S单质与亚硫酸钠反应得到硫代硫酸钠,C中反应导致装置内压强减小,因此B装置作用是防止倒吸。则
①该反应的实质是H+与SO32-反应,70%的硫酸中含水较多,c(H+)和c(SO32-)都较大,生成SO2速率更快;根据以上分析可知B装置作用是防止倒吸;②C中制备Na2S2O3发生的连续反应有:Na2S+H2O+SO2=Na2SO3+H2S、2H2S+SO2=3S↓+2H2O 或 2H2S+H2SO3=3S↓+3H2O 和Na2SO3+S![]() Na2S2O3;(4)由题目信息可知,FeS2与HCl反应生成H2S、S,同时还生成FeCl2,反应方程式为:FeS2+2HCl===FeCl2+H2S↑+S↓。
Na2S2O3;(4)由题目信息可知,FeS2与HCl反应生成H2S、S,同时还生成FeCl2,反应方程式为:FeS2+2HCl===FeCl2+H2S↑+S↓。


科目:高中化学 来源: 题型:
【题目】某元素的各级电离能(kJmol﹣1)分别为740、1 500、7700、10500、13600、18000、21700,当它与氯气反应时最可能形成的阳离子是( )
A.X+B.X2+C.X3+D.X4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究,其结构简式为 ,下列关于分枝酸的说法不正确的是
,下列关于分枝酸的说法不正确的是
A. 分子中含有3种含氧官能团
B. 1 mol分枝酸最多可与3mol NaOH发生中和反应
C. 在一定条件下可与乙醇、乙酸反应,且反应类型相同
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液退色,但退色原理不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,水既不做氧化剂,又不做还原剂的是( )
A. Cl2+H2O=HCl+HClO B. 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
C. 2Na+2H2O=2NaOH+H2↑ D. 2F2+2H2O=4HF+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸和亚硝酸盐在生产、医药等领域有着广泛应用。某校化学兴趣小组用下图所示仪器(夹持装置已省略)及药品,探究硫酸与亚硝酸钠反应生成气体的成分。已知NO2和NO液化温度分别为21 ℃和-152 ℃。
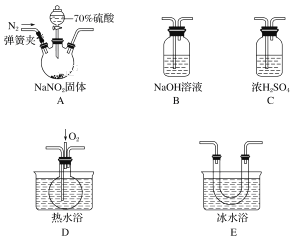
(1)A中盛放70%硫酸的仪器名称为___________________,反应前通入氮气的目的是_______________________________________________;仪器的连接顺序(按左→右连接)为A→________→________→________→B;
(2)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体。确认A中产生的气体含有NO,依据的现象是__________________________________;
(3)装置A中反应的化学方程式为________________________________;
(4)如果没有装置C,对实验结论造成的影响是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在元素周期表中纵行的编排依据是( )
A. 按元素的原子序数递增顺序从上到下排列
B. 按元素的原子最外层电子数依次递增顺序从上到下排列
C. 按元素的相对原子质量递增顺序从上到下排列
D. 最外层电子数相同的元素,按电子层数依次递增的顺序自上而下排列
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】江西曾发生居民误食工业用猪油的中毒事件,调查发现是因为其中混入了有机锡等。下列有关叙述正确的是( )
A.猪油是天然高分子化合物
B.猪油是含较多不饱和脂肪酸的甘油酯
C.猪油发生皂化反应后的反应液能使蓝色石蕊试纸变红
D.猪油发生皂化反应后,加入食盐搅拌,静置,有固体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题。(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是________;Y与过量浓硝酸反应后溶液中含有的盐的化学式为________。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是________。
A.Mg2+ B.Fe2+
C.Al3+ D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
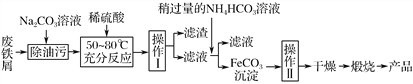
回答下列问题:
①操作Ⅰ的名称是________;操作Ⅱ的名称是________;操作Ⅱ的方法为________。
②请写出生成FeCO3沉淀的离子方程式:___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com