
【题目】燃料的使用和防污染是社会发展中一个无法回避的矛盾话题.
(1)我国北方冬季烧煤供暖所产生的废气是雾霾的主要来源之一.经研究发现将煤炭在O2/CO2的气氛下燃烧,能够降低燃煤时NO的排放,主要反应为:
2NO(g)+2CO(g)═N2(g)+2CO2(g)△H
若①N2(g)+O2(g)═2NO(g)△H1=+180.5kJmol﹣1
②2CO(g)═2C(s)+O2(g)△H2=+221kJmol﹣1
③C(s)+O2(g)═CO2(g)△H3=﹣393.5kJmol﹣1
则△H=kJmol﹣1 .
(2)为了提高燃料的利用率,可以将甲醇设计为燃料电池,写出熔融K2CO3做电解质时,甲醇燃料电池的负极反应式:;该电池负极与水库的铁闸相连时,可以保护铁闸不被腐蚀,这种方法叫做 .
(3)含有甲醇的废水随意排放会造成水污染,可用ClO2将其氧化为CO2 , 然后再加碱中和即可.写出处理甲醇酸性废水过程中,ClO2与甲醇反应的离子方程式: .
(4)机动车的尾气也是雾霾形成的原因之一. 
①近几年有人提出在催化剂条件下,利用汽油中挥发出来的C3H6催化还原尾气中的NO气体生成三种无污染的物质.请写出该过程的化学方程式:;
②电化学气敏传感器法是测定汽车尾气常用的方法之一.其中CO传感器的工作原理如上图所示,则对电极的电极反应式为 .
【答案】
(1)﹣746.5
(2)CH3OH﹣6e﹣+3CO32﹣=2H2O+4CO2↑;外加电流的阴极保护法
(3)6ClO2+5CH3OH=6Cl﹣+5CO2+6H++7H2O
(4)2C3H6+18NO=6CO2+9N2+6H2O;O2+4e﹣+4H+=2H2O
【解析】解:(1)②+③×2﹣①得到2NO(g)+2CO(g)N2(g)+2CO2(g),反应的焓变=+221kJmol﹣1+2(﹣393.5kJmol﹣1)﹣(180.5kJmol﹣1)=﹣746.5kJmol﹣1 , 所以答案是:﹣746.5;(2)负极发生氧化反应,甲醇燃料电池的负极反应式:CH3OH﹣6e﹣+3CO32﹣=2H2O+4CO2↑;该电池负极与水库的铁闸相连时,可以保护铁闸不被腐蚀,这种方法叫做外加电流的阴极保护法,所以答案是:CH3OH﹣6e﹣+3CO32﹣=2H2O+4CO2↑;外加电流的阴极保护法;(3)根据信息:二氧化氯和甲醇反应,生成Cl﹣、CO2和水2 , 所以反应方程式为:6ClO2+5CH3OH=6Cl﹣+5CO2+6H++7H2O,所以答案是:6ClO2+5CH3OH=6Cl﹣+5CO2+6H++7H2O;(4)①C3H6催化还原尾气中的NO气体,发生氧化还原反应生成无毒气体二氧化碳和氮气,所以反应方程式为:2C3H6+18NO=6CO2+9N2+6H2O,所以答案是:2C3H6+18NO=6CO2+9N2+6H2O;(4)①C3H6催化还原尾气中的NO气体,发生氧化还原反应生成无毒气体二氧化碳和氮气,所以答案是:2C3H6+18NO=6CO2+9N2+6H2O;
②电化学气敏传感器法是测定汽车尾气常用的方法之一.其中CO传感器的工作原理如上图所示,对电极氧气发生还原反应,电极反应式为O2+4e﹣+4H+=2H2O,所以答案是:O2+4e﹣+4H+=2H2O.
【考点精析】关于本题考查的反应热和焓变,需要了解在化学反应中放出或吸收的热量,通常叫反应热才能得出正确答案.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某主族元素R的最高正价与最低负价的代数和为4,由此可以判断( )
A. R一定是第四周期元素
B. R一定是ⅣA族元素
C. R气态氢化物化学式为H2R
D. R的气态氢化物比同周期其他元素气态氢化物稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化铝(AlON)属原子晶体,是一种超强透明材料,可以由反应Al2O3+C+N2 ![]() 2AlON+CO合成,下列有关说法正确的是( )
2AlON+CO合成,下列有关说法正确的是( )
A.氮氧化铝中氮的化合价是﹣3
B.反应中氧化产物和还原产物的物质的量之比是1:2
C.反应中每生成5.7gAlON同时生成1.12LCO
D.AlON和CO的化学键类型不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(g)=3C(g)+4D(g)中,表示该反应速率最快的是( )
A.v(A)=0.5molL﹣1 . mim﹣1
B.v(B)=0.3molL﹣1 . mim﹣1
C.v(C)=0.8molL﹣1 . mim﹣1
D.v(D)=1.0molL﹣1 . mim﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量为M的某物质在室温下溶解度为Sg,此时测得饱和溶液的密度为dg·mL-1 , 则该饱和溶液的物质的量浓度是( )
A.![]() mol·L-1
mol·L-1
B.![]() mol·L-1
mol·L-1
C.![]() mol·L-1
mol·L-1
D.![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Cl﹣、SO42﹣、CO32﹣、NH4+、Fe3+、Fe2+和Na+ . 某同学为了确认其成分,取部分溶液,设计并完成了如图实验:下列说法正确的是( ) 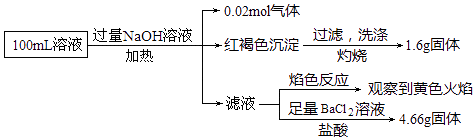
A.原溶液中c(Fe3+)=0.2molL﹣1
B.SO42﹣、NH4+、Na+一定存在,CO32﹣一定不存在
C.要确定原溶液中是否含有Fe2+ , 其操作为取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有Fe2+
D.溶液中至少有4种离子存在,其中Cl﹣一定存在,且c(Cl﹣)≥0.2molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是来自石油的重要有机化工原料,此物质可以用来衡量一个国家石油化工发展水平.C在一定条件下也会生成D,D能使石蕊溶液变红;E是具有果香味的有机物,F是一种高分子化合物,可制成多种包装材料. 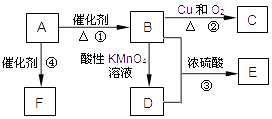
(1)A物质的结构简式为 .
(2)B→C的反应类型:;
(3)反应③的化学方程式为 .
(4)请设计一个简单的实验,以验证C物质存在该官能团的方法 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,原子数相同的是
A. 2 L CO和2 L O2
B. 标况下2 mol CO2和44.8 L水
C. 0.2 mol H2和4.48 L HCl
D. 同温同压下,2L氧气与2L氯气和氯化氢的混合气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com