
【题目】在标准状况下,11.2L 乙炔跟溴起加成反应,理论上有多少克溴参加反应____?
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 木材、纺织品浸过水玻璃后,具有防腐性能且不易燃烧
B. 金属镁的熔点高达2800℃,是优质的耐高温材料
C. 氧化铁红颜料跟某些油料混合,可以制成防锈油漆
D. 由于铜盐能杀死某些细菌,并能抑制藻类生长,因此游泳场馆常用硫酸铜作池水消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸铁锂电池具有高效率输出、可快速充电、对环境无污染等优点,其工作原理如图。M电极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许 Li+通过,电池反应式
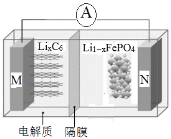
为LixC6+Li1-xFePO4 ![]() LiFePO4+6C。下列说法正确的是
LiFePO4+6C。下列说法正确的是
A.放电时Li+从右边移向左边
B.放电时M是负极,电极反应式为:C6x--xe-=6C
C.充电时N极连接电源的正极,电极反应式为:LiFePO4-xe-=Li1-xFePO4+xLi+
D.充电时电路中通过0.5mol电子,消耗36gC
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式与所述事实相符且正确的是
A. 氯气和水反应:Cl2 + H2O ![]() 2H+ + Cl- + ClO-
2H+ + Cl- + ClO-
B. 碳酸钙与醋酸溶液反应:CaCO3 + 2H+ = Ca2+ + H2O + CO2↑
C. 200 mL 2 mol/L的FeBr2溶液中通入11.2 L标准状况下的氯气:
4Fe2+ + 6Br-+ 5Cl2 == 4Fe3+ + 3Br2 + 10Cl-
D. Na2S水解的离子方程式:S2- + 2H2O ![]() H2S + 2OH-
H2S + 2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别将镁条和铝条平行插人盛有一定浓度稀盐酸、NaOH的烧杯中,用导线和电流计连接成两个原电池,装置如图所示。原电池工作时,下列叙述正确的是
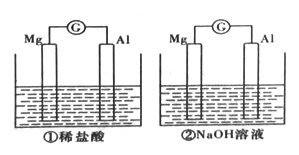
A. 因为Mg比Al活泼,所以两个原电池中负极都是Mg
B. 两个原电池中,电子都是由镁条通过导线流向铝条
C. 两个原电池中,反应放出的能量都完全转化成电能
D. 两个原电池中,正极都有氢气生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.常温常压下,断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为KJ.mol-1)下表是一些键能数据(KJ·mol-1)
化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 |
C-F | 427 | C-Cl | 330 | C-I | 218 |
H-H | 436 | S=S | 255 | H-S | 339 |
回答下列问题:
写出H2(g)与S2(g)反应生成H2S(g)的热化学方程式____________________________。
Ⅱ.某温度时,在2 L密闭容器中,三种气态物质X、Y、Z的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析可得:

(1)该反应的化学方程式为___________________。
(2)反应开始至2 min,用Y表示的平均反应速率为_____________,X的转化率为_________。
(3)在一定温度下,下列情况可作为上述反应达到反应限度的标志的是________。
A.X、Y、Z的浓度相等
B.X、Y、Z的分子数比为3︰1︰2
C.Z的生成速率是Y的生成速率的二倍
D.单位时间内生成n mol Y,同时生成3n mol X
Ⅲ.如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是________(填“a”或“b”)电极,该极的电极反应式为: ________________。
②电池工作一段时间后电解质溶液的pH__________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【加试题】铁在工业和生活中都具有非常重要的应用。某含铁化合物W,为探究其成分,化学兴趣小组的同学取化合物W粉末进行试验。经组成分析,该粉末除Fe外还有O和另一未知元素共三种元素。另取2.22g化合物W的粉末溶于适量稀硫酸,向反应后的溶液中加入含有3.20gNaOH的溶液,恰好完全反应。过滤,将洗涤后的沉淀充分灼烧,得到红棕色粉末1.60g;将所得滤液在一定条件下蒸发灼烧可得到一种纯净的不含结晶水的盐7.10g。请回答:
(1)则另一未知元素为________(填化学式)。
(2)①该化合物W的化学式为________________。
②该化合物W与适量稀硫酸反应的化学方程式___________________。
(3)草酸钴是广泛应用于磁性材料、电池材料、及超硬材料等领域。某研究小组在实验室探究CoC2O4分解反应的平衡常数。将一定量纯净的CoC2O4粉末置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解的平衡:
CoC2O4(S)![]() CoO(S)+CO(g)+CO2(g)
CoO(S)+CO(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
温度/℃ | 240 | 250 | 260 | 270 |
平衡总压强/kp | 5.7 | 8.3 | 12.0 | 17.1 |
平衡总浓度/mol·L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 |
由表中数据,列式计算250℃时CoC2O4分解平衡常数 。 该反应的焓变△H 0(填“>”、“=”或“<”)。
(4)温度加热至350℃,CO2的体积分数开始发生变化,体积分数和温度的关系如下:试画出CO的体积分数随温度升高的曲线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com