
【题目】下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。
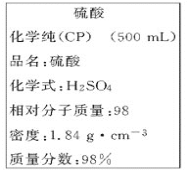
现用该浓硫酸配制240 mL 1.0 mol/L的稀硫酸。可供选用的仪器有:①玻璃棒;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。
请回答下列问题:
(1)配制上述稀硫酸时,还缺少的仪器有_____________________________(写仪器名称)。
(2)标签所示浓硫酸的物质的量浓度为___________________________。
(3)配制240 mL 1.0 mol/L的稀硫酸需要用量筒量取上述浓硫酸的体积为___________mL,量取硫酸时应选用 _____________ 规格的量筒。
A.10 mL B.50 mL C.100 mL D.200 mL
(4)根据计算结果,进行如下实验操作:
①用量筒取计算所需体积的浓硫酸
②向量筒中加入少量蒸馏水,并用玻璃棒搅拌
③立即将稀释后的溶液转入容量瓶中
④然后将蒸馏水沿玻璃棒注入容量瓶直至刻度线
⑤把容量瓶盖盖紧,上下颠倒摇匀
你认为上述实验中错误的操作是______________________________(填序号)
(5)经过测定,某同学配制的稀硫酸浓度偏高,则可能的原因是_____________(填序号)
①用量筒量取浓硫酸时,仰视刻度线
②容量瓶用蒸馏水洗涤后未经干燥
③洗涤烧杯内壁后将洗涤液弃去
④转移溶液时,不慎有少量溶液洒出
⑤定容时,俯视容量瓶刻度线
⑥定容、摇匀后发现溶液的凹液面低于刻度线
【答案】250mL容量瓶、胶头滴管 18.4 mol/L 13.6 B ②③④ ①⑤
【解析】
(1)配制稀硫酸需要使用①玻璃棒;③烧杯;⑤量筒,还缺少的仪器为:250mL容量瓶、胶头滴管;
(2) 标签所示浓硫酸的物质的量浓度为![]() =18.4 mol/L。
=18.4 mol/L。
(3) 配制240 mL 1.0 mol/L的稀硫酸,要使用250mL的容量瓶,所以配制250mL溶液。需要用量筒量取上述浓硫酸的体积![]() = 13.6mL。 所以选择50mL量筒。
= 13.6mL。 所以选择50mL量筒。
(4)不能在量筒中进行浓硫酸的稀释,故②错误。且稀释时放出大量的热,应冷却后再转移,故③立即将稀释后的溶液转入容量瓶中是错误的。加水到离容量瓶的刻度线下1-2cm改用胶头滴管加水到凹液面与刻度线相切,故错误。故选选②③④。
(5) ①用量筒量取浓硫酸时,仰视刻度线,浓硫酸体积变大,则浓度变大;②容量瓶用蒸馏水洗涤后未经干燥,对浓度没有影响,故错误;③洗涤烧杯内壁后将洗涤液弃去,溶质有损失,故浓度减小;④转移溶液时,不慎有少量溶液洒出,溶质有损失,浓度减小;⑤定容时,俯视容量瓶刻度线,溶液的体积变小,浓度变大;⑥定容、摇匀后发现溶液的凹液面低于刻度线,属于正常现象。故能使浓度变大的为①⑤。


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】有关原电池的下列说法中不正确的是( )
A.电池负极发生氧化反应
B.一般相对活泼的金属材料做电池的负极
C.电子流向是从负极流向正极(外电路)
D.阳离子移向负极(内电路)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机合成中碳环的形成非常重要。
(1)重氮甲烷(![]() )在加热或光照时分解成碳烯(∶CH2):
)在加热或光照时分解成碳烯(∶CH2):![]() 。碳烯与烯烃反应,生成含有三元环的环状化合物,如:
。碳烯与烯烃反应,生成含有三元环的环状化合物,如: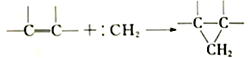 。则根据反应
。则根据反应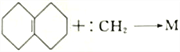 ,回答下列问题:
,回答下列问题:
①写出M 的结构简式:__________________。
②上述反应的反应类型是____________________。
③1mol M在氧气中完全燃烧,最多能消耗________mol O2。
④下列有关![]() 的说法正确的是____________
的说法正确的是____________
a.能使酸性KMnO4溶液褪色 b.核磁共振氢谱有四组吸收峰 c.属于烯烃
(2)1928年,狄尔斯和阿尔德在研究1,3-丁二烯的性质时发现如下反应: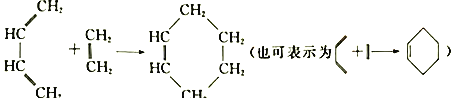 ,这种反应被称为狄尔斯一阿尔德(Diels-Alder)反应。据此回答下列问题:
,这种反应被称为狄尔斯一阿尔德(Diels-Alder)反应。据此回答下列问题:
①现有反应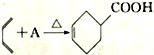 ,则物质A的结构简式为___________________。
,则物质A的结构简式为___________________。
②物质 与物质
与物质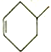 发生“Diels- Alder反应”的生成物为______________________。
发生“Diels- Alder反应”的生成物为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某CaCl2样品可能混有FeCl3、MgCl2、NaCl、Na2CO3中的一种或两种,取11.1克样品溶解,得无色溶液,再加入足量AgNO3溶液,得27.7克沉淀,由此可知样品中所含杂质的正确结论是
A.一定无Na2CO3,一定有MgCl2 B.一定无Na2CO3,一定有NaCl
C.一定有MgCl2,可能有NaCl D.一定有FeCl3,可能有NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】市售一种可充电电池,由LaNi5H6、NiO(OH)、KOH溶液组成。LaNi5H6+6Ni(OH)![]() LaNi5+6Ni(OH)2有关该电池的叙述正确的是:
LaNi5+6Ni(OH)2有关该电池的叙述正确的是:
A. 放电时,负极反应为LaNi5H6+6OHˉ-6eˉ=LaNi5+6H2O
B. 放电时,负极材料是Ni(OH)2
C. 充电时,阴极反应为Ni(OH)2+OHˉ-eˉ=NiO(OH)+H2O
D. 充电时,电池负极接充电器电源的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1L0.100mol·L-1的H2C2O4溶液中加入NaOH固体的过程中,部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的关系一定不正确的是

A. pH=3的溶液中:c(H2C2O4)+c(C2O42-)<c(HC2O4ˉ)
B. c(HC2O4ˉ)=c(C2O42-)的溶液中:c(Na+)<0. 100 mol·L-1+c(HC2O4ˉ)
C. 随着NaOH溶液的加入,![]() 减小
减小
D. c(Na+)=0.100mol·L-1的溶液中:c(H+)+c(H2C2O4)=c(OHˉ)+c(C2O42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下可合成甲醇。
(1)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(1) △H1=-Q1kJ·mol-1
②2CO(g)+O2(g)=2CO2 (g) △H2=-Q2kJ·mol-1
③H2O(g)=H2O(1) △H3=-Q3kJ·mol-1
请写出甲醇发生不完全燃烧生成一氧化碳和气态水的热化学反应方程式:_____________。
(2)合成甲醇发生的反应如下
①CO(g)+2H2(g) ![]() CH3OH(g) △H1=-a kJ·mol-1
CH3OH(g) △H1=-a kJ·mol-1
②CO2(g)+3H2(g) ![]() CH3OH(g) +H2O(g) △H2=-b kJ·mol-1
CH3OH(g) +H2O(g) △H2=-b kJ·mol-1
③CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H3=+c kJ·mol-1
CO(g)+H2O(g) △H3=+c kJ·mol-1
I:在以上制备甲醇的两个反应中,反应①优于反应②,原因为_____________。
Ⅱ:合成气的组成![]() 时体系中的CO平衡转化率(a)与温度和压强的关系如图所示。
时体系中的CO平衡转化率(a)与温度和压强的关系如图所示。
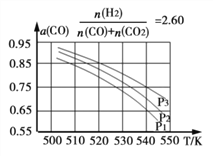
①a(CO)值随温度升高而_____________(填“增大”或“减小”),其原因是_____________
②图中的压强由大到小为_____________,其判断理由是_____________
(3)通常合成甲醇的主要反应为:CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
①在一定温度下,上述反应在一密闭容器中达到平衡,在保证H2浓度不变的情况下,增大容器的体积,平衡_____________(填字母);作出此判断的理由是_____________。
a.向正反应方向移动 b.向逆反应方向移动 c.不移动
②某温度下,将1 mol CO和4molH2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.1mol·L-1,则H2的转化率为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了使城市生活垃圾得到合理利用,减少垃圾的填埋量,近年来步实施了生活垃圾分类投放的办法。其中废旧塑料袋、废旧报纸和纸箱、废旧衣物等属于
A. 纯净物 B. 氧化物 C. 有机物 D. 非金属单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com