
����Ŀ����15�֣�ˮ���ܽ�����ˮ���������治��ȱ�ٵ�������ij����С����õ������ⶨѧУ�ܱߺ�ˮ�е��ܽ�����ʵ�鲽�輰�ⶨԭ�����£�
��ȡ�������Ĺ̶�
���ܽ���ƿ�ɼ�ˮ������¼����ѹ��ˮ���¶ȣ���ˮ����Mn��OH��2��������Һ������KI����ϣ���Ӧ����MnO��OH��2 �� ʵ�����Ĺ̶���
���ữ���ζ�
���������ˮ���ữ��MnO��OH��2��I����ԭΪMn2+ �� �ڰ�������5min��Ȼ���ñ�Na2S2O3��Һ�ζ����ɵ�I2��2S2O32��+I2=2I��+S4O62������
�ش��������⣺
��1��ȡˮ��ʱӦ���������Ŷ�ˮ����棬������������ҪĿ���� ��
��2�������Ĺ̶����з�����Ӧ�Ļ�ѧ����ʽΪ ��
��3��Na2S2O3��Һ���ȶ���ʹ��ǰ��궨�����Ƹ���Һʱ��Ҫ�IJ����������ձ������������Լ�ƿ��������ˮ���뾭����С���ȴ�����ʹ�ã���Ŀ����ɱ��������������̼��
��4��ȡ100.00mLˮ�����������ữ����a molL��1Na2S2O3��Һ�ζ����Ե�����Һ��ָʾ�����յ�����Ϊ��������Na2S2O3��Һ�����Ϊb mL����ˮ�����ܽ����ĺ���ΪmgL��1 ��
��5�������ζ���ɺ����ζ��ܼ��촦�������ݻᵼ�²������ƫ �� ����ߡ��͡���
���𰸡�
��1��ʹ�ⶨֵ��ˮ���е�ʵ��ֵ����һ�£�����������
��2��2Mn��OH��2+O2=2MnO��OH��2
��3��һ���ݻ�������ƿ����ͷ�ιܡ���Ͳ������
��4�����������һ��ʱ����Һ����ɫ��Ϊ��ɫ���Ұ�������ޱ仯��80ab
��5����
����������1��ȡˮ��ʱ�Ŷ�ˮ����棬����������ʹ�����ܽ�ȼ�С��Ϊ�ˣ�ȡˮ��ʱӦ���������Ŷ�ˮ����棬������������ҪĿ����ʹ�ⶨֵ��ˮ���е�ʵ��ֵ����һ�£����������
�ʴ�Ϊ��ʹ�ⶨֵ��ˮ���е�ʵ��ֵ����һ�£������������2�������Ĺ̶����з�����Ӧ�Ļ�ѧ����ʽΪ��2Mn��OH��2+O2=2MnO��OH��2 ��
�ʴ�Ϊ��2Mn��OH��2+O2=2MnO��OH��2����3������ˮ���뾭����С���ȴ�����ʹ�ã���Ŀ����ɱ������������������̼��
�ʴ�Ϊ����������4���������۱���ɫ����ѡ�������ָʾ��������Һ����ɫ��Ϊ��ɫ���Ұ������ɫ���ٱ仯˵���ζ������յ㣻���ݷ���ʽ��O2��2I2��4S2O32����n��O2��= ![]() mol��m��O2��=
mol��m��O2��= ![]() =8abmg����ˮ�����ܽ����ĺ���Ϊ��
=8abmg����ˮ�����ܽ����ĺ���Ϊ�� ![]() =80abmg��L��1 ��
=80abmg��L��1 ��
�ʴ�Ϊ�����������һ��ʱ����Һ����ɫ��Ϊ��ɫ���Ұ�������ޱ仯��80abmg��L��1����5������n��O2��= ![]() mol����������������b��Ӱ�죬bֵ��С����ᵼ�²������ƫ�ͣ�
mol����������������b��Ӱ�죬bֵ��С����ᵼ�²������ƫ�ͣ�
�ʴ�Ϊ���ͣ�
��1���ɼ���ˮ�����ܽ������������������ر����¶Ⱥ�ѹǿ���ı����ܽ�ȷ����ı䣻��2�������Ĺ̶����ķ����ǣ���Mn��OH��2��������Һ������KI����ˮ����ϣ���Ӧ����MnO��OH��2 �� ʵ�����Ĺ̶�����3�����ʵ���Ũ�ȵ�����ʵ�飬ʹ�õ������У��ձ�����������һ���ݻ�������ƿ����ͷ�ιܡ���Ͳ����ˮ���е������ʱ���ʹ�õ�����ˮ�ܽ���������4���������۱���ɫ����ѡ�������ָʾ��������Һ����ɫ��Ϊ��ɫ���Ұ������ɫ���ٱ仯˵���ζ������յ㣻���ݷ���ʽ�� I2��S2O32��֮��Ĺ�ϵʽ���㣻��5������n��O2��= ![]() mol����������������b��Ӱ�죬�Դ��жϲ����������
mol����������������b��Ӱ�죬�Դ��жϲ����������


 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����14�֣�H2S��SO2��Ի��������彡�����������Σ������ҵ�ϲ�ȡ���ַ���������Щ�к�������ŷţ��ش����з����е����⣮
��H2S�ij�ȥ
����1��������H2S��ԭ��Ϊ��
H2S+Fe2��SO4��3�TS��+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 ![]() 2Fe2��SO4��3+2H2O
2Fe2��SO4��3+2H2O
��1����˾�����ʱ��FeSO4����������������ʱ��5��105�����þ��������� ��
��2����ͼ1��ͼ2�ж�ʹ����˾����������Ϊ �� ����Ӧ�¶ȹ��ߣ���Ӧ�����½�����ԭ���� �� 
��3������2����һ�������£���H2O2����H2S
���Ųμӷ�Ӧ��n��H2O2��/n��H2S���仯���������ﲻͬ����n��H2O2��/n��H2S��=4ʱ����������ķ���ʽΪ ��
��4����SO2�ij�ȥ
����1��˫�������NaOH����SO2 �� ����CaOʹNaOH����
NaOH��Һ ![]() Na2SO3��Һ
Na2SO3��Һ
д�����̢ٵ����ӷ���ʽ����CaO��ˮ�д�������ת����
CaO��s��+H2O ��l���TCa��OH��2��s��Ca2+��aq��+2OH����aq��
��ƽ���ƶ��ĽǶȣ��������̢�NaOH������ԭ�� ��
��5������2���ð�ˮ��ȥSO2
��֪25�棬NH3H2O��Kb=1.8��10��5 �� H2SO3��Ka1=1.3��10��2 �� Ka2=6.2��10��8 �� ����ˮ��Ũ��Ϊ2.0molL��1 �� ��Һ�е�c��OH����=molL��1 �� ��SO2ͨ��ð�ˮ�У���c��OH��������1.0��10��7 molL��1ʱ����Һ�е�c��SO32����/c��HSO3����= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤����������ֵ������˵����ȷ���ǣ�������
A.23 g Na������H2O��Ӧ��ȫ�������NA��H2����
B.1 mol Cu��������Ũ���ᷴӦ������NA��SO3����
C.��״���£�22.4 L Cl2��NA��ԭ��
D.3 mol����Fe��ȫת��ΪFe3O4 �� ʧȥ8 NA������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D���ֶ�����Ԫ�ص�ԭ��������������B�ĺ˵������A��D�˵����֮�͵� ![]() ��A�ֱܷ���B��C��D�γɵ���������ȵķ���X��Y��Z���ش��������⣺
��A�ֱܷ���B��C��D�γɵ���������ȵķ���X��Y��Z���ش��������⣺
��1��B��D��Ԫ�ص����Ʒֱ����� ��
��2��������B2A2�ĵ���ʽΪ ��
��3��Y��C������������ˮ����պ���ȫ��Ӧʱ�����������ˮ��Һ���ԣ���ᡱ��������С�����ԭ���ǣ��������ӷ���ʽ��ʾ����
��4���ڣ�3�������������ˮ��Һ�У��������¹�ϵ��������Ũ�ȷ�����д�� ��c��H+��+=c��OH����+��
��c��H+��=c��OHһ��+ ��
��5����X��D2��NaOH��Һ�Ͷ��Ե缫�����һ��ȼ�ϵ�أ���ȼ�ϵ�ص� ������ӦΪ�� ��
������ӦΪ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����߸�ţ������������������������Ʒ�����е���������������ָ���ǣ� ��
A. ����B. ������C. ����D. Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����15�֣��ҹ���ѧ������ɹ��ϳ������������嵪�������Σ�N5��6��H3O��3��NH4��4Cl����R���������ش��������⣺
��1����ԭ�Ӽ۲���ӶԵĹ������ʽ�������Ų�ͼ��Ϊ ��
��2��Ԫ�صĻ�̬��̬ԭ�ӵõ�һ�������γ���̬��һ������ʱ���ų�������������һ�������ܣ�E1�����ڶ����ڲ���Ԫ�ص�E1�仯������ͼ��a����ʾ�� 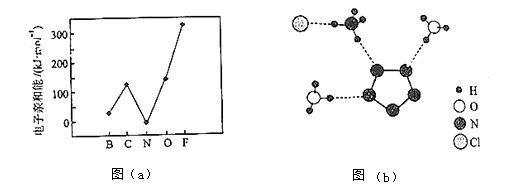
���г���Ԫ���⣬����Ԫ�ص�E1����������������ԭ��������Ԫ�ص�E1�����쳣��ԭ���� ��
��3����X���������û�����R�ľ���ṹ����ֲ��ṹ��ͼ��b����ʾ��
�ٴӽṹ�Ƕȷ�����R�����������ӵ���֮ͬ��Ϊ �� ��֮ͬ��Ϊ �� �����ţ�
A������ԭ�ӵ��ӻ��������
B������ԭ�ӵļ۲���Ӷ���
C������ṹ
D�����ۼ�����
��R��������N5���еĦҼ�����Ϊ���������еĴ�м����÷��Ŧ�mn��ʾ������m���������γɵĴ�м�ԭ������n���������γɵĴ�м����������籽�����еĴ�м��ɱ�ʾΪ��66������N5���еĴ�м�Ӧ��ʾΪ ��
��ͼ��b�������ߴ�����������ʾʽΪ��NH4+��N��H��Cl���� ��
��4��R�ľ����ܶ�Ϊdgcm��3 �� ��������������Ϊanm�������к���y��[��N5��6��H3O��3��NH4��4Cl]��Ԫ���õ�Ԫ���������ΪM����y�ļ������ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������4����ѧ��Ӧ��������3����Ӧ���Ͳ�ͬ���ǣ� ��
A.CH2�TCH��CH3+HCl ![]() CH3CHCH3Cl
CH3CHCH3Cl
B.CH3CHO+H2 ![]() CH3CH2OH
CH3CH2OH
C.CH3CH2Br+NaOH ![]() CH2�TCH2��+NaBr+H2O
CH2�TCH2��+NaBr+H2O
D.CH��CH+Br2�� 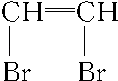
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л�������У�����ԭ��һ������ͬһƽ����ǣ� ��
A.CH3��CH=CH2
B.![]()
C.CH3��CH3
D.![]()
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com