
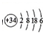 的元素,位于元素周期表的( )
的元素,位于元素周期表的( )| A. | 第六周期第IV族 | B. | 第四周期第VI族 | C. | 第六周期第A族 | D. | 第四周期第VIA族 |
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 金属钠保存在煤油中 | B. | 保存氯化亚铁溶液时加入少量铁粉 | ||
| C. | 过氧化钠应密封保存 | D. | 氢氟酸保存在玻璃试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去FeCl3溶液中的FeCl2杂质可以向溶液中通入氯气 | |
| B. | 铁与水蒸气在高温下的反应产物为Fe2O3和H2 | |
| C. | Fe3O4为红棕色晶体 | |
| D. | Fe(OH)2和Fe(OH)3都能在空气中稳定存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | x为NaOH溶液,y为盐酸 | |
| B. | a→b发生的反应为:AlO2-+H++H2O═Al(OH)3↓ | |
| C. | b→c→Al的反应条件分别为:加热、电解 | |
| D. | a、b、c既能与酸又能与碱反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{1}^{2}$H和D | B. | O2和O3 | ||
| C. | ${\;}_{92}^{235}$U和${\;}_{92}^{238}$U | D. | H2O和D2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;画出碳原子结构示意图
;画出碳原子结构示意图 ;氧元素位于周期表第周期第VIA族.
;氧元素位于周期表第周期第VIA族.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24g | B. | 3.36g | C. | 5.60g | D. | 10.08g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=3的醋酸溶液稀释100倍后,溶液的pH=5 | |
| B. | pH=2的盐酸与等体积0.01mol•L-1醋酸钠混合溶液后,溶液中c(Cl-)=c(CH3COO-) | |
| C. | 0.1mol AgCl和0.1mol AgI混合后加入1L水中,所得溶液中c(Cl-)>c(I-) | |
| D. | 氨水中通入过量CO2后,溶液中c(H+)+c(NH4+)=c(OH-)+c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯(硝基苯):加少量水振荡,待分层后分液 | |
| B. | 乙烷(乙烯):光照条件下通入Cl2,气液分离 | |
| C. | 苯(苯酚):加入浓溴水,振荡、静置、过滤 | |
| D. | 乙醇(乙酸):加足量生石灰,蒸馏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com