
【题目】【选做-选修3:物质结构与性质】硒化锌是一种半导体材料,回答下列问题。
(1)锌在周期表中的位置_______;Se基态原子价电子排布图为______。元素锌、硫和硒第一电离能较大的是________(填元素符号)。
(2)Na2SeO3分子中Se原子的杂化类型为_______;H2SeO4的酸性比H2SeO3强,原因是_______。
(3)气态SeO3分子的立体构型为_______;下列与SeO3互为等电子体的有__(填序号)。
A.CO32- B.NO3- C.NCl3 D.SO32-
(4)硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为______(填元素符号);该晶胞中硒原子所处空隙类型为_____(填“立方体”、“正四面体”或正八面体”);若该品晶胞密度为ρg/cm3,硒化锌的摩尔质量为Mg/mol。用NA代表阿伏加德罗常数的数值,则晶胞参数a为_______nm。

【答案】 第四周期IIB族 ![]() S sp3 H2SeO4的非羟基氧比H2SeO3多(或H2SeO4中Se的化合价更高) 平面三角形 AB Zn 正四面体
S sp3 H2SeO4的非羟基氧比H2SeO3多(或H2SeO4中Se的化合价更高) 平面三角形 AB Zn 正四面体 ![]()
【解析】(1)Zn锌的原子序数是30,其电子排布式为1S22S22P63S23P63d104S2,在周期表中的位置第四周期IIB族;Se原子序数是34,原子核外有34个电子,最外层电子排布式为4S24P6,基态原子价电子排布图为![]() 。元素锌金属性较强,第一电离能较小,硫和硒为同主族元素,同主族元素由上到下非金属性逐渐减弱,所以硫的非金属性强于Se,所以第一电离最大的是S。
。元素锌金属性较强,第一电离能较小,硫和硒为同主族元素,同主族元素由上到下非金属性逐渐减弱,所以硫的非金属性强于Se,所以第一电离最大的是S。
(2) Na2SeO3分子中Se原子的价电子对数为;(6+2)/2=4,所以Se原子的杂化类型为sp3;H2SeO4的非羟基氧比H2SeO3多(或H2SeO4中Se 的化合价更高),所以H2SeO4酸性比H2SeO3 强;答案:sp3 . H2SeO4的非羟基氧比H2SeO3多(或H2SeO4中Se 的化合价更高) 。
(3)气态SeO3分子的价层电子对数为3,Se没有孤对电子,故分子的立体构型为平面三角形;等电子体要求原子总数相同,价电子数相同,所以与SeO3互为等电子体的离子由有A.CO32-、B.NO3-。答案:AB。
(4)硒化锌的晶胞结构中原子个数比为1;1,其中Se原子4个,若X和Y点所堆积的原子均为锌原子,则8![]() +6
+6![]() 1/2=4,符合;则图中X和Y点所堆积的原子均为Zn原子,根据图中原子的位置可知,该晶胞中硒原子所处空隙类型为正四面体;若该品晶胞密度为ρg/cm3,硒化锌的摩尔质量为Mg/mol。用NA代表阿伏加德罗常数的数值,根据p=m/v=4M/(NA.V),则V=4M/PnA,则晶胞的边长为a为
1/2=4,符合;则图中X和Y点所堆积的原子均为Zn原子,根据图中原子的位置可知,该晶胞中硒原子所处空隙类型为正四面体;若该品晶胞密度为ρg/cm3,硒化锌的摩尔质量为Mg/mol。用NA代表阿伏加德罗常数的数值,根据p=m/v=4M/(NA.V),则V=4M/PnA,则晶胞的边长为a为![]() nm。
nm。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案科目:高中化学 来源: 题型:
【题目】氢气是一种清洁能源,氢气的制取和储存是氢能源利用领域的研究热点。
(1)H2S 热分解制氢的原理: 2H2S(g)=2H2(g) + S2(g) △H= 169.8 kJ/mol,分解时常向反应器中通入一定比例空气,使部分H2S 燃烧,其目的是______;燃烧生成的SO2与H2S 进一步反应,硫元素转化为S2,写出反应的化学方程式:________。
(2)氨硼烷(NH3BH3) 是储氢量最高的材料之一,其受热时固体残留率随温度的变化如图甲所示。氨硼烷还可作燃料电池,其工作原理如图乙所示。

①110℃时残留固体的化学式为_________。
②氨硼烷电池工作时负极的电极反应式为_________。
(3)十氢萘(C10H18)是具有高储氢密度的氢能载体,经历“C10H18- C10H12-C10H8”的脱氢过程释放氢气。己知:
C10H18(l)![]() C10H12(l) +3H2(g) △H1
C10H12(l) +3H2(g) △H1
C10H12(l)![]() C10H8(l)+2H2(g) △H2
C10H8(l)+2H2(g) △H2
温度335℃、高压下,在恒容密闭反应器中进行液态十氢萘( 1.00 mol) 催化脱氢实验,测得C10H12和C10H8的物质的量n1 和n2随时间的变化关系如图丙所示。图丁表示催化剂对反应活化能的影响。
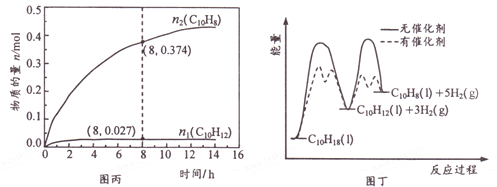
①△H1___△H2(选填“>”、“=”或“<”)。
② 8 h 时,反应体系内氢气的物质的量为_____mol(忽略其他副反应)。
③ n1 显著低于n2 可能的原因是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香烃化合物A(C9H12O)常用于药物及香料的合成,A的苯环上只有一个支链,支链上只有两种不同环境的氢原子,A有如下转化关系:

已知以下信息:
①
②![]()
请回答下列问题:
(1)A生成B的反应类型为________,由D生成E的反应条件为___________。
(2)F的官能团名称为________,_____________。
(3)I的结构简式为______________。
(4)由E生成F的反应方程式为________________。
(5)F有多种同分异构体,写出符合下列条件的同分异构体的结构简式为______________。
①能发生水解反应和银镜反应;
②属于芳香族化合物且分子中只有一个甲基;
③具有5个核磁共振氢谱峰
(6)糠叉丙酮(![]() )是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇(CH3)3COH]和糠醛(
)是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇(CH3)3COH]和糠醛(![]() )为原料制备糠叉丙酮的合成路线(无机试剂任用,用结构简式表示有机物),用箭头表示转化关系,箭头上往明试剂和反应条件)。_________________
)为原料制备糠叉丙酮的合成路线(无机试剂任用,用结构简式表示有机物),用箭头表示转化关系,箭头上往明试剂和反应条件)。_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃的分子球棍模型(如图),据此回答下列问题:


(1)常温下含碳量最高的气态烃是________(填字母)。
(2)E的一氯取代物同分异构有_______种。
(3)一卤代物种类最多的是________(填写字母)。
(4)能够与Br2发生加成反应的两种气态烃是________(填写字母)。
(5)写出C的加聚反应的化学方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的离子能大量共存且溶液呈无色的是( )
A.Na+、Ba2+、Cl-、SO42-B.Cu2+、H+、NO3-、SO42-
C.H+、Fe2+、NO3-、SO42-D.Na+、Ca2+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【选做-选修5: 有机化学基础】PET和PMMA是日常生活常见的两种高分子材料。下列是合成高分子材料的路线:

已知:①RCOOR1+R2OH![]() RCOOR2+R1OH
RCOOR2+R1OH
② (R1、R2表示烃基或氢原子)
(R1、R2表示烃基或氢原子)
回答下列问题:
(1)物质A的化学名称_______,物质H中官能团的名称________。
(2)由C生成D、I生成J的反应类型分别是_______、_______。
(3)由I生成J的反应中产生六元环的副产物,其结构简式为_______。
(4)写出D+乙二醇→F+G的化学反应方程式________________。
(5)D存在多种同分异构体,其中只含有一种官能团的三取代芳香族化合物且能与碳酸氢钠溶液作用产生气体的同分异构体有____种。
(6)写出用环己醇为原料制备 的合成路线(其他试剂任选)_________。
的合成路线(其他试剂任选)_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】比亚迪纯电动汽车采用一种具有高效率输出、可快速充电、对环境无污染等优点新型电池,其工作原理如图。M电极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,聚合物交换膜只允许Li+通过,而e-不能通过。电池反应式为LixC6+Li1-xFePO4![]() LiFePO4+6C。下列说法不正确的是
LiFePO4+6C。下列说法不正确的是

A. 放电时,N极是正极,电极反应式为Li(1-x)FePO4+xLi++xe-=LiFePO4
B. 充电时,Li+通过聚合物交换膜向M极迁移
C. 用该电池电解精炼铜,阴极质量增重19.2g时,通过聚合物交换膜的Li+数目为0.6NA
D. 充电时电路中通过0.5mol e-,消耗36gC
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列冶炼金属的方法错误的是( )
A.电解熔融NaCl制钠
B.加热HgO制汞
C.高温下用CO还原Fe2O3制铁
D.高温下用H2还原Al2O3制铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为泡沫灭火器构造示意图,内筒a装有Al2(SO4)3溶液,外筒b装有饱和NaHCO3溶液。结合生活中的应用,下列分析错误的是

A. 使用时必须将泡沫灭火器倒立
B. 工作时HCO3-水解较彻底
C. 灭火时产生的Al(OH)3覆盖可燃物有利于阻隔氧气
D. 该灭火器可用于扑灭Na等金属着火
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com