
| A. | CH2=CH2 | B. | CH≡C-CH3 | C. | CH2=CH-CH=CH2 | D. | CH3-CH=CH2 |
分析 气态烃1mol最多可与2molHBr加成,说明分子中含有2个C=C或1个C≡C键,所得产物与Cl2发生取代反应时,若将氢原子全部取代,需要8mol Cl2,说明加成产物含有8个H,其中有2个H为与HBr加成生成,则原烃中含有H为6,可用排除法解答该题.
解答 解:某气态烃1mol最多和2mol HBr发生加成反应,说明分子中含有1个C≡C或2个C=C键,所得产物又能与8mol氯气发生取代反应,说明加成产物中含有8个H原子,则该气态烃应含有6个H原子,
A.乙烯的分子式为C2H4,分子中含4个氢原子,不符合条件,故A错误;
B.丙炔分子式为C3H4,H原子数不符合,故B错误;
C.CH2═CH-CH═CH2分子中含有两个碳碳双键,且含有6个H,满足条件,故C正确;
D.丙烯分子式为C3H6,含有1个碳碳双键,不满足条件,故D错误;
故选C.
点评 本题考查有机物分子式确定的计算,题目难度中等,注意熟练掌握常见有机物结构与性质,明确取代反应与加成反应实质的实质为解答关键,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将废旧电池集中深埋,防止重金属污染 | |
| B. | 改善能源结构,大力发展太阳能、风能等清洁能源 | |
| C. | 推广碳捕集和转化成化工原料技术,逐步实现二氧化碳零排放 | |
| D. | 采用纳米TiO2光触媒技术,将装修材料中释放的HCHO转化为无害物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaO | B. | Na2CO3 | C. | SiO2 | D. | CaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
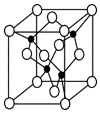 X、Y、Z、U、W 是原子序数依次增大的前四周期元素.其中 Y 的原子核外有 7 种运动状态不同的 电子;X、Z 中未成对电子数均为 2;U 是第三周期元素形成的简单离子中半径最小的元素;W 的内层电 子全充满,最外层只有 1 个电子.请回答下列问题:
X、Y、Z、U、W 是原子序数依次增大的前四周期元素.其中 Y 的原子核外有 7 种运动状态不同的 电子;X、Z 中未成对电子数均为 2;U 是第三周期元素形成的简单离子中半径最小的元素;W 的内层电 子全充满,最外层只有 1 个电子.请回答下列问题: .
.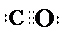 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 过氧乙酸(
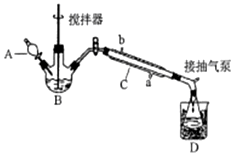
过氧乙酸( 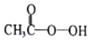 )是一种常见消毒剂,具强氧化性,减压蒸馏法制备过氧乙酸的步骤及装置如图:
)是一种常见消毒剂,具强氧化性,减压蒸馏法制备过氧乙酸的步骤及装置如图:| 反应物比例 CH3COOH/H2O2 | 反应时间(小时) | ||||
| 0.5 | 1 | 3 | 5 | 7 | |
| 2:1 | 7.38 | 8.46 | 9.42 | 11.26 | 13.48 |
| 1:1 | 10.56 | 12.92 | 13.54 | 20.72 | 20.70 |
| 1:2 | 6.14 | 7.10 | 7.96 | 10.38 | 12.36 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
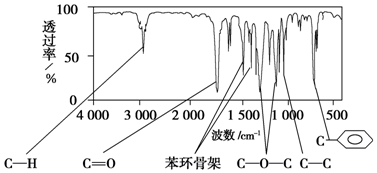
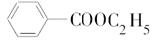 .
.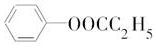 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
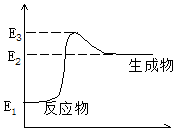 C(s)+H2O(g)→CO(g)+H2(g)+Q,反应过程中能量(E)的变化如图所示,下列说法正确的是( )
C(s)+H2O(g)→CO(g)+H2(g)+Q,反应过程中能量(E)的变化如图所示,下列说法正确的是( )| A. | 减小压强时,Q的值增大 | B. | 升高温度时,Q的值减小 | ||
| C. | 该反应是吸热反应 | D. | Q=E3-E1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 医学上可用碳酸钡代替硫酸钡用作“钡餐” | |
| B. | 生理盐水用于医疗输液是因为它属于强电解质 | |
| C. | 医学上用液氮作制冷剂是因为液氮的沸点很低 | |
| D. | 水中的钢闸门连接电源负极,利用了牺牲阳极的阴极保护法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com