
已知有下图所示物质相互转换关系

试回答:
(1)写出B的化学式 ,D的化学式 。
(2)写出由E转变成F的现象 ;其发生反应的化学方程式________。
(3)鉴别B溶液中阳离子的操作方法及实验现象__________________;
(4)向G溶液中加入A的离子方程式________
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
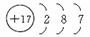
请回答下列问题:
(1)写出Z的原子结构示意图____________________________。
(2)写出图中D的电子式____________________________。
(3)确定图中单质F的依据是____________________________。
(4)利用图中反应③在标准状况下生成
(5)写出图中G溶液与H溶液相混合发生反应的离子方程式__________________________。
(6)如下图所示装置,两玻璃管中盛有A饱和溶液,两极为多孔石墨电极,给两极分别通入X2、Z2气体,电流表的指针发生偏转;通入X2气体的电极名称是_________________(填写“正极”或“负极”);通入Z2气体的电极反应式为____________________________。
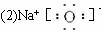
查看答案和解析>>
科目:高中化学 来源: 题型:

请回答下列问题:
(1)写出Z的原子结构示意图_______________。
(2)写出图中D的电子式_______________。
(3)确定图中单质F的依据是_______________。
(4)利用图中反应③在标准状况下生成
(5)写出图中G溶液与H溶液相混合发生反应的离子方程式_______________。
(6)如下图所示装置,两玻璃管中盛有A饱和溶液,两极为多孔石墨电极,给两极分别通入X2、Z2气体,电流表的指针发生偏转;通入X2气体的电极名称是_______________(填写“正极”或“负极”);通入Z2气体的电极反应式为_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
请从给出的3道化学题中任选一题做答
1.[化学——选修化学与技术]
请回答氯碱工业中的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k__________(要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、 等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是_________(填序号);
等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是_________(填序号);
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。

①图中X、Y分别是_________、_________(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________;
②分别写出燃料电池B中正极、负极上发生的电极反应
正极:_________;负极:_________;
③这样设计的主要节(电)能之处在于(写出2处)
___________________________、___________________________。
2.[化学——选修物质结构与性质]
已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为_________,该元素的符号为_________;
(2)Y元素原子的价层电子的轨道表示式为_________,该元素的名称是_________;
(3)X与Z可形成化合物XZ3,该化合物的空间构型为________________________;
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是____________________________________;
(5)比较X的氢化物与同族第二、三周期元素所形成的氢化物稳定性、沸点高低并说明理由____________________________________。
3.[化学——选修有机化学基础]
A~J均为有机化合物,它们之间的转化如下图所示:

实验表明:
①D既能发生银镜反应,又能与金属钠反应放出氢气;
②核磁共振氢谱表明F分子中有三种氢,且其峰面积之比为1∶1∶1;
③G能使溴的四氯化碳溶液褪色;
④1 mol J与足量金属钠反应可放出22.4 L氢气(标准状况)。
请根据以上信息回答下列问题:
(1)A的结构简式为_________(不考虑立体异构),由A生成B的反应类型是_________反应;
(2)D的结构简式为___________________________;
(3)由E生成F的化学方程式为____________,E中的官能团有____________(填名称),与E具有相同官能团的E的同分异构体还有____________(写出结构简式,不考虑立体异构);
(4)G的结构简式为____________________________________;
(5)由I生成J的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)
已知A、B、C、D四种短周期元素在元素周期表中的相对位置如下图所示,它们的原子序数之和为46。请填空:
(1)C元素的元素符号为 D元素的原子结构示意
图 。
(2)A元素可以形成多种同素异形体,其中硬度最大、不导电的是 (填物质的名称),其中形似足球的是 (填化学式)。
(3)B有多种氧化物,其中之一是一种无色气体。该气体在空气中会迅速变成红棕色,在一定条件下,4 L的该无色气体与3 L的氧气相混合,被足量的水完成吸收,且只生成一种B的含氧酸,该含氧酸的化学式为 。
(4)离子半径:D﹣ C2﹣(填“>”、“<”、“=”)。
还原性:D﹣ C2﹣(填“>”、“<”、“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(14分)夜幕降临,北京奥运会主会场“鸟巢”内灯火辉煌,鼓瑟齐鸣。璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应。鸟巢夜景照明由五个部分组成,其中主体照明以传统文化元素“中国红”为主色。请回答下列问题:
⑴火焰利用了部分金属的元素特征的 反应,该反应属于 (填“物理”或“化学”)变化。
⑵下图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2。根据以上信息回答下列问题:
①B的水溶液呈弱酸性,是二元弱酸,其主要的电离方程式可表示为__________
D的化学式是_____ ____。②A、B、E中均含有的一种元素为____________ (填元素名称) 。
③E电子式为____________________。
④NH3分子中的N原子有一对孤对电子,能发生反应:NH3+HCl=NH4Cl。试写出E与足量盐酸时,发生反应的化学方程式
。
⑶在实验室我国科研人员应用电子计算机模拟出具有高能的物质N60,它的结构与C60十分相似。已知N60分子中每个N原子均以氮氮单键结合三个氮原子,且N60结构中每个氮原子均形成8个电子的稳定结构。试推测1个N60分子的结构中含有_________个N—N。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com