
【题目】现有甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时 间长短来探究影响 H2O2 分解速率的因素(仅一个条件改变)。甲小组有如下实验设计方 案。
实验编号 | 温度 | 催化剂 | 浓度 |
甲组实验Ⅰ | 25 ℃ | 三氧化二铁 | 10 mL 5% H2O2 |
甲组实验Ⅱ | 25 ℃ | 二氧化锰 | 10 mL 5% H2O2 |
甲、乙两小组得出如下图数据。

(1)甲小组实验得出的结论是_____。
(2) 由乙组研究的酸、碱对 H2O2 分解影响因素的数据分析,相同条件下 H2O2 在______(填“酸”或“碱”)性环境下放出气体速率较快;由此,乙组提出可以用BaO2 固体与硫酸溶液反应制 H2O2,其反应的离子方程式为___________________________;支持这一方案的理由是_____。
(3)已知过氧化氢是一种极弱的二元酸:H2O2![]() H++HO2- (Ka1=2.4×10-12)。当稀 H2O2溶液在碱性环境下分解时会发生反应 H2O2+OH-
H++HO2- (Ka1=2.4×10-12)。当稀 H2O2溶液在碱性环境下分解时会发生反应 H2O2+OH-![]() HO2-+H2O,该反应中,正反应速率为 v 正=k正·c(H2O2)·c(OH-),逆反应速率为 v 逆=k 逆·c(H2O)·c(HO2- ),其中 k 正、k 逆为速率常数,则 k 正与 k 逆的比值为_________________________________________(保留 3 位有效数字)。
HO2-+H2O,该反应中,正反应速率为 v 正=k正·c(H2O2)·c(OH-),逆反应速率为 v 逆=k 逆·c(H2O)·c(HO2- ),其中 k 正、k 逆为速率常数,则 k 正与 k 逆的比值为_________________________________________(保留 3 位有效数字)。
【答案】H2O2 分解时,MnO2 比 Fe2O3 催化效率更高 碱 BaO2+2H+SO42-===BaSO4+H2O2 BaSO4 的生成使平衡右移,有利于 H2O2 的生成,酸性环境有利于 H2O2 的存在 1.33×104
【解析】
(1)在体积-时间图中,斜率即可代表化学反应速率,甲组实验Ⅰ、II催化剂不同;
(2)由乙组研究的酸、碱对H2O2分解影响因素的数据分析可知碱性越强,放出气体的速率越快;根据BaO2固体与硫酸溶液反应制H2O2和硫酸钡进行解答;
(3)根据Ka1、Kw、以及V正、v逆公式进行计算。
(1)由图象可知在体积-时间图,斜率即可代表化学反应速率,由甲组实验两条曲线可知,甲组实验Ⅱ斜率大,因此分解速率越快,说明H2O2分解时,MnO2比Fe2O3催化效率更高;
(2)由乙组研究的酸、碱对H2O2分解影响因素的数据分析可知碱性越强,放出气体的速率越快,由题意知BaO2固体与H2SO4溶液反应制H2O2的反应物为BaO2和H2SO4,产物为H2O2,根据原子守恒可知另一种产物为硫酸钡,即:BaO2+H2SO4=H2O2+BaSO4,离子方程式为:BaO2+2H++SO42-═BaSO4+H2O2,由图可知酸性条件下,H2O2分解的速率慢,相同条件下H2O2在碱性条件下反应速率快,可能BaSO4的生成有利于平衡右移即有利于H2O2的生成,或酸性环境有利于H2O2的存在;
(3)水的物质的量浓度为55.6 mol/L,![]() =
=![]() =
=![]() =
=![]() ≈1.33×104。
≈1.33×104。


科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1 mol·L1稀盐酸,CO2的生成量与加入盐酸的体积的关系如图。下列判断正确的是
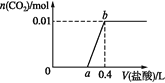
A. 在0~a范围内,只发生中和反应
B. ab段发生反应的离子方程式为:![]()
C. a=0.3
D. 原混合溶液中NaOH与Na2CO3的物质的量之比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下列物质中:
(1)互为同分异构体的有_______ (2)互为同素异形体的有_______
(3)属于同位素的有__________ (4)属于同一种物质的有______。(填序号)
①液氯和氯气 ②白磷和红磷 ③ 和
和![]() ④3717Cl和3517Cl ⑤(CH3)2CHCH3和CH3(CH2)2CH3 ⑥ CH4和CH3CH2CH3
④3717Cl和3517Cl ⑤(CH3)2CHCH3和CH3(CH2)2CH3 ⑥ CH4和CH3CH2CH3
Ⅱ.现有6种物质:①MgCl2 ②HCl ③SO2 ④K2CO3 ⑤CaO ⑥NaOH。请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物是_______。
(2)含共价键的离子化合物是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸铝广泛用于化工、石油等生产上,120150℃左右分解。在0℃时,溶解度为16g,100℃时,溶解度为18.4g。
首先用废铝渣制取AI(OH)3固体,流程如下:
![]()
(1)调节pH用_________试剂为好。某同学在减压过滤时,布氏漏斗内没有得到产品,可能原因是______________________。
然后将氢氧化铝和甲醛依次加入到质量分数为50%的过氧化氢溶液中(投料物质的量之比依次为1∶3∶2),装置如图1.最终可得到含甲酸铝90%以上的优质产品。反应式为:2Al(OH)3+6HCHO+3H2O2=2Al(HCOO)3+6H2O+3H2↑。

(2)反应过程可看作两步进行,第一步______________(写出化学方程式),第二步为甲酸与Al(OH)3 反应生成甲酸铝。
(3)反应温度最好控制在30—70℃之间,温度不宜过高,主要原因是_________________。
(4)实验时需强力搅拌45 min,最后将溶液____________,抽滤,洗涤,干燥得产品。可用酸性KmnO4标准溶液滴定法来测定产品纯度,滴定起始和终点的滴定管液面位置见上图2, 则消耗的酸性KmnO4标准溶液体积为__________________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学反应的理论是一个经过简化的概念模型,合理简化的概念模型是研究化学反应原理的基础。反应速率的碰撞理论提出:能引发化学反应的碰撞称为有效碰撞。
(1)图I是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是________(填“a”“b”或“c”)。
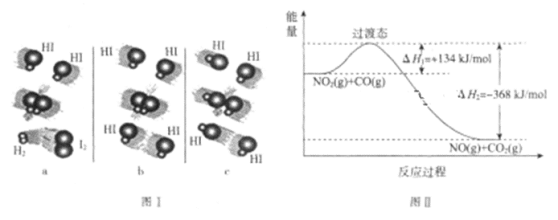
(2)过渡态理论是在碰撞理论的基础上提出的:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。根据图Ⅱ写出相应的热化学方程式:_____________________________________________ 。
(3)过渡态理论认为,催化剂改变反应速率的原因是改变了活化能从而改变了反应的途径。请在图Ⅱ中画出该反应在其他条件不变,仅使用催化剂而使反应速率加快的能量变化示意图。________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对反应类型的判断不正确的是
A. CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag↓+3NH3+H20 氧化反应
CH3COONH4+2Ag↓+3NH3+H20 氧化反应
B. ![]() 聚合反应
聚合反应
C.  取代反应
取代反应
D.  消去反应
消去反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com