
���� ��1�����ݻ�ѧƽ�ⳣ������ɵ�K�ı���ʽ�������¶ȶԻ�ѧƽ���Ӱ��ɵã�
��2�����º����£�2molZ��ȫת������ߣ��ɵ�2molX2��1molY2������ԭƽ��Ϊ��Чƽ�⣬ƽ��ʱZ��Ũ����ͬ��ͬһ���淴Ӧ����ͬ�¶��£������淴Ӧ�ķ�Ӧ����ֵ��ȣ��������෴����ƽ��ʱZ�����ʵ���Ϊnmol�����ݷ�Ӧ�ȼ����������̵�������ֵ���ݴ��жϣ�
��3�����ݻ�ѧƽ��ʱ�����淴Ӧ������ȣ�����ֵĺ������ֲ�������жϣ�
��4��ԭƽ���淴Ӧ���У�ѹǿ���ͣ���ѹ��������Ӧ����ʼ�����ͬ������ͬ�¶�����ʼ����2molX2��1molY2����ЧΪ��ԭƽ��Ļ���������ѹǿ��ƽ�������������С�ķ����ƶ����ݴ��жϣ�
��� �⣺��1��2X2��g��+Y2��g��?2Z��g������ѧƽ�ⳣ��K=$\frac{{c}^{2}��Z��}{{c}^{2}��{X}_{2}��•c��{Y}_{2}��}$����H=-akJ•mol-1��a��0�����H��0������ӦΪ���ȷ�Ӧ�������¶ȣ������淴Ӧ�����ƶ���K����
�ʴ�Ϊ��K=$\frac{{{c^2}��Z��}}{{{c^2}��{X_2}��•c��{Y_2}��}}$������
��2�����º����£�2molZ��ȫת������ߣ��ɵ�2molX2��1molY2������ԭƽ��Ϊ��Чƽ�⣬ƽ��ʱZ��Ũ����ͬ����c��Z��=Wmol•L-1��
ͬһ���淴Ӧ����ͬ�¶��£������淴Ӧ�ķ�Ӧ����ֵ��ȣ��������෴����ƽ��ʱZ�����ʵ���Ϊnmol��
���ڷ�Ӧ2X2��g��+Y2��g��?2Z��g����H=-akJ•mol-1����b=��b=n��$\frac{a}{2}$�����ڷ�Ӧ2Z��g��?2X2��g��+Y2��g����H=akJ•mol-1��Z�ֽ�����ʵ���Ϊ��2-n��mol����c=$\frac{2-n}{2}$��a=1-n��$\frac{a}{2}$����a=b+c��
�ʴ�Ϊ��=�� a=b+c��
��3��A�����뷴Ӧ��c��Z��=2c��Y2����ƽ��ʱ��һ�������ʽ����A����
B���÷�Ӧ�Ǹ����������С�ķ�Ӧ�����ŷ�Ӧ�Ľ��У�ѹǿ��С��������ѹǿ���ֲ���ʱ��˵����Ӧƽ�⣬��B��ȷ��
C��v����X2��=2v����Y2��=v����X2�������淴Ӧ������ȣ���Ӧƽ�⣬��C��ȷ��
D����������������䣬���������������䣬����$��=\frac{m}{V}$�������ڵ��ܶ�ʼ�ղ��䣬��D����
�ʴ�Ϊ��BC��
��4��ԭƽ���淴Ӧ���У�ѹǿ���ͣ���ѹ��������Ӧ����ʼ�����ͬ������ͬ�¶�����ʼ����2molX2��1molY2����ЧΪ��ԭƽ��Ļ���������ѹǿ��ƽ�������������С�ķ����ƶ�����������Ӧ�ƶ���Y2��ת���ʱ��
�ʴ�Ϊ�����
���� ���⿼�黯ѧƽ�ⳣ����ƽ��״̬�жϣ���ѧƽ����йؼ���ȣ���Ŀ�ۺ���ǿ���Ѷ��еȣ�ע����յ�Чƽ���ԭ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Mg2++2OH-�TMg��OH��2�� Mg��NO3��2+Ba��OH��2�TMg��OH��2��+Ba��NO3��2 | |
| B�� | Fe+Cu2+�TFe2++Cu Fe+CuO�TFeO+Cu | |
| C�� | Ag++Cl-�TAgCl�� Ag2SO4+2HCl�T2AgCl��+H2SO4 | |
| D�� | CO2+2OH-�TCO32-+H2O CO2+2NH3•H2O�T��NH4��2CO3+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ƹ��ܺ���ҵ���� | |
| B�� | ��������ɫ��ѧ�������ʵ�ֻ�����ҵ���ŷ� | |
| C�� | �Ӵ����Ⱦ��ҵ���������� | |
| D�� | ���Ƶؿ���ú��ʯ�͡���Ȼ���ȿ�����Դ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
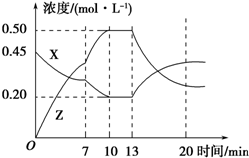
| A�� | ��X��ʾ0��10 min�ڸ÷�Ӧ��ƽ������Ϊv��X��=0.045 mol•L-1•min-1 | |
| B�� | ������ͼ����û�ѧ����ʽ��a��b=1��3 | |
| C�� | �Ʋ��ڵ�7 minʱ���߱仯��ԭ����������� | |
| D�� | �Ʋ��ڵ�13 minʱ���߱仯��ԭ������ǽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ��Ԫ�ؼ��仯���������������������Ź㷺��Ӧ�ã�
��Ԫ�ؼ��仯���������������������Ź㷺��Ӧ�ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��ѧʽ | CH3COOH | H2CO3 | AgCl | Ag2CrO4 |
| Ka��Ksp | Ka=1.8��10-5 | Ka1=4.1��10-7 Ka2=5.6��10-11 | Ksp=1.8��10-10 | Ksp=2.0��10-12 |
| A�� | �����£���ͬŨ�Ȣ�CH3COONH4 ��NH4HCO3 �ۣ�NH4��2CO3��Һ�У�c��NH4+���ɴ�С��˳���ǣ��٣��ڣ��� | |
| B�� | ����ˮ�еμ�NaOH ��Һ����Һ�պ�Ϊ����ʱ��c��Na+��=2c��ClO-��+c��HClO�� | |
| C�� | AgCl �����ڰ�ˮ������ˮ������AgCl �ڰ�ˮ�е�Ksp ����ˮ�е� Ksp | |
| D�� | ��Ũ�Ⱦ�Ϊ1��10-3mol•L-1��KCl ��K2CrO4���Һ�еμ�1��10-3mol•L-1 ��AgNO3��Һ��CrO42-���γɳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��CH3COOH ��Һ��������ʵ�飬���ݺܰ�����֤�� CH3COOH ��������� | |
| B�� | ��Ca��OH��2�ı�����Һ���ȣ�pH �� Kw������ | |
| C�� | 25��ʱ��1.0��10-3mol•L-1�����pH=3.0��1.0��10-8 mol•L-1�����pH=8.0 | |
| D�� | ��pH��ͬ�İ�ˮ������������Һ�зֱ��������NH4Cl��s��������Һ��pH����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�����Һ�ڵ��������µ����K+��Cl- | |
| B�� | Ħ���DZ�ʾ���������������Ƕ��ٵ������� | |
| C�� | ���ݶ����ЧӦ�ɽ���ɢϵ��Ϊ��Һ����������Һ | |
| D�� | ������ԭ��Ӧ�ı������е��ӵ�ת�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com