
| A. | 氯化氢的摩尔质量等于NA个氯化氢分子的质量 | |
| B. | 常温常压下1mol二氧化碳的体积大于22.4L | |
| C. | 64g金属铜发生氧化反应,一定失去2NA个电子 | |
| D. | 62g氧化钠溶于水后,所得溶液中含有NA个O2-离子 |
分析 A.摩尔质量和质量的单位不同;
B.常温常压下,温度高于标准状况,分子间距离增大1mol气体的体积大于标准状况下的气体摩尔体积;
C.铜反应后的化合价有-1、-2价;
D.Na2O溶于水后和水反应生成NaOH,故所得溶液中无O2-离子.
解答 A.氯化氢的摩尔质量为36.5g/mol,显然氯化氢的摩尔质量与NA个氯化氢分子的质量,单位不相同,故A错误;
B.常温常压下,温度高于标准状况,分子间距离增大1mol气体的体积大于标准状况下的气体摩尔体积,常温常压下,1mol CO2所占的体积大于22.4L,故B正确;
C.铜反应后生成的化合价有两种:-1、-2价,64g铜发生氧化还原反应,可能失去电子数是NA、2NA,故C错误;
D.Na2O溶于水后和水反应生成NaOH,故所得溶液中无O2-离子,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,题目难度不大.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:填空题
| 相关信息 | |
| X | 单质为双原子分子.若低温蒸发液态空气,因其沸点较低可先获得X的单质 |
| Y | 含Y元素的物质焰色反应为黄色 |
| Z | 同周期元素中原子半径最小 |
| R | R元素原子的最外层电子数是K层电子数的3倍 |
 ;
;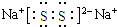 ,写出乙溶液在空气中变质过程的化学方程式4Na2S+O2+2H2O═4NaOH+2Na2S2 .
,写出乙溶液在空气中变质过程的化学方程式4Na2S+O2+2H2O═4NaOH+2Na2S2 .查看答案和解析>>
科目:高中化学 来源: 题型:选择题
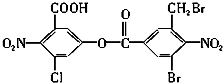 已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如下所示,1mol 该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为( )
已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如下所示,1mol 该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为( )| A. | 5 mol | B. | 6 mol | C. | 7 mol | D. | 8 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
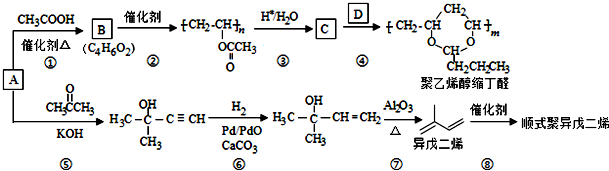
 ,B含有的含氧官能团是酯基(写名称).
,B含有的含氧官能团是酯基(写名称). ,D为CH3CH2CH2CHO.
,D为CH3CH2CH2CHO. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
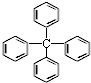
| A. | 该有机物分子式为C25H24 | |
| B. | 该多环芳烃属于稠环芳烃 | |
| C. | 该分子中最多可能有13个碳原子在同一平面上 | |
| D. | 该有机物能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用溴单质的氧化性可以把碘离子转化为碘单质 | |
| B. | 实验室常用NaOH溶液吸收多余的Cl2以避免污染 | |
| C. | Cl2不能使有色布条褪色,但Cl2具有氧化性 | |
| D. | 过量的红热的铁丝在Cl2中剧烈燃烧,反应生成FeCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
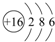
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 固态Na2O2和熔融态NaHSO4中的阴、阳离子个数比均为1:1 | |
| B. | 离子化合物中一定不含共价键 | |
| C. | 某主族元素的最高价含氧酸为HnROm,则其气态氢化物一般是H8-2m+nR或RH8-2m+n | |
| D. | 元素周期表中L层电子为奇数的元素的化合价也都是奇数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com