
某同学要对某溶液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
(1)
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1.检验Cl— | 取少许滤液于试管中,
|
| 含有Cl— |
| 2.检验NH4+ | 取少许滤液于试管中,
|
| 含有NH4+ |
| 3.检验Zn2+ | 取少许滤液于试管中,加入稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
(2)根据以上的实验报告,关于滤液的成分,他的结论是:滤液中含有氯化铵和氯化锌
若想从滤液中得到溶质固体,还应进行的操作是加热蒸发(加热浓缩), ,过滤。
若要将所得的溶质固体中的物质加以分离,可用 法。
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:阅读理解
| 实验 混合溶液 |
A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
科目:高中化学 来源:0110 模拟题 题型:填空题
查看答案和解析>>
科目:高中化学 来源:0118 期末题 题型:实验题
 等4中溶液,可与实验中
等4中溶液,可与实验中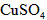 溶液起相似作用的是___________________;
溶液起相似作用的是___________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com