
【题目】配制VmL 2.0mol·L-1的氢氧化钠溶液,需要氢氧化钠固体质量______ g。 下列操作,会使所配的溶液浓度如何变化。
(1)称取氢氧化钠固体时将固体放在天平托盘的纸片上:______ ;
(2)称量时左码右物,且使用了游码:_______;
(3)容量瓶用蒸馏水洗净,没有烘干:________;
(4)没有等到溶液冷却到室温就将溶液注入容量瓶中:______;
(5)转移溶液时有溶液撒出:_____,
(6)没有用蒸馏水洗烧杯和玻璃棒:____,
(7)定容时仰视液面:_____,
(8)定容时俯视液面:____。
【答案】0.08V 降低 降低 不变 升高 降低 降低 升高 降低
【解析】
首先根据![]() 算出需要的
算出需要的![]() 的物质的量,再代入摩尔质量算出质量即可;在误差分析时按照
的物质的量,再代入摩尔质量算出质量即可;在误差分析时按照![]() 来分析,看看这些操作究竟会影响溶质的物质的量n还是溶液的体积V。
来分析,看看这些操作究竟会影响溶质的物质的量n还是溶液的体积V。
根据![]() 算出
算出![]() 的物质的量,再根据
的物质的量,再根据![]() 算出
算出![]() 的质量,接下来进行误差
的质量,接下来进行误差
(1)用纸片称量会造成部分![]() 残留在纸片上,n小了浓度降低;
残留在纸片上,n小了浓度降低;
(2)左码右物会导致实际称取的![]() 比需要的少,n小了浓度降低;
比需要的少,n小了浓度降低;
(3)容量瓶本身就要加蒸馏水定容,一开始存在少量蒸馏水无影响;
(4)根据热胀冷缩原理,热溶液的体积膨胀,因此实际上加的水会减少,V小了浓度升高;
(5)若转移时有溶液洒出,相当于部分![]() 溶质被洒出,n小了浓度降低;
溶质被洒出,n小了浓度降低;
(6)若不洗烧杯和玻璃棒,势必会有少量![]() 溶质未转移到容量瓶中,n小了浓度降低;
溶质未转移到容量瓶中,n小了浓度降低;
(7)根据仰小俯大原则,仰视液面会导致定容时实际加入的水低于刻度线,V小了浓度升高;
(8)根据仰小俯大原则,俯视液面会导致定容时实际加入的水高于刻度线,V大了浓度降低。


科目:高中化学 来源: 题型:
【题目】氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质作用(四种物质与氯水的重合部分代表物质间的反应,且氯水足量),请回答下列问题:

(1)反应d中,将氯水滴加到一张蓝色石蕊试纸上,试纸上会出现如图所示的半径慢慢扩大的内外两个圆环,且两环颜色不同,下列有关说法中错误的是___

A.此实验表明氯水具有酸性、漂白性
B.内环呈白色外环呈红色或浅红色
C.内外环上颜色的差异表明此变化过程中,酸使指示剂的颜色变化比氧化还原反应慢
D.氯气与水反应中氧化产物是HClO
(2)反应e的离子方程式为___。
(3)反应b有气体产生,生成该气体反应的化学方程式为___。
(4)久置的氯水最终会变成___(填名称),则反应a的化学方程式表示为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化锂(LiH)在干燥的空气中能稳定存在,遇水或酸能够引起燃烧。某活动小组准备使用下列装置制备LiH固体。
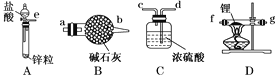
甲同学的实验方案如下:
(1)仪器的组装连接:上述仪器装置接口的连接顺序为___,加入药品前首先要进行的实验操作是___(不必写出具体的操作方法);其中装置B的作用是___。
(2)添加药品:用镊子从试剂瓶中取出一定量金属锂(固体石蜡密封),然后在甲苯(一种有机化合物)中浸洗数次,该操作的目的是除去锂表面的石蜡,然后快速把锂放入到石英管中。通入一段时间氢气后加热石英管,在加热D处的石英管之前,必须进行的实验操作是___。
(3)加热一段时间后停止加热,继续通氢气冷却,然后取出LiH,装入氮封的瓶里,保存于暗处。采取上述操作的目的是为了避免LiH与空气中的水蒸气接触而发生危险。分析该反应原理,完成LiH与水反应的化学方程式___。
(4)准确称量制得的产品0.174g,在一定条件下与足量水反应后,共收集到气体470.4mL(已换算成标准状况),则产品中LiH与Li的物质的量之比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用甲苯为原料生产对羟基苯甲酸乙酯![]() (—种常用的化妆品防腐剂)。其生产过程如下图所示(反应条件未全部注明),已知酚羟基(直接接连在苯环上的羟基)具有强还原性:
(—种常用的化妆品防腐剂)。其生产过程如下图所示(反应条件未全部注明),已知酚羟基(直接接连在苯环上的羟基)具有强还原性:
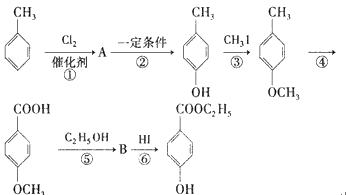
请回答下列问题:
(1)合成路线中有机物![]() 的名称为_______。
的名称为_______。
(2)有机物A的结构简式为____。
(3)写出反应②、④的反应类型:__________、__________。
(4)写出反应③的化学方程式(不必注明反应条件):__________________。
(5)在合成路线中,设计③和⑥的目的是__________。
(6)有机物![]() 的同分异构体有多种,其中既含有酚羟基又含有酯基的同分异构体共有__________种。
的同分异构体有多种,其中既含有酚羟基又含有酯基的同分异构体共有__________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体金即金溶胶,其具有光吸收性、呈色性和胶体性等特点。免疫胶体金技术作为胶体金标记物, 可实现对抗原抗体的测定。

用白磷还原法可制得一种金的分散系,该分散系在临床诊断及药物检测等方面有着广泛的应用。
其操作步骤如下:
a.取20%白磷(①)的乙醚溶液0.5 mL,加蒸馏水(②)60 mL。
b.先滴加1%氯化金水溶液(③)0.75 mL,再滴加0.1 mol·L-1的K2CO3(④)0.6 mL,振荡变成棕红色。
c.加热煮沸至溶液变成透明红色。
d.分离提纯,除去无机溶质。
所得分散系中,金颗粒直径在5~12 nm之间。
请回答下列问题:
(1)上述物质①②③④中属于单质的是________(填序号,下同),属于化合物的是________,属于盐的是________。
(2)该分散系属于________,其分散质是_______________。
(3)所得红色溶液________(填“能”或“不能”)继续加热。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入 6mol/L 的硫酸溶液,乙同学将电极放入 6mol/L 的氢氧化钠溶液中,如图所示:
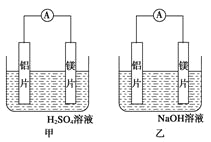
(1)写出甲电池中正极的电极反应式___________________ ;
(2)写出乙池中负极的电极反应式: 负极:_____ 总反应的离子方程式:_________
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金 属,则构成负极材料的金属活泼
,则甲会判断出_____活动性更强,而乙会判断出_____活动性更强(填名称)
(4)由此实验,可得到如下哪些正确结论(_____)
a. 利用原电池反应判断金属活动性顺序时应注意选择合适的介质
b. 镁的金属性不一定比铝的强
c. 该实验说明金属活动性顺序表已过时,已没有利用价值
d. 该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析
(5)上述实验也反过来证明了“直接利用金属活动性顺序表判断原电池中的正负极”这种做法__填 “可靠”或“不可靠”)。如不可靠,请你提出另一个判断原电池正负极的可行实验方案_______________ (如 可靠,可不填)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Cl-、Br-、Fe2+、I-的还原性依次增强。现向FeBr2、FeI2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示,请回答:
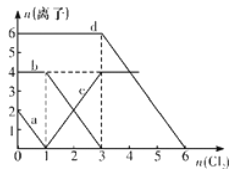
(1)a线分别代表溶液中____________的变化情况;
(2)c线分别代表溶液中____________的变化情况;
(3)原溶液中Br-与Fe2+的物质的量之比为____________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述正确的是
A.常温常压下,22gCO2含有的氧原子数为NA
B.标准状况下,2.24 L CCl4含有的分子数为0.1NA
C.常温常压下,0.1molL-1的MgCl2溶液中含Cl-数为0.2NA
D.常温常压下,5.6g铁与足量Cl2完全反应,转移电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究Na与CO2反应的产物,某化学兴趣小组按如图所示装置进行实验。
己知:CO+2Ag(NH3)2OH=2Ag↓+ (NH4)2CO3+2NH3
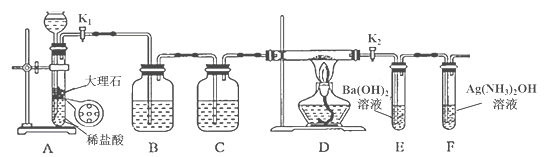
回答下列问题:
(1)B中的溶液为______________。
(2)先称量硬质玻璃管的质量为ml g,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是m2 g。再进行下列实验操作,其正确顺序是____________(填标号);重复上述操作步骤,直至硬质玻璃管恒重,称得质量为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.称量硬质玻璃管
d.打开K1和K2,通入CO2至E中出现浑浊 e.关闭K1和K2 f.冷却到室温
(3)加热硬质玻璃管一段时间,观察到以下现象:
①钠块表面变暗,熔融成金属小球;
②继续加热,钠迅速燃烧,产生黄色火焰。反应完全后,管中有大量黑色物质;
③F中试管内壁有银白物质产生。
产生上述②现象的原因是____________________________________________________;
(4)探究固体产物中钠元素的存在形式
假设一:只有Na2CO3; 假设二:只有Na2O; 假设三:Na2O和Na2CO3均有;
完成下列实验设计,验证上述假设:
步骤 | 操作和现象 | 结论 |
1 | 将硬质玻璃管中的固体产物溶于水后过滤; | 假设一成立 |
2 | 往步骤1所得滤液中_________________________________; 现象:____________________________________。 |
(5)根据上述实验现象及下表实验数据,写出Na与CO2反应的总化学方程式_____________。
m1 | m2 | m3 |
66.7g | 69.0g | 72.1g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com