
【题目】CO2气体在一定条件下可与金属镁反应,干冰在一定条件下可以形成CO2气体,这两个变化过程中需要克服的作用分别是
A.共价键,共价键 B.共价键,分子间作用力
C.分子间作用力,共价键 D.分子间作用力,分子间作用力
科目:高中化学 来源: 题型:
【题目】一定温度和压强下,30 L某种气态纯净物中含有6.02×1023 个分子,这些分子由1.204 ×1024个原子构成,下列有关说法中不正确的是( )
A. 该温度和压强可能是标准状况
B. 标准状况下该纯净物若为气态,其体积是 22.4 L
C. 该气体分子为双原子分子
D. 若在该条件下O2为气态,则此时1 mol O2的体积为30 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是重要的化工原料,也是应用广泛的化工产品。CO2与过氧化钠或超氧化钾反应可产生氧气。
完成下列计算:
(1)CO2通入氨水生成NH4HCO3,NH4HCO3很容易分解。2.00mol NH4HCO3完全分解,分解产物经干燥后的体积为_________L(标准状况)。
(2)某H2中含有2.40 molCO2,该混合气体通入2.00 L NaOH溶液中,CO2被完全吸收。如果NaOH完全反应,该NaOH溶液的浓度为_______。
(3)CO2和KO2有下列反应:
4KO2+2CO2→2K2CO3+3O2
4KO2+4CO2+2H2O→4KHCO3+3O2
若9 mol CO2在密封舱内和KO2反应后生成9 molO2,则反应前密封舱内H2O的量应该是多少?列式计算。
(4)甲烷和水蒸气反应的产物是合成甲醇的原料:CH4+H2O![]() CO+3H2
CO+3H2
已知:CO+2H2![]() CH3OH CO2+3H2
CH3OH CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
300 mol CH4完全反应后的产物中,加入100 mol CO2后合成甲醇。若获得甲醇350 mol,残留氢气120 mol,计算CO2的转化率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 同温同压下,相同体积的不同物质,其质量—定不相等
B. 任何条件下,等体积的甲烷和氮气所含的分子数—定相等
C. 1L一氧化碳气体一定比1L氧气的质量小
D. —氧化碳和氧气的混合气体,若平均相对分子质量为29,则一氧化碳气体和氧气的体积比为3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四支试管中分別盛有固体NaBr、NaCl、Na2SO3、Cu,分别向这四支试管中加入适量浓硫酸,部分现象如图所示:
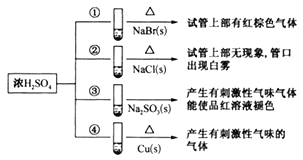
下列判断正确的是( )
A. 反应①和②的现象说明还原性:Br->Cl-
B. 浓硫酸与NaCl不反应,白雾是浓硫酸吸水所致
C. 反应③现象说明氧化性:浓硫酸>Na2SO3
D. 反应④的现象除产生刺激性气味的气体外,溶液中还析出蓝色晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱厂电解精制的饱和食盐水,利用电解产品可制取漂白粉等。
(1)如果粗盐中含有SO42﹣,精制时须添加试剂除去SO42﹣,该试剂不能选用______。
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(2)电解饱和食盐水发生的化学方程式_________________。
(3)利用氯气和氢氧化钠溶液制取“84”消毒液的化学方程式____________。
(4)漂白粉在空气中久置后会变质的化学方程式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不属于配合物的是( )
A. [Cu(H2O)4]SO4·H2O B. [Ag(NH3)2]OH
C. KAl(SO4)2·12H2O D. Na[Al(OH)4]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏伽德罗常数的值为NA,下列说法正确的是( )
A. pH=1的H2SO3溶液中,含有H+数为0.1NA
B. 1molCl2与足量的铁反应,转移的电子数为3NA
C. 标准状况时,2.24LNO和1.12LO2于密闭容器中充分反应后,其分子数为0.1NA
D. 100mL0.1mol·L-1的CH3COONa溶液中,CH3COO-的数量少于0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯氧化铁是现代电子工业的重要材料。以下是用硫酸厂产生的烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2)为原料制备高纯氧化铁(软磁a-Fe2O3)的生产流程示意图:

(1)酸浸时,常需将烧渣粉碎、并加入过量H2SO4,其目的是____ ;滤渣的主要成分为 _____(填化学式)。
(2)加入FeS2时,发生反应②的离子方程式为___________。
(3)加入NH4HCO3目的是__________________。“沉淀”时,pH不宜过高,否则制备的FeCO3中可能混有的杂质是_________________。检验FeCO3是否洗涤干净的方法是_____________。
(4)煅烧时,发生反应④的化学方程式为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com