
【题目】下列反应中,是吸热反应,也是氧化还原反应的是( )
A. Ba(OH)2﹒8H2O与NH4Cl晶体混合 B. 醋酸与NaOH溶液混合
C. 炽热的碳与水蒸气反应 D. 高温煅烧石灰石
科目:高中化学 来源: 题型:
【题目】文献报道:利用氯化氢氧化反应一脱水耦合工艺,可用有机氯化工艺的副产品氯化氢为原料制备氯气,实现氯的循环利用,原理为4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g).将HC1和O2分别以5种物质的量比:①1:1 ②2:1 ③4:1 ④6:1 ⑤8:1,向五个容积可变的容器中投料时,反应温度对HCl平衡转化率影响的曲线如图.
2Cl2(g)+2H2O(g).将HC1和O2分别以5种物质的量比:①1:1 ②2:1 ③4:1 ④6:1 ⑤8:1,向五个容积可变的容器中投料时,反应温度对HCl平衡转化率影响的曲线如图.

请回答下列问题:
(1)可以判断该反应已经达到化学平衡的是__. (填字母).
A.密闭容器中总压强不变 B.密闭容器中混合气体的密度不变
C.v(HCl)=2v(Cl2) D.密闭容器中氯气的体积分数不变
(2)d曲线对应的投料比是__(填比值,从题干中选择,下同).有机工业需要含O2量低的氧气和氯化氢混合气体,可控制n(HCl):n(O2)=_______制备.
(3)该反应的平衡常数表达式为________.
(4)若按b曲线对应的投料比进行反应,且温度为415℃,反应达到平衡时Cl2的体积分数为_______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用双线桥法表示下列反应中电子转移的方向和数目:Cl2+SO2+2H2O=2HCl+H2SO4_________________________。
在上述反应中,若反应消耗35.5 g Cl2,同时消耗标准状况下SO2的体积约为______L,转移电子的物质的量为________mol。
(2)实验室利用如图装置快速制备少量氯气,可利用以下反应:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O。此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。

①写出该反应的离子方程式:_______________________________。
②该反应中,氧化产物是________。
③当电子转移的数目为6.02×1023时,生成的氯气在标准状况下的体积为________,被氧化的Cl-个数为________。
(3)实验室也可以利用如图装置制备氯气,反应方程式为:2MnO2+4HCl![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。

在上述反应中,还原剂是_____,若有1 mol氧化剂参与反应,转移电子的物质的量为____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)从樟科植物枝叶提取的精油中含有甲、乙两种成分:

①请写出甲的一种能同时满足下列3个条件的同分异构体的结构简式________。
a.苯环上有两个不同的取代基
b.能与Br2的CCl4溶液发生加成反应
c.遇FeCl3溶液显呈现紫色
②由甲转化为乙的过程为(已略去无关产物):

反应Ⅰ的反应类型为________,Y的结构简式__________。
(2)写出下图高聚物所对应的单体:
____________________,_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的量浓度表述正确的是
A. 0.2mol·L-1Na2SO4溶液中含有Na+和SO42—总物质的量为0.6mol
B. 50mL 2mol·L-1的NaCl溶液和100 mL L 0.5mol·L-1MgCl2溶液中,Cl-的物质的量浓度相等
C. 用1L水吸收22.4L氯化氢(标况下)所得盐酸的浓度是1mol·L-1
D. 10g 98%的硫酸(密度为1.84g·cm—3)与10mL 18.4mol·L—1的硫酸的浓度是相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是1 L“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
成分 | 质量(g) | 摩尔质量(g ·mol-1) |
蔗糖 | 50.00 | 342 |
硫酸钾 | 0.87 | 174 |
阿司匹林 | 0.35 | 180 |
高锰酸钾 | 0.158 | 158 |
硝酸银 | 0.04 | 170 |
⑴下列“鲜花保鲜剂”的成分中,属于非电解质的是_______。
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
⑵“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为___________molL-1。
⑶配制上述1 L“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、____________、__________、________________。(在横线上填写所缺仪器的名称)
⑷在溶液配制过程中,下列操作正确且对配制结果没有影响的是__________。
A.将药品放入容量瓶中加蒸馏水溶解
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸性溶液X可能含有Na+、Al3+、NH4+、I-、SO32-、SO42-离子,为探究该溶液的成分,进行了如下实验:

(1)操作①用到的玻璃仪器是________;操作②的名称为______________。
(2)实验室中检验气体B的方法是_____________________________。
(3)写出生成气体A的离子反应方程式____________________________。
(4)该实验能否说明一定存在Al3+_________(填“能”或“否”),依据是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水煤气的主要成分是氢气和一氧化碳,由水蒸气和炽热的无烟煤或焦炭作用而得.是重要的化工原料,可用于合成甲醇和甲醚等有机化合物,已知:
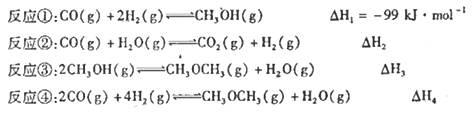
(1)△H1= ______(用△H2、△H3、△H4)。
(2)反应②的存在,可大大提高CH30CH3的产率,原因是: ________。
C0(g)和H2(g)以物质的量之比1:2混合,一定条件下在1L固定容积内发生反应①,下图表示温度分别为300℃、500℃的密闭容器中,甲醇的物质的量与时间的关系。回答下列问题:

①C、D两点平衡常数KC _____KD(填>、<、= )。
②在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2下列有关该体系的说法正确的是 _______。
a. 正反应速率加快,逆反应速率也加快
b.甲醇的物质的量增加
c.重新平衡时n(H2)/n(CH3OH)增大
(4)温度为T时,向容积1L的密闭容器甲、乙中分别充入一定量的CO(g)和H20(g),发生反应②,相关数据如下:

①甲容器中,反应在t1min内的平均速率v(H2)= ____mol/(Lmin)。
②乙容器中,a=_____mol。
③解释降低温度使C02平衡浓度增大的原因___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、NH4+、Ba2+、Fe3+、C1-、SO42-、CO32-,将该混合物溶于水后得澄清溶液,现取3份100 mL该溶液分别进行如下实验:
序号 | 实验内容 | 实验结果 |
1 | 加过量盐酸 | 无气体产生 |
2 | 加足量NaOH溶液并加热 | 收集到气体2.24 L(标准状况),并有红褐色沉淀生成,将沉淀过滤洗涤、干燥、灼烧至质量不再变化,称重得1.60 g固体。 |
3 | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量 | 称量读数为2.33g |
试确定溶液中一定存在的离子及其物质的量浓度(可不填满):
离子符号 | 物质的量浓度(mol·L-1) |
_____ | _____ |
_____ | _____ |
_____ | _____ |
_____ | _____ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com