
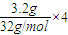 =0.4mol;
=0.4mol;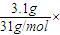 3=0.3mol,得失电子数不相等,所以该固体不是纯净的三氧化二磷;
3=0.3mol,得失电子数不相等,所以该固体不是纯净的三氧化二磷; 5=0.5mol,得失电子数不相等,所以该固体不是纯净的三氧化二磷;
5=0.5mol,得失电子数不相等,所以该固体不是纯净的三氧化二磷; O2(g)=
O2(g)= P2O5 (s)△H=-Y KJ/mol①,
P2O5 (s)△H=-Y KJ/mol①, 得P(s)+
得P(s)+ O2(g)=
O2(g)= P2O3(s)△H=-(20X-Y)KJ/mol,
P2O3(s)△H=-(20X-Y)KJ/mol, O2(g)=
O2(g)= P2O3(s)△H=-(20X-Y)KJ/mol.
P2O3(s)△H=-(20X-Y)KJ/mol.

 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
| 3 |
| 4 |
| 1 |
| 2 |
| 3 |
| 4 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 4 |
| 1 |
| 2 |
| 3 |
| 4 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
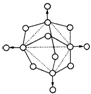 磷在空气中充分燃烧,生成X的分子结构如右图所示.图中实线表示化学键,圆圈表示原子(不考虑原子体积大小)
磷在空气中充分燃烧,生成X的分子结构如右图所示.图中实线表示化学键,圆圈表示原子(不考虑原子体积大小)查看答案和解析>>
科目:高中化学 来源: 题型:
(1)通过计算确定反应产物的组成(用化学式表示)是________,其相应的质量(g)为_______。
(2)已知单质磷的燃烧热为Y kJ·mol-1,则1 mol P与O2反应生成固态P2O3的反应热ΔH=______。
(3)写出1 mol P与O2反应生成固态P2O3的热化学方程式:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)通过计算确定反应产物的组成(用化学式表示)是 ,其相应的质量(g)为 。
(2)已知单质磷的燃烧热为Y kJ/mol,则1mol P与O2反应生成固态P2O3的反应热ΔH= 。
(3)写出1mol P与O2反应生成固态P2O3的热化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com