
| A. | 在食盐中加入碘 | B. | 在自来水中加入碘 | ||
| C. | 在饮料中加入碘 | D. | 在饮用酒中加入碘 |
科目:高中化学 来源: 题型:多选题
| A. | C物质的物质的量浓度不变 | B. | 物质C和物质D的物质的量浓度相等 | ||
| C. | B物质的转化率不发生变化 | D. | 反应速率v (A)=v (D) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用稀盐酸冲洗 | B. | 加稀盐酸溶解,再用蒸馏水冲洗 | ||
| C. | 用热的碳酸钠溶液冲洗 | D. | 加热,使碳酸盐分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合物电离时,生成的阳离子是氢离子的是酸 | |
| B. | 化合物电离时,生成的阴离子是氢氧根离子的是碱 | |
| C. | 化合物电离时,生成金属阳离子和酸根离子的是盐 | |
| D. | NH4Cl的电离方程式是:NH4Cl═NH4++Cl-,NH4+不是金属阳离子,所以NH4Cl不是盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氧化钠与水反应生成氢氧化钠 | B. | 碳酸钠俗称纯碱 | ||
| C. | 钠及钠的化合物的焰色反应为黄色 | D. | 钾的金属性比钠弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②和③ | B. | ②和① | C. | ③和① | D. | ④和① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加Fe(s)的量 | B. | 将容器的体积缩小一半 | ||
| C. | 升高温度 | D. | 通入水蒸气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
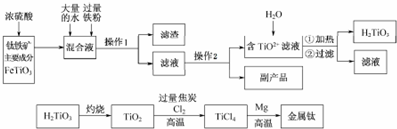
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com