
【题目】某校化学兴趣小组用如图所示过程除去AlCl3中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失。请回答下列问题:
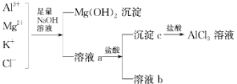
(1)写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:_______________________。
(2)氢氧化钠溶液能否用氨水代替,为什么?___________________________。
(3)溶液a中存在的离子有________________;在溶液a中加入盐酸时需控制盐酸的量,为什么?__________________________________。为此,改进方法是___________________________。
【答案】Mg2++2OH===Mg(OH)2↓、Al3++3OH===Al(OH)3↓、Al(OH)3+OH===![]() +2H2O 不能,因为在Al3+与氨水反应生成Al(OH)3后,Al(OH)3不能与氨水继续反应,从而不能将Al(OH)3与Mg(OH)2分开 Na+、
+2H2O 不能,因为在Al3+与氨水反应生成Al(OH)3后,Al(OH)3不能与氨水继续反应,从而不能将Al(OH)3与Mg(OH)2分开 Na+、![]() 、K+、Cl、H+、OH 因为氢氧化铝能与强酸反应,所以在加入盐酸沉淀
、K+、Cl、H+、OH 因为氢氧化铝能与强酸反应,所以在加入盐酸沉淀![]() 时,需要控制溶液的pH,以防止部分
时,需要控制溶液的pH,以防止部分![]() 转化成Al3+ 通入过量CO2气体
转化成Al3+ 通入过量CO2气体
【解析】
(1)首先加入过量的强碱NaOH溶液的目的是沉淀Mg2+并且使铝以偏铝酸盐的形式存在于溶液中
(2)不能使用弱碱氨水,否则Al3+与氨水反应生成Al(OH)3后,Al(OH)3不能与氨水继续反应,从而不能将Al(OH)3与Mg(OH)2分开
(3)在溶液a中加入盐酸是为了沉淀AlO2-,但生成的Al(OH)3沉淀可继续溶解,为此最好改为向溶液a中通入过量二氧化碳气体以防Al(OH)3溶解


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】将一定量的镁铝合金样品分成两等份,一份加入足量NaOH溶液中,充分反应后,收集到标准状况下气体6.72L;另一份加入到足量稀盐酸中,充分反应后,收集到标准状况下气体11.2L。则原合金样品中镁的质量为
A. 4.8 g B. 6 g C. 9.6 g D. 12 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用含少量银和锌的粗铜做阳极,纯铜片做阴极,CuSO4溶液做电解液,电解一段时间后,阳极质量减少了x g,则( )
A. 电解液质量增加x g B. 阴极质量增加x g
C. 阴极质量增加a g,a>x D. 阴极质量增加b g,b<x
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下六个图中,横坐标为某溶液中加入某物质的物质的量,纵坐标为生成沉淀的物质的量,将图中的字母代号填入下表。

溶液 | 加入的物质 | 字母代号 |
①饱和石灰水 | 通过量CO2 | ________ |
②AlCl3溶液 | 通过量NH3 | ________ |
③MgCl2、AlCl3混合溶液 | 逐滴加NaOH溶液至过量 | ________ |
④AlCl3溶液 | 逐滴加NaOH溶液至过量 | ________ |
⑤含少量HCl的AlCl3溶液 | 逐滴加NaOH溶液至过量 | ________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请用下图所示仪器装置设计一个包括电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。
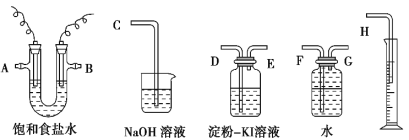
(1)所选仪器 连接时,各接口的顺序是(填各接口的代号字母):A 接 , 接 ,B 接 , 接 。_____________
(2)实 验 时 , 装 置 中 的 石 墨 电 极 接 电 源 的 _____极 , 所 发 生 的 电 极 反 应 式 为_____;铁电极接电源的_____极,所发生的电极反应式为_____; 此电解总反应方程式为_________。
(3)实验测得产生的氢气体积(已折算成标准状况)为 5.60 mL,电解后溶液的体积恰好为50.0 mL,则溶液中 OH-的浓度为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液滴加到某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如下图所示【已知:P[c(A-)/c(HA)]=-1g[c(A-)/c(HA)]】。下列叙述不正确的是
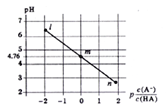
A. Ka(HA)的数量级为10-5
B. 滴加NaOH溶液过程中,c(A-)/[c(HA)×c(OH-)]保持不变
C. m点所示溶液中:c(H+)=c(HA)+c(OH-)-c(Na+)
D. n点所示溶液中:c(Na+)=c(A-)+c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,当容器A中的反应开始后,若分别进行下列操作,请回答有关问题:
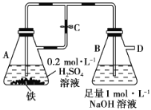
(1)若止水夹C打开,B容器中有什么现象发生:__________________________________________。
(2)若开始时止水夹C关闭,容器A中的反应还在进行时,B容器中有什么现象发生:_________________,写出B容器中有关反应的化学方程式:_____________________。
(3)若先打开止水夹C一段时间,容器A中的反应还在进行时,再关闭止水夹C一会儿,B容器中有什么现象发生:_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸、醋酸和氨水是中学化学中常见的三种物质,某校实验小组利用浓盐酸、冰醋酸和浓氨水分别配制了浓度均为0.1 mol·L-1的三种溶液各100 mL并进行相关实验,据此回答下列问题:
(1)常温下上述三种溶液的PH由大到小的顺序是____________________。
(2)25℃时,利用pH试纸测得0.1 mol·L-1醋酸溶液的pH约为5,则可以估算出醋酸的电离常数约为__________________;向10 mL此溶液中加入少量冰醋酸,忽略溶解过程中溶液温度和体积的微小变化,溶液中![]() 的值将_________(填“增大”“减小”或“无法确定”)。
的值将_________(填“增大”“减小”或“无法确定”)。
(3)将浓度均为0.1 mol·L-1的盐酸和氨水等体积混合,则:①所得混合溶液显_______性(填“酸性”“碱性”或“中性”),原因是__________________(用离子方程式表示)。
②所得混合溶液中所有离子的物质的量浓度由大到小的顺序为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com