
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,常用于水的消毒以及纺织高漂白。过氧化氢法生产亚氯酸钠的流程图如下

已知NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O且NaClO2在碱性条件下稳定性较高。试回答下列问题:
(1)在ClO2发生器中同时有氯气产生,则在发生器中发生反应的化学方程式为
(2)在NaClO2稳定装置中,H2O2作 (选填序号)。
A.氧化剂 B.还原剂
C.既作氧化剂又作还原剂 D.既不作氧化剂也不作还原剂
(3)在实验室模拟“固体分离装置”中的技术,必须进行的实验操作是 (按实验后顺序填写操作代号)。
A.过滤 B.加热 C.分液 D.蒸馏 E.冷却
(4)经查阅资料知道:当pH≤2.0时,ClO-2能被I完全还原成Cl—;
溶液中Na2S2O3能与I2反应生成NaI和Na2S4O6。
欲测定成品中NaClO2的含量,现进行如下操作:

①步骤Ⅱ中发生反应的离子方程式是 ,
步骤Ⅲ中达到滴定终点时的现象是 。
②若上述滴定操作中用去了V mL Na2S2O3溶液,则样品中NaClO2的质量分数 (用字母表示)。
【知识点】工艺流程题 A4 B1 D2 C1 J1 B2
【答案解析】(1)2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
(2)B (3)BEA
(4)ClO2-+4H++4I-=2I2+Cl-+2H2O
滴入最后一滴标准液(Na2S2O3溶液),溶液由蓝色变为无色,且半分钟内不变色
9.05×10-2VC/4W
解析: ⑴ClO2发生器中有氯气产生,是NaClO2氧化浓盐酸:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
⑵ClO2在稳定装置中变为NaClO2,发生的是还原反应,因此H2O2作还原剂
⑶根据NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O知采取冷却结晶的方法,即加热→冷却→过滤。
⑷①根据当pH≤2.0时,ClO-2能被I完全还原成Cl—知步骤Ⅱ中发生反应是ClO2-将I-氧化为I2,步骤Ⅲ发生的反应是2Na2S2O3+I2=2NaI+Na2S4O6,即终点时的现象是滴入最后一滴标准液(Na2S2O3溶液),溶液由蓝色变为无色,且半分钟内不变色
②NaClO2~2I2~4 Na2S2O3
90.5 4mol
m VC×10-3,m=9.05×10-2VC/4,因此质量分数为9.05×10-2VC/4W
【思路点拨】多步反应计算采取关系式法;根据物质的溶解度随温度的变化结晶方法有蒸发结晶(物质的溶解度随温度的变化小)和冷却结晶(物质的溶解度随温度的变化大)。


科目:高中化学 来源: 题型:
已知25℃、101kPa下,稀的强酸与强碱溶液反应的中和热为57.3kJ/mol.
(1)写出表示稀硫酸与稀烧碱溶液发生反应的中和热的热化学方程: .
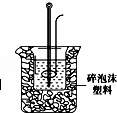
(2)学生甲用稀硫酸与稀烧碱溶液测定中和热装置如图.
①实验时所需的玻璃仪器除烧杯、量筒外还需: .
②该装置中有一处错误是: ,如果用该错误
装置测定,结果会 (填“偏高”“偏低”“无影响”)
③如果该生用50mL 0.25mol/L的稀硫酸与50mL 0.55mol/L的稀烧碱溶液,他用试剂的用量的理由是: .在该实验中需要测定某种数据,完成一次实验,需要测定该数据的次数为 次.使用正确的装置进行实验,取上述溶液在小烧杯中进行中和反应,三次实验温度平均升高3.4℃.已知中和后生成的溶液的比热容为4.18J/(g•℃),溶液的密度均为1g/cm3.通过计算可得中和热△H= .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是A、B、C、D、E五种元素的某些性质:
|
| A | B | C | D | E |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 |
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是________。
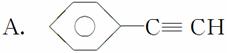
B.CH4
C.CH2===CHCH3
D.CH3CH2C≡CH
E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键___________________________________________。
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是________(化学式),理由是________________________。
(4)B、D形成的氢化物沸点:________更高,热稳定性________更强。(写化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
配位化学创始人维尔纳发现,将各为1 mol的CoCl3·6NH3(黄色)、CoCl3·5NH3(紫红色)、CoCl3·4NH3(绿色)、CoCl3·4NH3(紫色)四种配合物溶于水,加入足量硝酸银溶液,立即沉淀的氯化银分别为3 mol、2 mol、1 mol、和1 mol。已知上述配合物中配离子的配位数均为6。
(1)请根据实验事实用配合物的形式写出它们的化学式。
CoCl3·6NH3______________________,
CoCl3·5NH3____________________,
CoCl3·4NH3(绿色和紫色)____________。
(2)后两种物质组成相同而颜色不同的原因是它们互为同分异构体,已知绿色的配合物内界结构对称,请在下图中用元素符号标出氯原子的位置。

查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中有CO、H2、O2共16.5g和足量的Na2O2,用电火花引燃,使其完全反应,Na2O2增重7.5g,则原混合气体中O2的质量分数是( )
A.54.5% B.40%
C.36% D.33.3%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于糖类的说法正确的是( )
|
| A. | 所有糖类物质都有甜味,但不一定都溶于水 |
|
| B. | 蔗糖和葡萄糖都是单糖 |
|
| C. | 葡萄糖和果糖性质不同,但分子式相同 |
|
| D. | 摄入人体的纤维素在酶的作用下能水解为葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 使用食品添加剂与提倡绿色食品相违背 |
|
| B. | 没有食品添加剂的天然食品是最安全的 |
|
| C. | 含有食品添加剂的食品应该少吃,以防中毒 |
|
| D. | 食品添加剂在合理限量范围内不影响人体健康 |
查看答案和解析>>
科目:高中化学 来源: 题型:
食物是维持人类生命和健康的支柱.下表是某食品包装袋上的说明( )
| 品名 | ***蔬菜苏打饼 |
| 配料 | 面粉、鲜鸡蛋、精炼食用植物油、白砂糖、奶油、食盐、脱水青菜、橙汁 |
| 保质期 | 十二个月 |
| 生产日期 | 2011 年8月20日 |
对上表中各种配料的成分的理解不正确的是( )
|
| A. | 富含蛋白质的是鸡蛋 |
|
| B. | 富含维生素的是脱水青菜和橙汁 |
|
| C. | 富含糖类的物质只有白砂糖 |
|
| D. | 富含油脂的是精炼食用植物油和奶油 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com