
【题目】如图曲线 a 表示放热反应X(g)+Y(g) ![]() Z(g) + M(g) + N(s)进行过程中 X 的转化率随时间变化的关系。若要改变起始条件,使反应过程按 b 曲线进行,可采取的措施是( )
Z(g) + M(g) + N(s)进行过程中 X 的转化率随时间变化的关系。若要改变起始条件,使反应过程按 b 曲线进行,可采取的措施是( )
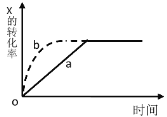
A.升高温度B.加大 X 的投入量
C.加催化剂D.增大体积
科目:高中化学 来源: 题型:
【题目】常温下,分别调节浓度均为0.1 mol·L-1 HA溶液、HB的溶液的pH,所得溶液中酸分子的百分含量ω%(如HA的百分含量为![]() ×100%)与pH的变化关系如图所示。已知调节pH时不影响溶液总体积。下列说法不正确的是
×100%)与pH的变化关系如图所示。已知调节pH时不影响溶液总体积。下列说法不正确的是
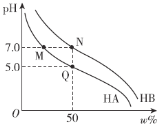
A.常温下,Ka(HA)=1.0×10-5B.M、N两点对应离子浓度:c(A-)=c(B-)
C.将M、N两点溶液等体积混合,溶液呈中性D.水的电离程度:M=N>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿托酸是用于合成治疗胃肠道痉挛及溃疡药物的中间体,其结构如图所示。下列有关说法正确的是
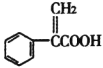
A.阿托酸分子中所有碳原子一定处于同一平面
B.阿托酸是含有两种官能团的芳香烃
C.阿托酸苯环上的二氯代物超过7种
D.一定条件下,1mol阿托酸最多能4mol H2、1mol Br2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸锰可用于制造钠离子电池的负极材料。可用如下反应制得乙酸锰: 4Mn(NO3)2·6H2O+26(CH3CO)2O=4(CH3COO)3Mn+8HNO2+3O2↑+40CH3COOH。
(1)Mn3+基态价层电子排布图为________。
(2)Mn(NO3)2·6H2O中非金属元素第一电离能从大到小的顺序__________。从电子云重叠的方式看N中存在的化学键类型有__________。
(3)与NO2-互为等电子体的一种分子的化学式为________。
(4)1molCH3COOH中含有的σ键数目为___________。CH3COOH分子通过氢键形成环状二聚物,写出含氢键表示的环状二聚物的结构简式___________。
(5)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为_________。镁铝合金密度为ρg/cm3,则该晶胞的边长为__________nm(阿伏加德罗常数的值为N)。
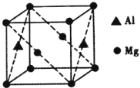
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
①氯化钠饱和溶液![]()
![]() NaHCO3(s)
NaHCO3(s)
② Al2O3![]() AlCl3(aq)
AlCl3(aq)![]() Al(OH)3
Al(OH)3
③海水![]() Mg(OH)2
Mg(OH)2![]() MgCl2(aq)
MgCl2(aq)![]() MgCl2(s)
MgCl2(s)
④N2![]() NO2
NO2![]() HNO3
HNO3
⑤重晶石(BaSO4)![]() BaCO3
BaCO3![]() BaCl2(aq)
BaCl2(aq)
A. ①③⑤ B. ②③④
C. ②④⑤ D. ①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】R、X、Y、Z的原子序数依次增大,且都不超过10.这四种元素可组成一种化合物的结构如图所示。下列说法正确的是( )
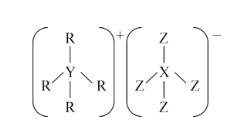
A.常温常压下,上述元素的单质都呈气态
B.最高价氧化物对应水化物的酸性:X>Y
C.Y、Z的气态氢化物能发生化合反应
D.由R、X两种元素只能形成一种化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是合成抗炎药洛索洛芬钠的关键中间体,它的一种合成路线如下:
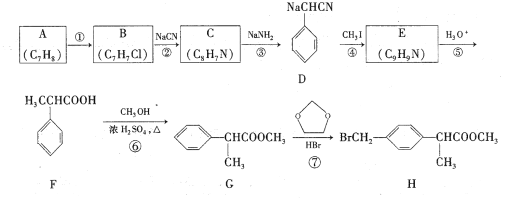
回答下列问题:
(1)A的名称是____,H中官能团名称是____;
(2)反应①的反应条件为____;
(3)反应⑥的化学方程式为________;反应类型为____。
(4)反应⑦除生成H外,还生成了另一种有机产物的结构简式为____。
(5)符合下列条件的G的同分异构体有____种。
I.能发生银镜反应 Ⅱ.苯环上一氯取代物只有一种 Ⅲ.核磁共振氢谱有4组峰
(6)仿照H的合成路线,设计一种由B合成![]() 的合成路线___。
的合成路线___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯是一种食用香料,其结构简式如图。有关柠檬烯的分析正确的是
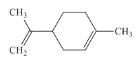
A.它的一氯代物有9种,和H2充分反应后的产物一氯代物有7种
B.它和丁基苯![]() 互为同分异构体
互为同分异构体
C.它的分子中所有的碳原子一定在同一平面上
D.柠檬烯可以发生加成、取代、氧化、加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种常见元素的性质或结构信息如F表所示,请问答下列问题。
元素 | A | B | R | D |
相关信息 | 基态原子核外电子占据3个能级且最高能级上有3个电子 | B的单质是最常见半导体材料 | 位于第四周期IB族 | 是非金属元素,其形成的某种单质是电的良导体,有的分子形状似足球 |
(1)R的基态原子价层电子排布式为________,这四种元素的第一电离能由大到小的顺序为________________(写元素符号)。
(2)A、B,D均可形成多种氢化物,在最常见的三种氢化物中,分子构型为三角锥的氢化物分子式为_______,任意写出一种中心原子存在sp2、sp3两种杂化类型的物质的结构简式________,与A的常见单质互为等电子体的上述元素的氧化物是________。
(3)B、D均可形成氧化物,等物质的量的B、D的最高价氧化物中σ键之比为________,已知有下列两种数据:
键能(kJ/mol) | 熔点(K) | 沸点(K)) | |
BO2 | B-O:452 | 1923 | 2503 |
DO2 | D=O:615,D-O:348 | 216 | 195 |
请解释键能大小与两种氧化物熔点、沸点高低差异过大的原因________。
(4)在一定条件下,Cl-与R2+可形成一种无限长链离子,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氧与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为________。
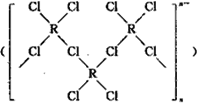
(5)A元素能形成组成为Pt(AH3)2Cl2的配合物,该配合物存在两种同分异构体:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大。
①Q是________(填“极性”或“非极性”)分子,
②P的结构简式为________(AH3配体作为一个整体写)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com