
如图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是
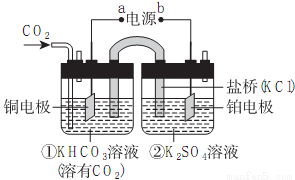
A.该过程是电能转化为化学能的过程
B.铜电极的电极反应式为CO2+8H++8e-=CH4+2H2O
C.一段时间后,①池中n(KHCO3)不变
D.一段时间后,②池中溶液的pH一定升高
科目:高中化学 来源:2016届吉林省高三第八次模拟理综化学试卷(解析版) 题型:选择题
化学与人类社会的生产、生活有着密切联系。下列叙述中正确的是( )
A. “歼﹣20”飞机上大量使用的碳纤维是一种新型的有机高分子材料
B.“神舟十号”宇宙飞船返回舱外表面主要是导电导热良好的新型金属材料钛合金
C.“天宫一号”是中国第一个空间实验室,其太阳能电池板的主要材料是硅
D.“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源:2016届海南海南中学高三考前模拟十一化学试卷(解析版) 题型:选择题
天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子.火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示:
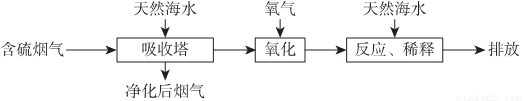
下列说法错误的是
A.天然海水pH≈8的原因是由于海水中的CO32-、HCO3-水解
B.“氧化”是利用氧气将H2SO3、HSO3-、SO32-等氧化生成SO42-
C.“反应、稀释”时加天然海水的目的是防止净化海水时生成沉淀
D.“排放”出来的海水中SO42-的物质的量浓度与进入吸收塔的天然海水相同
查看答案和解析>>
科目:高中化学 来源:2016届海南海南中学高三考前模拟十一化学试卷(解析版) 题型:填空题
消除氮氧化物和硫氧化物有助于预防雾霾天气的形成。
(1)某恒容密闭容器中存在如下反应:C(s)+2NO(g)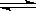 N2(g)+CO2(g)△H。维持温度不变,测得不同时刻几种气体物质的浓度如下表所示:
N2(g)+CO2(g)△H。维持温度不变,测得不同时刻几种气体物质的浓度如下表所示:
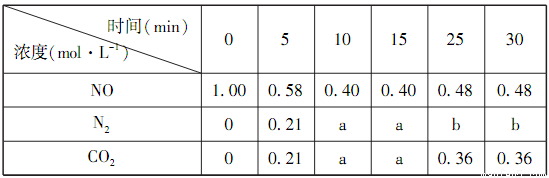
①0~10min内,NO的平均反应速率v(NO)=___________,该温度下反应的平衡常数K=___________。
②表中25min的数据变化与反应进行到22min时改变了反应体系中的某一条件有关,则b=___________,改变的条件可能是___________。
A.加入一定量的活性炭
B.通入一定量的N2
C.适当缩小容器的体积
③若15min时升高温度,达到平衡时容器中NO、N2、CO2的浓度之比为5:3:3,则△H___________0(填“>”、“=”或“<”)。
(2)NH3催化还原氮氧化物(产物是N2、H2O)是目前广泛采用的烟气脱氮技术
①当废气中NO2、NO的体积分数相等时脱氮率最高,若此情况下生成1molN2时反应放出的热量为akJ,则对应的热化学方程式为___________。
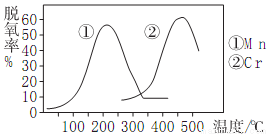
②右图使用不同催化剂时的脱氮率,则脱氮时最佳的温度、催化剂应是___________。
(3)用石灰浆作吸收剂也可脱去废气中的SO2,若处理结束时,测得吸收液中c(Ca2+)=0.70mol/L,则c(SO32-)=___________(已知Ksp(CaSO3)=1.4×10-7)。
查看答案和解析>>
科目:高中化学 来源:2016届海南海南中学高三考前模拟十一化学试卷(解析版) 题型:选择题
某烃X能使溴的CCl4溶液褪色,完全燃烧时1molX需要消耗9molO2且生成等物质的量的CO2与H2O。若其结构中含有两个—CH3,则该物质的结构(不考虑立体异构)最多有
A.6种B.5种C.4种D.7种
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三第五次适应性考试理综化学试卷(解析版) 题型:实验题
钴(Co)及其化合物在工业上有广泛应用。为从某工业废料中回收钴,某学生设计流程如下(废料中含有Al、Li、Co2O3和Fe2O3等物质)。
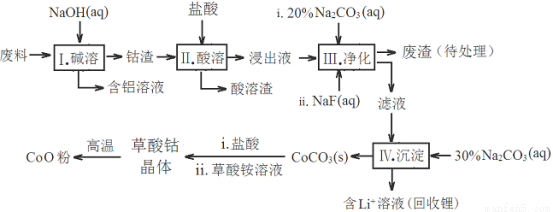
已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表:
Fe3+ | Co2+ | Co3+ | Al3+ | |
pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
请回答:
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式是____________________________。
(2)写出步骤Ⅱ中Co2O3与盐酸反应的离子方程式_________________________
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过__________。废渣中的成分有______________________。
(4)NaF与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是___________。
(5)在空气中加热CoC2O4固体,经测定,210~290℃的过程中只产生CO2和一种二化合物,该化合物中钴元素的质量分数为73.44%。此过程发生反应的化学方程式是_________________。
(6)某锂离子电池的总反应为C+LiCoO2 LixC+Li1-xCoO2,LixC中Li的化合价为______价,该锂离子电池充电时阳极的电极反应式为______________。
LixC+Li1-xCoO2,LixC中Li的化合价为______价,该锂离子电池充电时阳极的电极反应式为______________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古包头九中高一下第一次月考化学试卷(解析版) 题型:选择题
标准状况下,将aLH2和Cl2的混合气体点燃,充分反应后,将混合气体通入含b molNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl―、ClO―、ClO3―,且三者物质的量之比为8:1:1,则原混合气体中H2的物质的量
A.a/2mol B.(a/22.4-b)mol C(a/22.4-b/2)mol D.b/2mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:选择题
已知:1molH2(g)与1molBr2(g)完全反应生成2molHBr(g)时放出72kJ的热量,有关物质的相关数据如下表:则表中a为
化学键 | H-H | Br- Br | H-Br |
断裂1mol化学键需要吸收的能量/kJ | 436 | a | 369 |
A.200 B.230 C.260 D.404
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com