
分析 将生成的气体依次通过CaCl2管(A)和碱石灰(B),A管质量增加了2.16g,应为水的质量,B管增加了9.24g,应为二氧化碳的质量,根据有机物的相对分子质量可知一定物质的量的有机物中含有的C、H原子个数,结合质量守恒计算是否含有O,并计算O原子个数,以此计算分子式,从质量守恒的角度计算耗氧量,结合有机物的性质判断可能的结构.
解答 解:(1)化学反应遵循质量守恒定律,则消耗O2的质量为:2.16+9.24-3.24=8.16g,
答:燃烧此有机物3.24g需消耗O28.16g;
(2)试管A吸水质量增加2.16g,为生成水的质量,水的物质的量=$\frac{2.16g}{18g/mol}$=0.12mol,含H0.24mol,
碱石灰吸CO2增加9.24g,即生成二氧化碳的物质的量=$\frac{9.24g}{44g/mol}$=0.21mol,
该有机物物质的量为=$\frac{3.24g}{108g/mol}$=0.03mol,
所以有机物分子中,N(C)=$\frac{0.21mol}{0.03mol}$=7,
N(H)=$\frac{0.12mol×2}{0.03mol}$=8,
N(O)=$\frac{108-12×7-8}{16}$=1,
所以有机物的分子式为:C7H8O,
答:有机物的分子式为C7H8O;
(3)若该有机物属于芳香族化合物,含有1个苯环,C7H8O的不饱和度=$\frac{2×7+2-8}{2}$=4,侧链不含不饱和键,若只有1个侧链,则为-CH2OH或-OCH3,若侧链有2个,为-OH、-CH3,有邻、间、对三种位置关系,故符合条件的有机物的结构简式为: ,
,
答:符合条件的有机物的结构简式为 .
.
点评 本题考查有机物分子式的计算,题目难度中等,本题注意根据有机物燃烧产物的质量关系确定有机物的分子式,为解答该题的关键,注意结合有机物的性质判断可能的结构.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:解答题
 A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:
A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径X>Y | |
| B. | X与Y处于同一周期 | |
| C. | 离子半径X+>Y2- | |
| D. | X的单质与Y的单质发生反应只能生成X2Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.36 LNO2与水充分反应转移的电子数目为0.1NA | |
| B. | 4.0 gH218O与D2O的混合物中所含中子数为2NA | |
| C. | 50 g质量分数为68%的H2O2的水溶液中含氧原子数为2NA | |
| D. | 常温下,l L0.1 mol•L-1的硝酸铵溶液中氮原子数目小于0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知硫酸铜在加热条件下发生分解反应,生成氧化铜、二氧化硫、三氧化硫和氧气.请用如图所示装置,测定硫酸铜在加热分解时产生的各物质与参加反应的硫酸铜的物质的量的关系.
已知硫酸铜在加热条件下发生分解反应,生成氧化铜、二氧化硫、三氧化硫和氧气.请用如图所示装置,测定硫酸铜在加热分解时产生的各物质与参加反应的硫酸铜的物质的量的关系.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:3 | B. | 1:2 | C. | 3:1 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
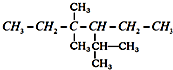 系统命名:2,4,4-三甲基-3-乙基己烷.
系统命名:2,4,4-三甲基-3-乙基己烷. 的系统名称3-甲基-2-乙基-1-丁烯,将其在催化剂存在下完全氢化所得烷烃的系统名称是2,3-二甲基戊烷.
的系统名称3-甲基-2-乙基-1-丁烯,将其在催化剂存在下完全氢化所得烷烃的系统名称是2,3-二甲基戊烷.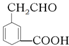 碳碳双键、醛基、羧基.
碳碳双键、醛基、羧基.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池放电时,负极上发生反应的物质是Zn | |
| B. | 负极发生的反应是Zn+2OH--2e-═Zn(OH)2 | |
| C. | 工作时,负极区溶液碱性减弱,正极区溶液碱性增强 | |
| D. | 溶液中OH-向正极移动,K+、H+向负极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
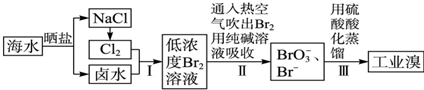
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com