
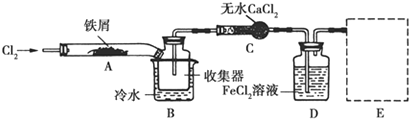
���� ��1��װ��A������������Ӧ�����Ȼ�����
��2��Ҫʹ������FeCl3�����ռ���������FeCl3��������������ȡ���ȷ�����
��3��B�е���ˮ����Ϊ����ȴFeCl3ʹ������������ռ���Ʒ��
��4������FeCl2�Ƿ�ʧЧӦ�����Ƿ����������ӣ�������KMnO4��Һ��K3[Fe��CN��6]��Һ���飻
��5��������������Һ���յ�����������ֹ��Ⱦ������
��6�����������������ԣ�������л�ԭ�ԣ�����֮�䷢��������ԭ��Ӧ��2FeCl3+3H2S=2FeCl2+6HCl+3S����
��� �⣺��1��װ��A������������Ӧ�����Ȼ�������Ӧ����ʽΪ��2Fe+3Cl2 $\frac{\underline{\;\;��\;\;}}{\;}$2FeCl3��
�ʴ�Ϊ��2Fe+3Cl2 $\frac{\underline{\;\;��\;\;}}{\;}$2FeCl3��
��2����FeCl3���ȷ�������ʹ������FeCl3�����ռ�����
�ʴ�Ϊ���ڳ�����FeCl3�����·����ȣ�
��3��B�е���ˮ����Ϊ����ȴFeCl3ʹ������������ռ���Ʒ��װ��C������Ϊ����ܣ�
�ʴ�Ϊ����ȴ��ʹFeCl3�����������ռ���Ʒ������ܣ�KMnO4��Һ��
��4������FeCl2�Ƿ�ʧЧӦ�����Ƿ����������ӣ�������KMnO4��Һ��K3[Fe��CN��6]��Һ���飬
�ʴ�Ϊ��KMnO4��Һ��K3[Fe��CN��6]��Һ��
��5��������������Һ���յ�����������ֹ��Ⱦ������װ��ͼΪ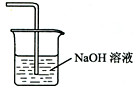 ��
��
�ʴ�Ϊ�� ��
��
��6�����������������ԣ�������л�ԭ�ԣ�����֮�䷢��������ԭ��Ӧ��2FeCl3+3H2S=2FeCl2+6HCl+3S�������ӷ���ʽΪ��2Fe3++H2S=2Fe2++S��+2H+��
�ʴ�Ϊ��2Fe3++H2S=2Fe2++S��+2H+��
���� ���⿼�������Ʊ�ʵ�飬�漰��ԭ��������ķ������ۡ�β��������������ԭ��Ӧ�����Ӽ���ȣ�����������ѧ����Ϣ��ȡ��Ǩ������������������ѧʵ���л�����ʶ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HF�ĵ���ʽ��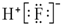 | |
| B�� | H��D��T����Ԫ�ص����ֲ�ͬ���أ�����ͬλ�� | |
| C�� | K+���ӵĽṹʾ��ͼ��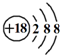 | |
| D�� | �廯�Ƶĵ���ʽ��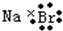 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
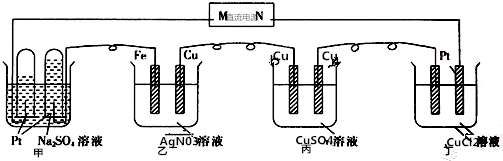
| A�� | NΪֱ����Դ������ | |
| B�� | �ҳص��ܷ�ӦΪ4AgN03+2H20�T4Ag+4HNO3+O2�� | |
| C�� | ���صķ�Ӧ���ϵ�⾫��ͭԭ�� | |
| D�� | Ҫʹ���ص������Һ��ԭ�����������CuCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | �������� | ���� | ���ͻ����ӷ���ʽ |
| A | AgNO3��Һ | �а�ɫ�������� | Cl-+Ag+�TAgCl�� |
| B | ʯ����Һ | �Ժ�ɫ | ��ˮ�������ᡢ������ |
| C | CaCO3 | ������ų� | CO32-+2H+�TH2O+CO2�� |
| D | FeCl2��KSCN��Һ | �к�ɫ�������� | 2Fe2++Cl2�T2Fe3++2Cl- |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
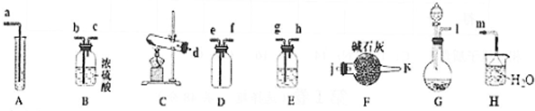
| װ�ñ�� | |||
| װ���е��Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ˮ�ĵ���̶�ʼ������ | |
| B�� | c��NH4+����c��NH3•H2O��ʼ�ռ�С | |
| C�� | c��CH3COOH����c��CH3COO?��֮��ʼ�ձ��ֲ��� | |
| D�� | �����백ˮ�����Ϊ10mLʱ��c��NH4+��=c��CH3COO-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
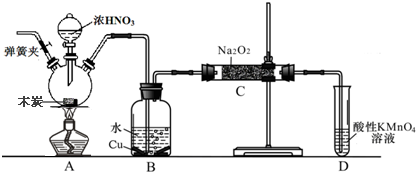
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2�� | B�� | 3�� | C�� | 4�� | D�� | 5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ�� | B�� | ���� | C�� | ������ | D�� | ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com