
(16分)Fe2+和I-是两种常见的还原性离子。
(1)向FeSO4溶液中滴加氯水,溶液由浅绿色变成黄色,反应的离子方程式为 ;向KI溶液中滴加氯水,溶液由无色变成黄色,反应的离子方程式: 。
(2)请以FeSO4溶液、KI溶液、氯水为试剂验证I-的还原性强于Fe2+。设计实验方案,补充完成实验步骤、预期现象和结论。其他限选试剂:3 mol·L-1 H2SO4、0.01 mol·L-1 KMnO4、20% KSCN、3%H2O2、淀粉溶液、紫色石蕊溶液。
实验步骤 | 预期现象与结论 |
步骤1:取2mLFeSO4溶液和2mLKI溶液混合于试管中,再滴加1~2滴氯水。 |
; |
步骤2: ____________________________________ ____________________________________。 |
|
(3)利用(2)提供的试剂证明碘与铁的化合物中铁显+2价,实验操作和现象是:
取少量样品溶于水, 。
33.(1)2Fe2++Cl2=2Fe3++2Cl—(3分)2I—+Cl2=I2+2Cl—(3分)

【解析】
试题分析:(1)亚铁离子为浅绿色,铁离子为黄色,氯水中的氯气把亚铁离子氧化为铁离子,离子方程式为:2Fe2++Cl2=2Cl-+2Fe3+,氯水中的氯气把碘离子氧化为碘单质,离子方程式为:2I-+Cl2=2Cl-+I2,
答案为:2Fe2++Cl2=2Cl-+2Fe3+;2I-+Cl2=2Cl-+I2;(2)步骤一:向FeSO4溶液中滴加氯水,溶液由浅绿色变成黄色,向KI溶液中滴加氯水,溶液由无色变成黄色,因此取2mL FeSO4溶液和2mL KI溶液混合于试管中,再滴加1~2滴氯水的现象为溶液变为黄色;答案为:溶液变为黄色;步骤二:可以用淀粉溶液检验碘单质的存在,溶液变蓝,证明I-的还原性强于Fe2+,也可以用20%KSCN溶液检验铁离子的存在,向试管中继续滴加几滴KSCN溶液,若溶液不变红,也说明I-的还原性强于Fe2+,答案为:向试管中继续滴加几滴20%KSCN溶液或向试管中继续滴加几滴淀粉溶液;溶液不变红说明I-的还原性强于Fe2+或溶液变蓝,说明I-的还原性强于Fe2+;(3)先滴加20%KSCN溶液不变红,然后滴加3% H2O2把亚铁离子氧化铁离子,溶液变红色,证明含有亚铁离子,答案为:滴加几滴20%KSCN溶液,无明显现象,再滴加3% H2O2溶液,溶液变红色。
考点:考查氧化性、还原性强弱的比较,离子方程式的书写。


科目:高中化学 来源:2014秋季甘肃省高二第一学期期中考试文科化学试卷(解析版) 题型:选择题
日常生活中遇到的很多问题都涉及到化学知识,下列有关做法在日常生活中可行的是
A.医用酒精和工业酒精的主要成分相同,都可用于伤口消毒
B.可利用米汤检验含碘盐的真假
C.低血糖症状出现时,吃馒头要比喝葡萄糖水见效快
D.用食醋清洗热水瓶中的水垢
查看答案和解析>>
科目:高中化学 来源:2015届广东省韶关市十校高三10月联考化学试卷(解析版) 题型:选择题
下列陈述I、 II正确并且有因果关系的是( )
选项 | 叙述I | 叙述II |
A | 锌金属活动性比铁强 | 海轮外壳上装锌块可减缓腐蚀 |
B | Ba(OH)2可与盐酸反应 | Ba(OH)2可用于治疗胃酸过多 |
C | SiO2是酸性氧化物 | SiO2能与水反应生成硅酸 |
D | H2O2有氧化性 | H2O2能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市毕业班调研测试理综化学试卷(解析版) 题型:实验题
(17分)化学兴趣小组的同学设计实验探究浓硫酸与木炭反应后产生气体的成分。
(1)写出浓硫酸与木炭反应方程式,并标明电子转移的方向和数目:____________________。
【装置设计】组装如下的实验装置,然后进行实验探究。

(2)装入反应物之前,必须先 。
(3)要验证产生的气体中含有CO2,请在答题卡中完成图中虚线框内的装置简图,并标明试剂。
【实验探究】
(4)观察实验,完成实验现象的部分记录:
实验装置 | ① | ② | ③ |
实验现象 |
| …… |
|
(5)实验装置②中品红溶液Ⅰ的作用 ,III的作用 。
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市毕业班调研测试理综化学试卷(解析版) 题型:选择题
常温下,0.1 mol·L-1的一元酸HA与0.1 mol·L-1的NaOH溶液等体积混合后,所得溶液pH>7, 下列说法正确的是
A.混合前一元酸HA的c(H+)=0.1 mol·L-1
B.该混合溶液中:c(Na+)>c(A-)>c(OH-)>c(H+)
C.HA在水溶液中的电离方程式:HA = H+ + A-
D.该混合溶液中:c(A-)+ c(HA)=0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:选择题
标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为c mol/L,则下列关系中不正确的是
A.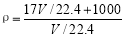 B.
B.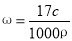
C. D.
D.
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高一第一学期期中考试化学试卷(解析版) 题型:实验题
(16分)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。

图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
(1)装置①是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其反应的化学方程式为 。
(2)工业上常用氯气与熟石灰反应制漂白粉,漂白粉的有效成分为 (填化学式)。
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是 。
(4)反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是 (填写编号字母);
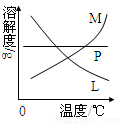
从②的试管中分离出该晶体的方法是 (填写实验操作名称)。
(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性 。为什么? 。
(6)若②的试管溶液中不但有KClO3生成还有KClO生成,且二者的物质的量之比为1∶2,则该反应中氧化剂和还原剂的物质的量之比为: 。
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高一第一学期期中考试化学试卷(解析版) 题型:选择题
“纳米技术是当今科学研究的前沿之一,l纳米(nm)=10-9m,其研究成果广泛应用于催化及军事科学中,“纳米材料是指研究、开发出的直径从几纳米至几十纳米的材料,如将“纳米材料”分散到液体分散剂中,所得混合物可能具有的性质是
A.所得分散系不稳定 B.一定能形成溶液
C.不能透过滤纸 D.有丁达尔效应
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.铁表面镀铜时,铜与电源的正极相连,铁与电源的负极相连
B.用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大
C.一定温度下,反应2Mg(s)+CO2(g)=2MgO(s)+C(s)能自发进行,则该反应△H<0
D.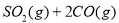

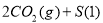 达到平衡,保持其他条件不变,分离出硫,正反应速率加快,SO2的转化率提高
达到平衡,保持其他条件不变,分离出硫,正反应速率加快,SO2的转化率提高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com