
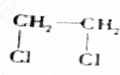 +2NaOH$→_{△}^{H_{2}O}$HOCH2CH2OH+2NaCl;
+2NaOH$→_{△}^{H_{2}O}$HOCH2CH2OH+2NaCl;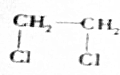 +2NaOH$→_{△}^{乙醇}$CH≡CH↑+2NaCl+2H2O;
+2NaOH$→_{△}^{乙醇}$CH≡CH↑+2NaCl+2H2O;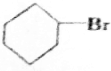 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$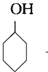 +NaBr;
+NaBr;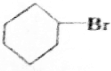 +NaOH$→_{△}^{C_{2}H_{5}OH}$
+NaOH$→_{△}^{C_{2}H_{5}OH}$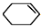 +H2O+NaBr.
+H2O+NaBr. 分析 (1)1,2-二氯乙烷与NaOH的水溶液共热,发生水解反应生成乙二醇;
(2)1,2-二氯乙烷在碱的醇溶液中加热发生消去反应生成炔烃;
(3)1-溴环己烷在氢氧化钠的水溶液中发生取代反应生成环己醇;
(4)1-溴环己烷在氢氧化钠的醇溶液中发生消去反应生成环己烯.
解答 解:(1)卤代烃在氢氧化钠的水溶液中发生水解反应生成醇类,所以1,2-二氯乙烷与氢氧化钠水溶液共热可以生成乙二醇(HOCH2CH2OH)的反应方程式为:
ClCH2CH2Cl+2NaOH$\stackrel{△}{→}$HOCH2CH2OH+2NaCl,
故答案为:ClCH2CH2Cl+2NaOH$\stackrel{△}{→}$HOCH2CH2OH+2NaCl;
(2)卤代烃与KOH的乙醇溶液供热发生消去反应,1,2-二氯乙烷在碱的醇溶液中反应方程式为:ClCH2CH2Cl+2NaOH$→_{△}^{乙醇}$CH≡CH↑+2NaCl+2H2O,
故答案为:ClCH2CH2Cl+2NaOH$→_{△}^{乙醇}$CH≡CH↑+2NaCl+2H2O;
(3)1-溴环己烷在氢氧化钠的水溶液中发生水解反应生成醇类,反应为: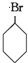 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +NaBr,
+NaBr,
故答案为: +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +NaBr;
+NaBr;
(4)1-溴环己烷在氢氧化钠的醇溶液中发生消去反应生成烯烃,反应为: +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$ +H2O+NaBr,
+H2O+NaBr,
故答案为: +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$ +H2O+NaBr.
+H2O+NaBr.
点评 本题考查了方程式的书写,侧重考查有机反应方程式的书写,熟悉有机物的结构是解题关键,注意反应条件,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | X | 946 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;过氧化钠
;过氧化钠 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高反应体系的温度,可使反应速率变大 | |
| B. | 该反应中N2不可能100%转化为NH3 | |
| C. | 该反应达到平衡状态时,N2、H2和NH3三者的浓度一定相等 | |
| D. | 为了提高H2的转化率,可适当提高N2的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Br-、CO${\;}_{3}^{2-}$ | B. | Ba2+、Al3+、Cl- | ||
| C. | NH${\;}_{4}^{+}$、Fe3+、SO${\;}_{4}^{2-}$ | D. | Ag+、H+、NO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
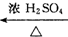 A(C4H8O3)$→_{△}^{浓H_{2}SO_{4}}$乙,甲、乙的分子式都为C4H6O2,甲能使溴的四氯化碳溶液褪色,乙为五元环状化合物,则甲不能发生的反应类型有( )
A(C4H8O3)$→_{△}^{浓H_{2}SO_{4}}$乙,甲、乙的分子式都为C4H6O2,甲能使溴的四氯化碳溶液褪色,乙为五元环状化合物,则甲不能发生的反应类型有( )| A. | 消去反应 | B. | 酯化反应 | C. | 加聚反应 | D. | 氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;RCN$\stackrel{H_{2}O/H+}{→}$RCOOH;RCOOH$\stackrel{SOCl_{2}}{→}$RCOCl$\stackrel{R'OH}{→}$RCOOR′
;RCN$\stackrel{H_{2}O/H+}{→}$RCOOH;RCOOH$\stackrel{SOCl_{2}}{→}$RCOCl$\stackrel{R'OH}{→}$RCOOR′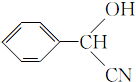 ;
; ;
;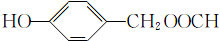 (填结构简式).
(填结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:多选题
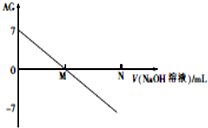 为了更好地表示溶液的酸碱性,科学家提出了酸度(aciditygrade)的概念,定义AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$,室温下用0.01mol•L-1的氢氧化钠溶液滴定20.00mL0.01mol•L-1 醋酸,滴定结果如图所示,下列有关叙述不正确的是( )
为了更好地表示溶液的酸碱性,科学家提出了酸度(aciditygrade)的概念,定义AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$,室温下用0.01mol•L-1的氢氧化钠溶液滴定20.00mL0.01mol•L-1 醋酸,滴定结果如图所示,下列有关叙述不正确的是( )| A. | 室温下,醋酸的电离平衡常数约为10-6 | |
| B. | M点加入NaOH溶液的体积大于20.00mL | |
| C. | M点时溶液中:c(CH3COO-)=c(Na+) | |
| D. | 若N点时加入NaOH溶液的体积为40mL,则N点时溶液中:c(Na+)=2[c(CH3COO-)+c(CH3COOH)] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醛和酮是不同类的同分异构体,二者的化学性质相似 | |
| B. | 能发生银镜反应的物质是醛,1mol醛与银氨溶液反应只能还原出2mol Ag | |
| C. | 醛类化合物既能发生氧化反应,又能发生还原反应 | |
| D. | 丙醛、丙酮、丙酸均能与氢气在催化剂作用下发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com