
| A、用酸式滴定管滴至终点时,俯视滴定管读数 |
| B、将碱液移入锥形瓶后,加了10 ml蒸馏水再滴定 |
| C、酸式滴定管用蒸馏水润洗后,未用标准盐酸溶液润洗 |
| D、酸式滴定管注入酸液时,尖嘴处留有气泡,达滴定终点时气泡消失 |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
| A、NaHSO3在水中的电离:NaHSO3═Na++H++SO32- |
| B、碳酸钠水溶液的水解:CO32-+2H2O?H2CO3+2OH- |
| C、向含有Pb2+的工业废水中加入FeS:Pb2++FeS═PbS↓+Fe2+ |
| D、向硫酸铜溶液中滴加过量氨水:Cu2++2NH3?H2O═Cu(OH)2↓+2NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
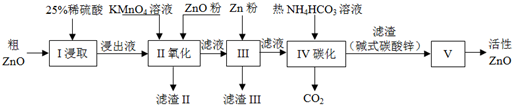
| Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀pH | 5.4 | 7.0 | 2.3 | 4.7 |
| 完全沉淀pH | 8.0 | 9.0 | 4.1 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:

 .请写出以
.请写出以 、CH3CH2CH2COCl、CH3OH为原料制备
、CH3CH2CH2COCl、CH3OH为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如图:
的合成路线流程图(无机试剂任用).合成路线流程图示例如图: .
.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu中混有CuO,可以通过加入足量盐酸溶液,再过滤、洗涤、干燥可得到洁净的Cu |
| B、把1 mL饱和FeCl3溶液逐滴加入到20 mL的沸水中,边加边搅拌,加热到沸腾即可得Fe(OH)3胶体 |
| C、蒸发结晶时当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干 |
| D、进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
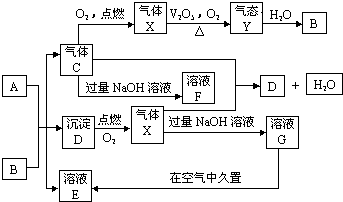
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、分子中所有官能团均能与NaOH反应,且反应原因相同 |
| B、一定条件下,咖啡酸能够发生取代反应、加聚反应、缩聚反应,但不能与NaHCO3溶液反应 |
| C、分子中的所有碳原子可能共平面,但氧原子不可能与所有碳原子处于同一平面上 |
| D、咖啡酸与浓溴水反应,一个咖啡酸分子中最多能引入5个溴原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、-441.8 kJ?mol-1 |
| B、260.4 kJ?mol-1 |
| C、-254.6 kJ?mol-1 |
| D、-260.4 kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com