
| A. | 从100mL1.0mol•L-1的NaOH溶液中取出10mL该溶液,其溶液浓度仍为1.0mol•L-1 | |
| B. | 分离酒精和水可以采用分液的方法 | |
| C. | 在蒸发NaCl溶液时,等蒸发至少量液体时,停止加热,利用余热继续蒸干 | |
| D. | 在盛有碘水的试管中加入少量的CCl4后,充分振荡后下层颜色变为紫色 |
分析 A、溶液是均匀的,取出溶液的浓度与原溶液浓度相同;
B、水和酒精能相互溶解;
C、当蒸发皿中出现较少量液体时即停止加热;
D、碘易溶于CCl4,溶液呈紫红色,密度比水大.
解答 解:A、溶液是均匀的,与取出溶液的浓度与体积大小无关,浓度与原溶液浓度相同,故A正确;
B、水和酒精是互溶的,不能用分液漏斗分离,故B错误;
C、蒸发结晶时应,当蒸发皿中出现较少量液体时即停止加热,利用余热使溶液蒸干,故C正确;
D、碘易溶于CCl4,溶液呈紫红色,由于CCl4密度比水大,则层为无色下层为紫红色,故D正确;
故选B.
点评 本题考查化学实验方案评价,涉及物质性质、基本操作,明确实验原理及基本操作规范性是解本题关键,题目难度不大.


科目:高中化学 来源: 题型:填空题
 .
. .
.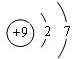 .
.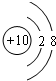 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
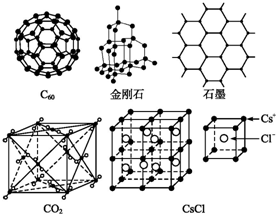
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气在氧气中燃烧时,存在化学键的断裂和形成 | |
| B. | 有化学键断裂的过程一定是化学变化 | |
| C. | 化学反应过程中,所有反应物中都要断裂化学键 | |
| D. | 干冰升华时,分子中的共价键发生断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是一个电化学过程的示意图.
如图是一个电化学过程的示意图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石>晶体硅>晶体硅>二氧化硅>碳化硅 | |
| B. | 氟化氢>碘化氢>溴化氢>氯化氢 | |
| C. | 氧化镁>氧气>氮气>水 | |
| D. | 铯>铷>钾>钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )| A. | 等物质的量的两种物质跟足量的NaOH反应,消耗NaOH的量相等 | |
| B. | 完全燃烧等物质的量的两种物质生成二氧化碳和水的量分别相等 | |
| C. | 一定条件下,两种物质都能发生酯化反应和氧化反应 | |
| D. | 鞣酸分子中,可能在同一平面上的原子最多有14个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com