
用pH试纸检测溶液的pH时的正确操作是( )
A.将pH试纸浸入溶液中,观察并比较变色情况
B.用蒸馏水冲洗玻璃棒后,用玻璃棒蘸取溶液点在试纸上,与标准比色卡比色
C.将试纸用少量蒸馏水润湿,沾在玻璃棒的一端,在溶液里浸一下,与标准比色卡比色
D.用洁净,干燥的玻璃棒蘸取溶液,点在试纸上,与标准比色卡比色
科目:高中化学 来源:物理教研室 题型:013
A.将pH试纸浸入溶液中,观察并比较变色情况
B.用蒸馏水冲洗玻璃棒后,用玻璃棒蘸取溶液点在试纸上,与标准比色卡比色
C.将试纸用少量蒸馏水润湿,沾在玻璃棒的一端,在溶液里浸一下,与标准比色卡比色
D.用洁净,干燥的玻璃棒蘸取溶液,点在试纸上,与标准比色卡比色
查看答案和解析>>
科目:高中化学 来源: 题型:
A.氯水或浓硝酸应存在配有磨口玻璃塞的棕色试剂瓶中
B.碱式滴定管中装满标准NaOH溶液后,尖嘴部分若有气泡,赶走气泡的方法是:用手将下端胶管弯曲,使尖嘴部分向上倾斜,然后挤压玻璃珠,快速放液至赶走气泡为止
C.用pH试纸检测溶液的酸性的操作是:先取一条试纸放在表面皿上,用干燥洁净的玻璃棒蘸取待测液点在试纸的中部,30 s内观察颜色的变化并与标准比色卡比较,确定溶液的pH
D.用25 mL量筒量取3.0 mL浓硫酸
E.液态氯乙烷试样加入稀NaOH溶液煮沸,然后再加入硝酸银溶液检验氯元素
F.在2 mL 10%NaOH溶液中滴加2% CuSO4溶液4—6滴,振荡后加入乙醛溶液0.5 mL,加热至沸腾,则有红色沉淀生成
查看答案和解析>>
科目:高中化学 来源:2012届湖北省高二上学期期末考试化学试卷 题型:选择题
下列有关化学实验的叙述不正确的是:( )
A.用托盘天平称量氢氧化钠固体时,应将药品放在烧杯中称量
B.中和热的测定试验中,若用弱酸代替强酸做实验,会导致反应产生的热量少
C.为抑制硫酸亚铁溶液中Fe2+ 的水解,可加稀硝酸酸化
D.用PH试纸检测溶液的PH值时,用洁净干燥的玻棒蘸取溶液,点在试纸上,再与标准比色卡比色
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:实验题
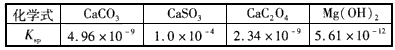
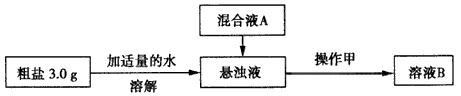
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学实验的叙述不正确的是:( )
A.用托盘天平称量氢氧化钠固体时,应将药品放在烧杯中称量
B.中和热的测定试验中,若用弱酸代替强酸做实验,会导致反应产生的热量少
C.为抑制硫酸亚铁溶液中Fe2+ 的水解,可加稀硝酸酸化
D.用PH试纸检测溶液的PH值时,用洁净干燥的玻棒蘸取溶液,点在试纸上,再与标准比色卡比色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com