
”¾ĢāÄæ”æļ§ŃĪŌŚ¹¤Å©ŅµÉś²śÖŠÓŠ×ÅÖŲŅŖµÄÓĆĶ¾”£»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ń.ij»ÆѧŠĖȤŠ”×éÓū“ÓĻĀĮŠ×°ÖĆ֊єȔ±ŲŅŖµÄ×°ÖĆÖĘČ”(NH4)2SO4ČÜŅŗ£ŗ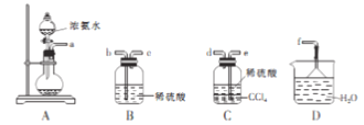
(1)ÓĆ×°ÖĆAÖʱø°±ĘųŹ±£¬¼ģŃéa“¦ŹĒ·ńÓŠ°±Ęų²śÉśµÄ·½·ØŹĒ____________________”£
(2)ÖĘČ”(NH4)2SO4 ČÜŅŗŹ±ŅĒĘ÷Į¬½ÓµÄĖ³Šņ(ÓĆ½ÓæŚ×ÖÄøŗĶ¼żŗÅ”°”ś”±±ķŹ¾)ŹĒa”ś______________(ĖłŃ”×°ÖĆ²»ÖŲø“Ź¹ÓĆ)”£
(3)½«×°ÖĆCÖŠĮ½ÖÖŅŗĢå·ÖĄė£¬ĖłŠčµÄÖ÷ŅŖ²£Į§ŅĒĘ÷ŹĒ______________________”£
¢ņ.ĪŖĢįøßĀČ»Æļ§µÄ¾¼Ć¼ŪÖµ£¬ĪŅ¹ś»Æѧ¼ŅÉč¼ĘĮĖĄūÓĆÓĆĒāŃõ»ÆĆ¾ČČ·Ö½āĀČ»Æļ§ÖĘøÉŌļ°±Ęų²¢µĆµ½¼īŹ½ĀČ»ÆĆ¾[Mg(OH)Cl]µÄ¹¤ŅÕ”£Ä³Ķ¬Ń§øł¾ŻøĆŌĄķÉč¼ĘµÄŹµŃé×°ÖĆČēĶ¼£ŗ
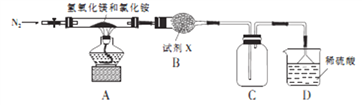
(4)ĀČ»Æļ§µÄµē×ÓŹ½ĪŖ_________________£¬×°ÖĆAÖŠ·¢Éś·“Ӧɜ³É¼īŹ½ĀČ»ÆĆ¾µÄ»Æѧ·½³ĢŹ½ĪŖ_____________________”£
(5)×°ÖĆBÖŠŹŌ¼ĮXĪŖ_______________________”£
(6)ÉĻŹö×°ÖĆĶ¼ÖŠÓŠŅ»“¦“ķĪó£¬ĒėÖø³öøÄÕżµÄ·½·Ø£ŗ_______________________”£
(7)MgCl2”¤6H2OŌŚæÕĘųÖŠ¼ÓČČ£¬Éś³ÉMg(OH)Cl£¬ČōÓÉMgCl2”¤6H2OÖʱøĪŽĖ®MgCl2£¬ŹµŃé·½·ØĪŖ________________________”£
”¾“š°ø”æ ½«ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½ÖĆÓŚaæŚ“¦£¬ČōŹŌÖ½±äĄ¶£¬ŌņĖµÓŠ°±Ęų²śÉś e”śd”śf ·ÖŅŗĀ©¶· ![]() Mg(OH)2+NH4Cl
Mg(OH)2+NH4Cl![]() Mg(OH)Cl+NH3”ü+H2O ¼īŹÆ»Ņ CÖŠµ¼Ęų¹ÜÓ¦¶Ģ½ų³¤³ö ŌŚHClĘųĮ÷ÖŠ¼ÓČČ
Mg(OH)Cl+NH3”ü+H2O ¼īŹÆ»Ņ CÖŠµ¼Ęų¹ÜÓ¦¶Ģ½ų³¤³ö ŌŚHClĘųĮ÷ÖŠ¼ÓČČ
”¾½āĪö”æ±¾Ģāæ¼²éŹµŃé·½°øÉč¼ĘÓėĘĄ¼Ū£¬£Ø1£©¼ģŃé°±ĘųµÄ·½·ØŹĒ½«ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½ÖĆÓŚaæŚ“¦£¬ČōŹŌÖ½±äĄ¶£¬ŌņĖµÓŠ°±Ęų²śÉś£»£Ø2£©ŹµŃéÄæµÄŹĒÖĘČ”ĮņĖįļ§£¬·ĄÖ¹µ¹Īü£¬Ó¦ÓĆ×°ÖĆCĪüŹÕ°±Ęų£¬NH3ÓŠ¶¾£¬ĪŖ·ĄÖ¹ĪŪČ¾æÕĘų£¬±ŲŠėĪ²Ęų“¦Ąķ£¬Ī²Ęų“¦ĄķŹ±»¹ŅŖ×¢Ņā·Ąµ¹Īü£¬Į¬½ÓĖ³ŠņŹĒa”śe”śd”śf£»£Ø3£©CCl4ŗĶĮņĖįļ§»„²»ĻąĶ¬£¬Ņņ“Ė²ÉÓĆ·ÖŅŗµÄ·½·Ø½ųŠŠ·ÖĄė£¬ŠčŅŖÓƵ½µÄ²£Į§ŅĒĘ÷ÓŠ·ÖŅŗĀ©¶·ŗĶÉÕ±£»£Ø4£©ĀČ»Æļ§ŹōÓŚĄė×Ó»ÆŗĻĪļ£¬Ęäµē×ÓŹ½ĪŖ![]() £»×°ÖĆAÖŠÖʱø¼īŹ½ĀČ»ÆĆ¾£¬øł¾ŻĢāÄæÖŠĖłøųŠÅĻ¢£¬ĄūÓĆÓĆĒāŃõ»ÆĆ¾ČČ·Ö½āĀČ»Æļ§ÖĘøÉŌļ°±Ęų²¢µĆµ½¼īŹ½ĀČ»ÆĆ¾[Mg(OH)Cl]£¬Ņņ“Ė·“Ó¦·½³ĢŹ½ĪŖMg(OH)2+NH4Cl
£»×°ÖĆAÖŠÖʱø¼īŹ½ĀČ»ÆĆ¾£¬øł¾ŻĢāÄæÖŠĖłøųŠÅĻ¢£¬ĄūÓĆÓĆĒāŃõ»ÆĆ¾ČČ·Ö½āĀČ»Æļ§ÖĘøÉŌļ°±Ęų²¢µĆµ½¼īŹ½ĀČ»ÆĆ¾[Mg(OH)Cl]£¬Ņņ“Ė·“Ó¦·½³ĢŹ½ĪŖMg(OH)2+NH4Cl ![]() Mg(OH)Cl+NH3”ü+H2O£»£Ø5£©ŹµŃéÄæµÄÖ®Ņ»ŹĒŹÕ¼ÆøÉŌļµÄ°±Ęų£¬ĶعżA×°ÖĆ³öĄ“µÄ°±ĘųÖŠŗ¬ÓŠĖ®ÕōĘų£¬Ņņ“Ė×°ÖĆBµÄ×÷ÓĆŹĒøÉŌļ°±Ęų£¬ŹŌ¼ĮXĪŖ¼īŹÆ»Ņ»ņŃõ»ÆøĘ£»£Ø6£©×°ÖĆCµÄ×÷ÓĆŹĒŹÕ¼Æ°±Ęų£¬ŅņĪŖ°±ĘųµÄĆܶȊ”ÓŚæÕĘų£¬Ó¦ĪŖ¶Ģ¹Ü½ųĘų£¬³¤¹Ü³öĘų£»£Ø7£©ĪŖĮĖ·ĄÖ¹Mg2£«Ė®½ā£¬ÓÉMgCl2”¤6H2OÖʱøĪŽĖ®MgCl2Ź±£¬ŠčŅŖŌŚHClµÄĘųĮ÷ÖŠ¼ÓČČ”£
Mg(OH)Cl+NH3”ü+H2O£»£Ø5£©ŹµŃéÄæµÄÖ®Ņ»ŹĒŹÕ¼ÆøÉŌļµÄ°±Ęų£¬ĶعżA×°ÖĆ³öĄ“µÄ°±ĘųÖŠŗ¬ÓŠĖ®ÕōĘų£¬Ņņ“Ė×°ÖĆBµÄ×÷ÓĆŹĒøÉŌļ°±Ęų£¬ŹŌ¼ĮXĪŖ¼īŹÆ»Ņ»ņŃõ»ÆøĘ£»£Ø6£©×°ÖĆCµÄ×÷ÓĆŹĒŹÕ¼Æ°±Ęų£¬ŅņĪŖ°±ĘųµÄĆܶȊ”ÓŚæÕĘų£¬Ó¦ĪŖ¶Ģ¹Ü½ųĘų£¬³¤¹Ü³öĘų£»£Ø7£©ĪŖĮĖ·ĄÖ¹Mg2£«Ė®½ā£¬ÓÉMgCl2”¤6H2OÖʱøĪŽĖ®MgCl2Ź±£¬ŠčŅŖŌŚHClµÄĘųĮ÷ÖŠ¼ÓČČ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻČēĶ¼µÄÄÜĮæĶ¼£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
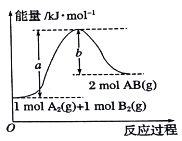
A. A2(g)+B2(g)=2AB(g)ŹĒŅ»øö·ÅČČ·“Ó¦
B. 2molABµÄ×ÜÄÜĮæ“óÓŚ1molA2ŗĶlmolB2µÄÄÜĮæÖ®ŗĶ
C. 1molA2(g)ŗĶ1molB2(g)µÄÄÜĮæÖ®ŗĶĪŖakJ
D. 2AB(g)=A2(l)+B2(l)”÷H<(b-a)kJ/mo1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æX”¢Y”¢Z”¢P”¢QĪŖĪåÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×Ó°ė¾¶ŗĶ×īĶā²ćµē×ÓŹżÖ®¼äµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
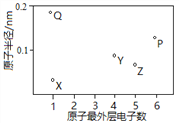
A. XÓėQŠĪ³ÉµÄ»ÆŗĻĪļŹĒĄė×Ó»ÆŗĻĪļ
B. XÓėZµÄŌ×Ó¾łŗ¬ÓŠ1øöĪ“³É¶Ōµē×Ó
C. YÓėPŠĪ³ÉµÄ»ÆŗĻĪļYP2µÄ·Ö×Óæռ乹ŠĶŹĒÖ±ĻߊĪ
D. Qµ„ÖŹŗ¬ÓŠ½šŹō¼ü£¬ÓŠ×ŌÓÉŅĘ¶ÆµÄµē×Ó£¬Ņņ“ĖæÉŅŌµ¼µē
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ·“Ó¦A£Øg£©+3B£Øg£©ØT2C£Øg£©+D£Øg£©ŌŚÄ³¶ĪŹ±¼äÄŚŅŌAµÄÅØ¶Č±ä»Æ±ķŹ¾µÄ»Æѧ·“Ó¦ĖŁĀŹĪŖ1mol/£ØLmin£©£¬Ōņ“Ė¶ĪŹ±¼äÄŚŅŌCµÄÅØ¶Č±ä»Æ±ķŹ¾µÄ»Æѧ·“Ó¦ĖŁĀŹĪŖ£Ø £©
A.0.5 mol/£ØLmin£©
B.1 mol/£ØLmin£©
C.2 mol/£ØLmin£©
D.3 mol/£ØLmin£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹŅĪĀŹ±£¬Ģå»żĪŖ1mL”¢ÅØ¶Č¾łĪŖ0.1mol”¤L-1µÄĮ½ÖÖ³£¼ūĪļÖŹX(OH)n”¢K2AO3µÄČÜŅŗ·Öe¼ÓĖ®Ļ”ŹĶÖĮĢå»żĪŖVmL£¬pHĖęlgVµÄ±ä»ÆĒéæöČēĻĀĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹö“ķĪóµÄŹĒ£Ø £©
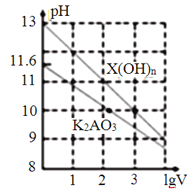
A. n=1
B. H2AO3µÄ¶ž¼¶µēĄė³£ŹżKa2Ō¼ĪŖ1.0”Į10-10.2
C. pH=10µÄĮ½ÖÖČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶ČĻąĶ¬
D. ÉżøßĪĀ¶Č£¬K2AO3ČÜŅŗpHŌö“ó£¬X(OH)nČÜŅŗpH¼õŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŖŃųĀóʬŗ¬ÓŠ¶ąÖֳɷ֣¬ĘäÖŠŹōÓŚĪŽ»śĪļŹĒ
A. ÓńĆ×·Ū B. “󶹷Ū C. Na2HPO4 D. °×É°ĢĒ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠ£¬Ö÷ŅŖ³É·Ö²»ŹĒ¹čĖįŃĪµÄŹĒ£Ø £©
A.ĢÕ“É
B.“óĄķŹÆ
C.²£Į§
D.Ė®Äą
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻąĶ¬ĪĀ¶ČĻĀ£¬Ģå»ż¾łĪŖ0.25 LµÄĮ½øöĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗX2(g)£«3Y2(g) ![]() 2XY3(g)””¦¤H£½£92.6 kJ”¤mol£1ŹµŃé²āµĆ·“Ó¦ŌŚĘšŹ¼”¢“ļµ½Ę½ŗāŹ±µÄÓŠ¹ŲŹż¾ŻČēĻĀ±ķĖłŹ¾£ŗ
2XY3(g)””¦¤H£½£92.6 kJ”¤mol£1ŹµŃé²āµĆ·“Ó¦ŌŚĘšŹ¼”¢“ļµ½Ę½ŗāŹ±µÄÓŠ¹ŲŹż¾ŻČēĻĀ±ķĖłŹ¾£ŗ
ĘšŹ¼Ź±ø÷ĪļÖŹĪļÖŹµÄĮæ/mol | “ļĘ½ŗāŹ±ĢåĻµÄÜĮæµÄ±ä»Æ | |||
ČŻĘ÷ | X2 | Y2 | XY3 | |
ČŻĘ÷¢ŁŗćĪĀŗćČŻ | 1 | 3 | 0 | ·ÅČČ 23.15 kJ |
ČŻĘ÷¢ŚŗćĪĀŗćŃ¹ | 1 | 3 | 0 | Q(Q£¾0) |
ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
A. ČŻĘ÷¢Ł”¢¢ŚÖŠ·“Ó¦ĪļX2µÄ×Ŗ»ÆĀŹĻąĶ¬
B. “ļĘ½ŗāŹ±£¬Į½øöČŻĘ÷ÖŠXY3µÄĪļÖŹµÄĮæÅØ¶Č¾łĪŖ2 mol”¤L£1
C. ČŻĘ÷¢Ł”¢¢Ś“ļµ½Ę½ŗāŹ±¼äĻąĶ¬
D. ČŻĘ÷¢Ś£¬ Q“óÓŚ23£®15 kJ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©ÖŹĮæ±ČĪŖ51£ŗ32£ŗ34µÄNH3”¢CH4”¢H2S£¬ĘäĪļÖŹµÄĮæÖ®±ČĪŖ__________£¬ĖüĆĒĖłŗ¬ĒāŌ×ÓŹżÖ®±ČĪŖ_________£¬Ėłŗ¬ÖŹ×ÓŹżÖ®±ČĪŖ__________”£
£Ø2£©ÓŠ7.8gNa2Rŗ¬Na+ĪŖ0.2mol£¬ŌņNa2RµÄĦ¶ūÖŹĮæĪŖ__________£¬RµÄĻą¶ŌŌ×ÓÖŹĮæĪŖ_________”£
£Ø3£©ŌŚ150”ćC£¬m gNH4HCO3¹ĢĢåĶźČ«·Ö½āÉś³ÉNH3”¢CO2”¢H2O£¬ČōĖłµĆ»ģŗĻĘųĢå¶ŌH2µÄĻą¶ŌĆܶČĪŖd£¬ŌņÓĆŗ¬m”¢dµÄ“śŹżŹ½±ķŹ¾»ģŗĻĘųĢåµÄĪļÖŹµÄĮæĪŖ_________£»ÓĆŗ¬m”¢dµÄ“śŹżŹ½±ķŹ¾NH4HCO3µÄĦ¶ūÖŹĮæĪŖ________________”£
£Ø4£©Ä³»ÆѧŠĖȤŠ”×é¶Ō”°Å©·ņɽČŖ”±æóČŖĖ®½ųŠŠ¼ģ²āŹ±£¬·¢ĻÖ1.0 LøĆæóČŖĖ®ÖŠŗ¬ÓŠ45.6 mg Mg2£«£¬ŌņøĆæóČŖĖ®ÖŠMg2£«µÄĪļÖŹµÄĮæÅضČĪŖ_______”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com