
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:黑龙江省大庆实验中学2010-2011学年高二上学期期末考试化学试题 题型:022
火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的.
(1)脱硝.利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为________.
(2)脱碳.将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ΔH3
CH3OH(g)+H2O(g)ΔH3
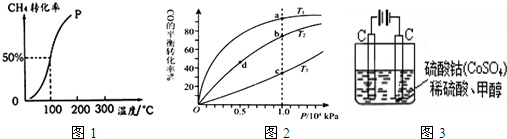
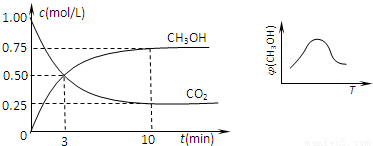
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如下图所示,则上述CO2转化为甲醇的反应的ΔH3________0(填“>”、“<”或“=”).
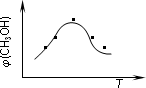
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应.测得CO2和CH3OH(g)的浓度随时间变化如下图所示.下列说法正确的是________(填字母代号).
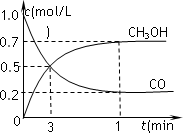
A.第10 min后,向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时c(CH3OH)=1.5 mol·L-1
B.0-10 min内,氢气的平均反应速率为0.075 mol/(L·min)
C.达到平衡时,氢气的转化率为0.75
D.该温度下,反应的平衡常数的值为3/16
E.升高温度将使n(CH3OH)/n(CO2)减小
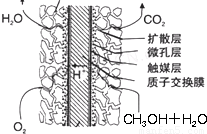
③甲醇燃料电池结构如下图所示.其工作时正极的电极反应式可表示为________.
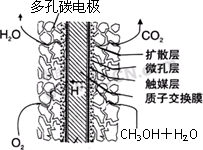
(3)硫酸铵和硝酸铵的水溶液的pH<7,其中原因可用一个离子方程式表示为:________;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中c(Na+)+c(H+)________c(NO3-)+c(OH-)(填写“>”“=”或“<”)
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省高三百校大联考一模考试化学试卷 题型:选择题
正丁醛可在羰基钴催化下由丙烯氢甲酰化获得:CH3CH=CH2+CO+H2 CH3CH2CH2CHO(正丁醛)副反应:CH3CH=CH2+CO+H2
CH3CH2CH2CHO(正丁醛)副反应:CH3CH=CH2+CO+H2 (CH3)2CHCHO(异丁醛),温度对丙烯氢甲酰化产物中正/异醛比的影响如下图:
(CH3)2CHCHO(异丁醛),温度对丙烯氢甲酰化产物中正/异醛比的影响如下图:
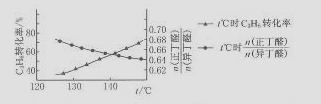
下列说法正确的是 ( )
A.丙烯氢甲酰化反应是放热反应
B.丙烯与CO4H2混合催化时,可能有丙烷及正丁醇等副产物生成
C.相同物质的量的丙烯合成正丁醛时,温度越高,所获得的正丁醛的产量一定越大
D.温度不变时,只改变体系的压强,对产率没有影响
查看答案和解析>>
科目:高中化学 来源:2011年北京市东城区示范校高考化学综合练习试卷(一)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com