
·ÖĪö £Ø1£©FeµÄŌ×ÓŠņŹżĪŖ26£¬Ō×Ó½į¹¹ÖŠÓŠ4øöµē×Ó²ć£¬×īĶā²ćµē×ÓŹżĪŖ2£»
£Ø2£©FeCl3ČÜŅŗæÉĪüŹÕSO2£¬·¢ÉśŃõ»Æ»¹Ō·“Ó¦£»
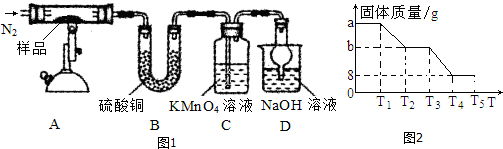
£Ø3£©ÓÉĮ÷³ĢæÉÖŖ£¬ĻČĶØČėµŖĘų£¬Åųö×°ÖĆÖŠµÄæÕĘų£¬·ĄÖ¹ŃĒĢśĄė×Ó±»Ńõ»Æ£¬ŌŚAÖŠ³ä·Ö¼ÓČČĮņĖįŃĒĢś¾§Ģå£ØFeSO4•xH2O£©£¬µŖĘųÄܽ«·Ö½ā²śĪļÅųö£¬BÖŠĮņĖįĶæɼģŃéĖ®£¬CÖŠČÜŅŗĶŹÉ«£¬æÉÖŖCÖŠ¶žŃõ»ÆĮņÓėøßĆĢĖį¼Ų·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬D×°ÖĆĪüŹÕĪ²Ęų£¬×°ÖĆBÖŹĮæŌö¼Ó9.0g£¬ĪŖĖ®µÄÖŹĮ棬½įŗĻŌ×ÓŹŲŗć¼°ÖŹĮæ¹ŲĻµ¼ĘĖćx£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ£Ø1£©FeµÄŌ×ÓŠņŹżĪŖ26£¬Ō×Ó½į¹¹ÖŠÓŠ4øöµē×Ó²ć£¬×īĶā²ćµē×ÓŹżĪŖ2£¬Ī»ÓŚÖÜĘŚ±ķÖŠµŚĖÄÖÜĘŚ¢ų×壬¹Ź“š°øĪŖ£ŗĖÄ£»¢ų£»
£Ø2£©FeCl3ČÜŅŗæÉĪüŹÕSO2£¬·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬Ąė×Ó·“Ó¦ĪŖ2Fe3++SO2+2H2O=2Fe2++SO42-+4H+£¬¹Ź“š°øĪŖ£ŗ2Fe3++SO2+2H2O=2Fe2++SO42-+4H+£»
£Ø3£©ÓÉĮ÷³ĢæÉÖŖ£¬ĻČĶØČėµŖĘų£¬Åųö×°ÖĆÖŠµÄæÕĘų£¬·ĄÖ¹ŃĒĢśĄė×Ó±»Ńõ»Æ£¬ĒŅÄܽ«·Ö½ā²śĪļÅųö£¬ŌŚAÖŠ³ä·Ö¼ÓČČĮņĖįŃĒĢś¾§Ģå£ØFeSO4•xH2O£©£¬BÖŠĮņĖįĶæɼģŃéĖ®£¬CÖŠČÜŅŗĶŹÉ«£¬æÉÖŖCÖŠ¶žŃõ»ÆĮņÓėøßĆĢĖį¼Ų·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬D×°ÖĆĪüŹÕĪ²Ęų£¬
¢Ł×°ÖĆAÖŠŠč³ÖŠųĶØČėN2£¬ĘäÄæµÄŹĒ³ÖŠų³äČėµŖĘų£¬æÉÅųż×°ÖĆÖŠµÄæÕĘų£¬½«¾§Ģå·Ö½āµÄĘųĢå²śĪļČ«²æ“ÓAÖŠÅųö£¬
¹Ź“š°øĪŖ£ŗ³ÖŠų³äČėµŖĘų£¬æÉÅųż×°ÖĆÖŠµÄæÕĘų£¬½«¾§Ģå·Ö½āµÄĘųĢå²śĪļČ«²æ“ÓAÖŠÅųö£»
¢ŚAÖŠ²ŠĮōÓŠŗģ×ŲÉ«¹ĢĢ壬BÖŠ¹ĢĢå±äĄ¶£¬CÖŠČÜŅŗĶŹÉ«£¬æÉÖŖ¼ÓČČ·Ö½āÉś³ÉŃõ»ÆĢś”¢¶žŃõ»ÆĮņ£¬½įŗĻŌ×Ó¼°µē×ÓŹŲŗćæÉÖŖ£¬·“Ó¦ĪŖ2FeSO4$\frac{\underline{\;\;”÷\;\;}}{\;}$Fe2O3+SO2”ü+SO3”ü£¬
¹Ź“š°øĪŖ£ŗ2FeSO4$\frac{\underline{\;\;”÷\;\;}}{\;}$Fe2O3+SO2”ü+SO3”ü£»
¢Ū×°ÖĆDÖŠøÉŌļ¹ÜµÄ×÷ÓĆĪŖ·ĄÖ¹ĒāŃõ»ÆÄĘČÜŅŗµ¹Īü£¬¹Ź“š°øĪŖ£ŗ·ĄÖ¹ĒāŃõ»ÆÄĘČÜŅŗµ¹Īü£»
¢Ü×°ÖĆBÖŹĮæŌö¼Ó9.0g£¬ĪŖĖ®µÄÖŹĮ棬ÓÉĶ¼æÉÖŖ×īŗóµĆµ½Ńõ»ÆĢśĪŖ8g£¬
ÓÉ2FeSO4$\frac{\underline{\;\;”÷\;\;}}{\;}$Fe2O3+SO2”ü+SO3”ü”¢FeSO4•xH2OæÉÖŖ£¬
Fe2O3”«2xH2O
160 36x
8g 9g
$\frac{160}{36x}=\frac{8g}{9g}$£¬½āµĆx=5£¬
¹Ź“š°øĪŖ£ŗ5£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄŠŌÖŹ¼°ĪļÖŹ×é³ÉµÄ²ā¶Ø£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŹµŃé×°ÖƵÄ×÷ÓĆ”¢ĪļÖŹµÄŠŌÖŹ”¢ĪļÖŹ»ÆѧŹ½¼ĘĖć·½·ØĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėŹµŃéÄÜĮ¦µÄ漲飬ĢāÄæÄѶČÖŠµČ£®


 Č«ÓÅ漵䵄ŌŖ¼ģ²ā¾ķ¼°¹éĄą×Üø“Ļ°ĻµĮŠ“š°ø
Č«ÓÅ漵䵄ŌŖ¼ģ²ā¾ķ¼°¹éĄą×Üø“Ļ°ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | PŹĒŃõ»Æ¼Į | B£® | Ńõ»ÆŠŌH2O2£¾Na2H2P2O6 | ||
| C£® | 1mol H2O2·“Ó¦£¬×ŖŅʵē×Ó1mol | D£® | Na2H2P2O6ÖŠĮ×ŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ+3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
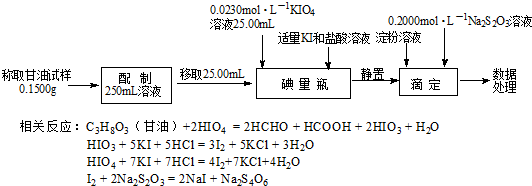
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚÓŠ»śĪļÖŠĢ¼Ō×ÓÓėĘäĖūŌ×Ó×ī¶ąŠĪ³É4 øö¹²¼Ū¼ü | |
| B£® | ÓĆäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ¼ČæÉŅŌ¼ų±š¼×ĶéŗĶŅŅĻ©£¬Ņ²æÉŅŌ³żČ„¼×ĶéÖŠµÄŅŅĻ© | |
| C£® | ĆŗøÉĮóŗóµÄĆŗ½¹ÓĶÖŠŗ¬ÓŠ±½”¢¼×±½”¢¶ž¼×±½µČÓŠ»śĪļ£¬æÉŅŌĶعżŻĶČ”µÄ·½·Ø½«ĘäĢį“æ³öĄ“ | |
| D£® | ÓĆĖįŠŌøßĆĢĖį¼ŲČÜŅŗæÉŅŌ¼ų±š¼ŗĶéŗĶ¼×±½ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µćŹÆ³É½š | B£® | ¾ĘĻć²»ÅĀĻļ×ÓÉī | C£® | µĪĖ®³É±ł | D£® | Ģś°ōÄ„³ÉÕė |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ū¢Ż | B£® | ¢Ł¢Ū | C£® | ½öÓŠ¢Ż | D£® | ¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²ÉČ”µĶĢ¼”¢½Ś¼óµÄÉś»ī·½Ź½ | |
| B£® | °“ÕÕ¹ę¶Ø¶ŌÉś»ī·ĻĘśĪļ½ųŠŠ·ÖĄą·ÅÖĆ | |
| C£® | ¾³£Ź¹ÓĆŅ»“ĪŠŌæź×Ó”¢Ö½±”¢ĖÜĮĻ“üµČ | |
| D£® | øĽųĘū³µĪ²Ęų¾»»Æ¼¼Źõ£¬¼õÉŁ“óĘųĪŪČ¾ĪļµÄÅÅ·Å |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com