

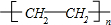 ,据此解答.
,据此解答.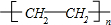 ,
,| 催化剂 |
| Cu |
| △ |
| 浓硫酸 |
| △ |
| 催化剂 |
| 催化剂 |
 ,
,| 催化剂 |
| Cu |
| △ |
| 浓硫酸 |
| △ |
| 催化剂 |
 ;
;| 催化剂 |


科目:高中化学 来源: 题型:
 喷泉是一种常见的自然现象,其产生原因是存在压强差.图中为化学教学中所用的喷泉实验装置实验装置.已知3NO2+H2O=2HNO3+NO (NO为气体,难溶于水)在烧瓶中充满干燥NO2气体,胶头滴管及烧杯中分别盛有水进行喷泉实验.假设实验在标准状况下进行,经充分反应后,计算瓶内HNO3溶液的物质的量浓度为多少?
喷泉是一种常见的自然现象,其产生原因是存在压强差.图中为化学教学中所用的喷泉实验装置实验装置.已知3NO2+H2O=2HNO3+NO (NO为气体,难溶于水)在烧瓶中充满干燥NO2气体,胶头滴管及烧杯中分别盛有水进行喷泉实验.假设实验在标准状况下进行,经充分反应后,计算瓶内HNO3溶液的物质的量浓度为多少?查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠在氯气中燃烧,生产食盐 |
| B、二氧化锰和浓盐酸共热,制取氯气 |
| C、氯气与消石灰反应,生产漂白粉 |
| D、氢气和氯气混合见光爆炸制氯化氢,再生产盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 5 |
| A、1.4mol/L |
| B、2.5mol/L |
| C、无法计算 |
| D、5.0mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
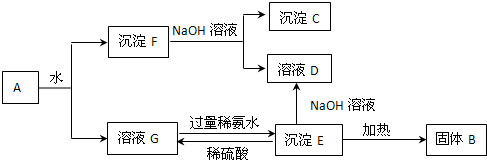
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由于燃烧均为放热反应,所以石墨为重要的能源 |
| B、由于燃烧反应放热,所以△H1和△H2均取正值 |
| C、由于石墨和金刚石同为碳元素组成,所以△H1=△H2 |
| D、由于石墨和金刚石属于不同的单质,所以△H1和△H2不等 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、图Ⅰ可能是不同压强对反应的影响,且P2>P1,a>n |
| B、图Ⅱ可能是在同温同压下催化剂对反应的影响,且2使用的催化剂效果好 |
| C、图Ⅱ可能是不同压强对反应的影响,且P1>P2,n=a+b |
| D、图Ⅲ可能是不同温度对反应的影响,且T1>T2,Q>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com