
| A. | 金属钠着火时,立即用沾水的毛巾覆盖 | |
| B. | 将含有硫酸的废液倒人水池,用大量水冲人下水道 | |
| C. | 锌和稀硫酸反应生成的氢气可直接点燃,观察火焰的颜色 | |
| D. | 大量氯气泄漏时,迅速离开现场并尽量往高处去 |
分析 A.钠化学性质非常活泼,能够与水发生反应,不能使用沾水的毛巾灭火;
B.硫酸具有腐蚀性,能够腐蚀地下管道、污染地下水,应该倒入指定的废液缸中;
C.氢气具有可燃性,注意防止发生爆炸;
D.氯气密度比空气大.
解答 解:A.钠能够与水反应生成氢氧化钠和氢气,所以钠着火不能使用沾水的毛巾覆盖,可以使用砂子灭火,故A错误;
B.若将含有硫酸的废液倒入水池,用大量水冲入下水道,会腐蚀地下管道、污染地下水,应该将含有硫酸的废液倒入废液缸中,故B错误;
C.氢气具有可燃性,为防止发生爆炸,点燃氢气前必须验纯,故C错误;
D.氯气密度比空气大,氯气是一种有毒的气体,当有大量氯气泄漏时,人应沿逆着风向方向疏散,故D正确.
故选D.
点评 本题考查了化学实验及安全事故的处理、常见生活环境及治理,题目难度不大,注意掌握常见化学试剂的性质及正确处理安全事故的方法,做到人身、财产安全.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+,无K+ |
| B | 将SO2和CO2气体分别通入水中至饱和,立即用pH计测两溶液的pH | 前者的pH小于后者 | H2SO3酸性强于H2CO3 |
| C | 铝热剂溶于足量稀盐酸再滴加KSCN溶液 | 未出现血红色 | 铝热剂中不能确定是否含有铁的氧化物 |
| D | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入几滴新制Cu(OH)2悬浊液,加热 | 没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
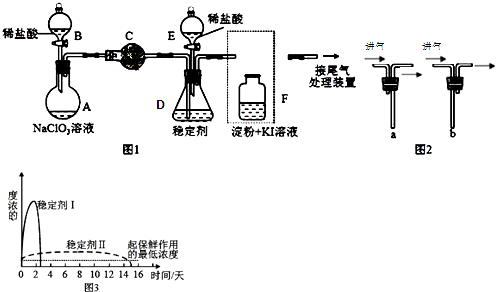
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
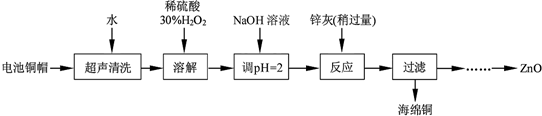
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Fe3+、OHˉ、SO42ˉ | B. | Mg2+、Na+、Clˉ、SO42ˉ | ||
| C. | NH4+、Mg2+、NO3-、OHˉ | D. | H+、K+、NO3-、CO32ˉ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2g | B. | 5.6g | C. | 2.8g | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Na+、NO3-、Cl- | B. | K+、Na+、Cl-、NO3- | ||
| C. | K+、Na+、Cl-、AlO2- | D. | K+、NH4+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 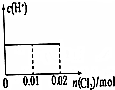 | B. |  | C. | 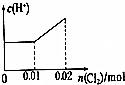 | D. |  |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com