
【题目】无水氯化铝常作为有机合成和石油化工的催化剂,并用于处理润滑油等。工业上可由金属铝和纯净的氯气作用制备。某课外兴趣小组在实验室里,通过下图所示装置,制取少量纯净的无水氯化铝。据此回答下列问题:
查阅资料:常温下,无水氯化铝为白色晶体,易吸收水分,在178℃升华。装有无水氯化铝的试剂瓶久置潮湿空气中,会自动爆炸并产生大量白雾。

(1)写出A装置中,实验室制取Cl2的离子方程式________________。
(2)仪器甲______(写名称);仪器乙________(写名称)
(3)在E处可收集到纯净的氯化铝,F装置所起的作用是__________。
(4)装置B、C中的试剂分別是_________________。
(5)从A装置中导出的气体若不经过B、C装置而直接进入D装置中,产生的后果是______________。
【答案】 4H++2Cl-+MnO2![]() Mn2++Cl2↑+2H2O 分液漏斗 圆底烧瓶 防止外界水蒸气进入 饱和食盐水,浓硫酸 引起爆炸(合理均可)
Mn2++Cl2↑+2H2O 分液漏斗 圆底烧瓶 防止外界水蒸气进入 饱和食盐水,浓硫酸 引起爆炸(合理均可)
【解析】(1)根据流程图,A装置是制取氯气的装置,实验室制取Cl2的离子方程式为4H++2Cl-+MnO2![]() Mn2++Cl2↑+2H2O,故答案为:4H++2Cl-+MnO2
Mn2++Cl2↑+2H2O,故答案为:4H++2Cl-+MnO2![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(2)根据装置图,仪器甲为分液漏斗;仪器乙为圆底烧瓶,故答案为:分液漏斗;圆底烧瓶;
(3) 氯化铝易吸收水分,为了防止外界水蒸气进入,需要用F中的碱石灰吸收,故答案为:防止外界水蒸气进入;
(4)制取的氯气中含有氯化氢和水蒸气,装置B中装入饱和食盐水,除去氯化氢、装置C中装入浓硫酸,除去水蒸气,故答案为:饱和食盐水;浓硫酸;
(5)从A装置中导出的气体若不经过B、C装置而直接进入D装置中,潮湿的氯化氢与铝反应生成氢气,会引起爆炸,故答案为:引起爆炸。


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】使1.0体积的某气态烷烃和烯烃的混合气体在足量空气中完全燃烧,生成2.0体积的二氧化碳和2.2体积的水蒸气(均在120℃、1.01×105Pa条件下测定),则混合气体中烷烃和烯烃的体积比为
A. 2:3 B. 1:4 C. 4:1 D. 3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,表中所列字母分别代表一种元素。
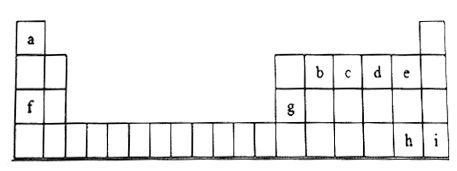
根据表格所给信息,回答下列问题:
(1)c元素原子的最高价氧化物对应的水化物的化学式___________(填化学式)
(2)b、c、d、e的原子半径依次_______(填“增大”或“减小”)
(3)e、h元素原子形成的氢化物中,热稳定性大的是__________(填氢化物的化学式)
(4)f、g元素的最高价氧化物对应水化物之间发生反应的化学方程式__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素的性质及其递变规律正确的是( )
A. 第二周期元素从左到右,最高正价从+1递增到+7
B. 同一主族的元素,原子半径越大,越容易失去电子,其单质的氧化性越强
C. 最外层电子数比次外层电子数多的元素一定位于第二周期
D. 碱金属元素是指ⅠA族的所有元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃A、B组成的混合气体完全燃烧后得到CO2和H2O(g)的物质的量随混合烃的总物质的量的变化如图所示,则下列说法正确的是( )

A. 混合烃中一定不含有乙烯 B. 混合烃中n(C)∶n(H)=2∶5
C. 若混合烃为CH4、C3H4,则体积比为3∶7 D. 若混合烃为CH4、C4H4,则体积比为4∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:

(1)步骤①获得Br2的离子反应方程式为:________________________________________;
(2)步骤③所发生反应的化学方程式为:________________________________________。在该反应中,氧化剂是______________(填化学式);若反应中生成2molHBr,则转移电子数约为_____________个。
(3)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是:_______________
(4)步骤②通入热空气或水蒸气吹出Br2,利用了溴的________。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(5)提取溴单质时,蒸馏溴水混合物Ⅱ而不是蒸馏溴水混合物Ⅰ,请说明原因:________________。(6)步骤⑤的蒸馏过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,请解释原因:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得70℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是( )

A. 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 图乙表明,其他条件相同时,溶液PH 越小,H2O2分解速率越快
C. 图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快
D. 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 乙酸、水、乙醇和金属钠反应剧烈程度,从剧烈到逐渐平缓
B. 淀粉和纤维素的组成可用(C6H10O5)n 表示,它们互为同分异构体
C. 硝酸不慎滴到皮肤上,发现皮肤变黄
D. 苯的结构式虽然用![]() 表示,但苯的结构却不是单、双键交替组成的环状结构,可以从它的邻二氯代物结构只有一种得到证明
表示,但苯的结构却不是单、双键交替组成的环状结构,可以从它的邻二氯代物结构只有一种得到证明
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铝是一种具有广泛用途的重要化工产品,以高岭土(含SiO2、A12O3、少量Fe2O3 等)为原料制备硫酸铝晶体[Al2(SO4)3·18H2O]的实验流程如图所示。

回答以下问题
(1)高岭土需进行粉粹,粉粹的目的是_____________________。
(2)滤渣1经过处理可作为制备水玻璃(Na2SiO3水溶液)的原料,写出滤渣1与烧碱溶液反应的化学方程式____________________________________。
(3)加入试剂除铁前,滤液1中的阳离子除了Al3+、Fe3+外还有的阳离子是__________(填离子符号)。滤渣2主要成分为Fe(OH)3,由于条件控制不当,常使Fe(OH)3 中混有Al(OH)3影响其回收利用,用离子方程式表示除去A1(OH)3的原理____________________________________________。
(4)检验滤液2中是否含有Fe3+的实验方法是(要求写出实验步骤和现象):__________________。
(5)要从滤液2获取硫酸铝晶体需要经过多步处理,其中从溶液中得到晶体的方法是__________(填标号)。
a.蒸发结晶 b.蒸发浓缩、冷却结晶
(6)某兴趣小组为了测定晶体中Al2(SO4)3·18H2O(M=666g·mol-1)的质量分数,进行如下实验:
①准确称取l.00g晶体样品,溶于一定量水中;
②滴入0.100 mol·L-1 EDTA溶液,与Al3+反应所消耗EDTA溶液的体积25.00 mL。 (已知:EDTA与Al3+以物质的量之比1∶1反应,假设杂质不与EDTA反应)则晶体中Al2(SO4)3·18H2O的质量分数是__________;若样品中的杂质离子能与EDTA反应,所测定质量分数将会__________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com