
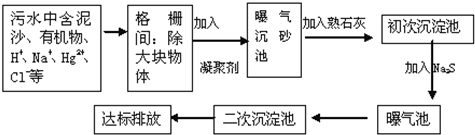
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含纯碱的废水 | 加石灰水反应 | 化学法 |
| m |
| M |
| 13g |
| 65g/mol |
| m |
| M |


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
| A、v(N2)=0.01 mol?(L?s)-1,v(H2)=0.02 mol?(L?s)-1 |
| B、v(H2)=0.02 mol?(L?s)-1,v(NH3)=0.02 mol?(L?s)-1 |
| C、v(N2)=0.01 mol?(L?s)-1,v(NH3)=0.03 mol?(L?s)-1 |
| D、v(H2)=0.06 mol?(L?s)-1,v(NH3)=0.04 mol?(L?s)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
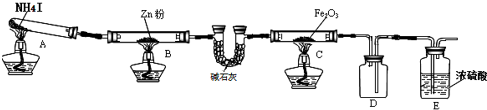
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 3 | 向步骤2溶液中滴加新制氯水 | 红色先变深后褪去 | 先变红后也褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
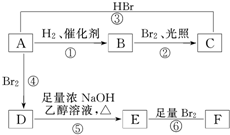 (1)某元素的基态原子最外层电子排布为3s23p2,它的次外层上电子云形状有
(1)某元素的基态原子最外层电子排布为3s23p2,它的次外层上电子云形状有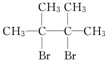
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一氯乙烷的结构式CH3Cl |
| B、丁烷的结构简式CH3(CH2)2CH3 |
C、四氯化碳的电子式 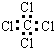 |
D、C2H4分子比例模型: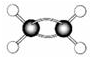 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com