
| �¶ȣ��棩 | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| ƽ��������Ũ�� ��10-3mol/L�� | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
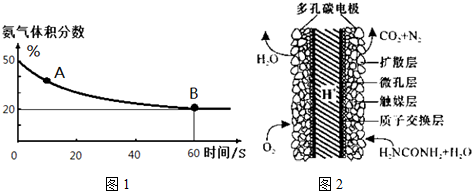
���� ��1��ͼ��������������������50%�仯Ϊ20%������������ֲ��䣬˵��B�㷴Ӧ�ﵽƽ��״̬��A�㰱������ٷֺ�������B�İ�������ٷֺ�����˵����Ӧ������дﵽƽ��״̬��A�������Ӧ���ʴ���B�������Ӧ���ʣ����ݰ���������������ƽ������ʽ��ʽ����ƽ��ת���ʣ�
��2���ٸ��ݱ��е����ݷ������¶�Խ�ߣ���ƽ���������Ũ��Խ�����������¶ȣ�ƽ�������ƶ�������Ӧ��Ӧ�Ƿ��ȷ�Ӧ��
��Ӧ�������壬�����ǹ��壬�÷�Ӧ���ؼ�С�Ĺ��̣�
��A����Ϊ���������Ϊ���壬����������İ�������泥�ƽ�ⲻ�ƶ���
B�����������Ϊ���壬����NH3��CO2ʼ��Ϊ2��1��
C����Ϊ�����Ϊ2��1��NH3��CO2���������뷴Ӧ��NH3��CO2�ְ���2��1�����ģ�����NH3��ת����ʼ�յ���CO2��ת���ʣ�
D������ֻ�ı����ʣ����ı�ƽ���ƶ����ɴ˽����жϣ�
�۸��ݰ�������識���ˮ���̼��泥�����ӦʽΪNH2COONH4��s��+H2O?��NH4��2CO3������������立�ĩ����1L0.1mol/L��������Һ��ֱ��pH=7������Һ�м�������̼Ԫ�أ�������Һ��ֻ��H+��NH4+��OH-��Cl-�����ݵ���غ����c��NH4+��������NH4++H2O?NH3•H2O+OH-���K=$\frac{c��NH{\;}_{3}•H{\;}_{2}O��c��H{\;}^{+}��}{c��NH{\;}_{4}{\;}^{+}��}$���м��㣻
��3������ȼ�ϵ���������ٸ�����ʧȥ�������ɵ�����������̼��
��� �⣺��1�����������������50%�仯Ϊ20%������������ֲ��䣬˵��B�㷴Ӧ�ﵽƽ��״̬��A�㰱������ٷֺ�������B�İ�������ٷֺ�����˵����Ӧ������дﵽƽ��״̬��A�������Ӧ���ʴ���B�������Ӧ���ʣ���v����CO2����v����CO2����
�谱���������ʵ���x����ʼ�����������Ϊ50%�����谱��Ϊ50mol��������̼Ϊ50mol��
CO2+2NH3?��NH2��2CO+H2O
��ʼ����mol�� 50 50 0 0
�仯����mol�� 0.5x x 0.5x 0.5x
ƽ������mol�� 50-0.5x 50-x 0.5x 0.5x
�������������=$\frac{50-x}{50-0.5x+50-x+0.5x}$=20%�����x=37.5mol��
������ƽ��ת����=$\frac{37.5mol}{50mol}$��100%=75%��
�ʴ�Ϊ������75%��
��2���ٸ��ݱ��е����ݷ������¶�Խ�ߣ���ƽ���������Ũ��Խ�����������¶ȣ�ƽ�������ƶ�������Ӧ��Ӧ�Ƿ��ȷ�Ӧ���ʡ�H��0��
��Ӧ�������壬�����ǹ��壬�÷�Ӧ���ؼ�С�Ĺ��̣�������S��0����ѡ��A��
��A����Ϊ���������Ϊ���壬����������İ�������泥�ƽ�ⲻ�ƶ������Է�Ӧ���ת���ʲ��䣬��A����
B��ƽ��ʱ������ϵ�¶ȣ�ƽ������ȷ�������Ӧ�����ƶ����ְ��������Ϊ���壬����NH3��CO2ʼ��Ϊ2��1����CO2������������䣬��B����
C����Ϊ�����Ϊ2��1��NH3��CO2���������뷴Ӧ��NH3��CO2�ְ���2��1�����ģ�����NH3��ת����ʼ�յ���CO2��ת���ʣ���C��ȷ��
D������ֻ�ı����ʣ����ı�ƽ���ƶ������Լ�����Ч�Ĵ������ܹ���߰�������淋IJ��ʣ���D����
��ѡ��C��
����Ϊ��������識���ˮ���̼��泥�����ӦʽΪNH2COONH4��s��+H2O?��NH4��2CO3������1L0.1mol/L��������Һ��ֱ����ҺpH=7������Һ�м�������̼Ԫ�أ�������Һ��ֻ��H+��NH4+��OH-��Cl-�����ݵ���غ�c��NH4+��=c��Cl-��=0.1mol/L������ȥ0.052mol��������泥����Կ�ʼ��Һ�е�笠�����Ũ��Ϊ0.052mol/L��2=0.104mol/L��
NH4++H2O?NH3•H2O+H+��
��ʼ 0.104mol/L 0
ת�� 0.004mol/L 0.004mol/L
ƽ�� 0.1mol/L 0.004mol/L
����ҺΪpH=7������������Ũ��Ϊ10-7mol/L����NH4+ˮ��ƽ�ⳣ��K=$\frac{c��NH{\;}_{3}•H{\;}_{2}O��c��H{\;}^{+}��}{c��NH{\;}_{4}{\;}^{+}��}$=$\frac{0.004��10{\;}^{-7}}{0.1}$=4��10-9���ʴ�Ϊ��0.1mol/L��4��10-9��
��3������ȼ�ϵ���������ٸ�����ʧȥ�������ɵ�����������̼��������ӦΪCO��NH2��2+H2O-6e-�TN2��+CO2��+6H+���ʴ�Ϊ��CO��NH2��2+H2O-6e-�TN2��+CO2��+6H+��
���� ���⿼�黯ѧ��Ӧ���ʡ���ѧƽ����ƶ�ԭ�����������������Һ�е�ˮ��ƽ��ļ���Ӧ���Լ�ȼ�ϵ�ظ�����Ӧʽ����д��֪ʶ���ۺ��Խϴ��Ѷ��еȣ�


 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ԫ�ط�����ȷ���л�����������ʱ����������Ʒ��С�������ٶȿ���ŵ� | |
| B�� | ���ڷ����Զ���ȷ���л������Ƿ���C��H��O��Ԫ�� | |
| C�� | �ⶨ�л����������Ԫ�صķ������к˴Ź�������ȷ��� | |
| D�� | ���Ѻ��Ҵ���ͬ���칹�壬�����ں˴Ź������г��ֵ�������ֱ���1����2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
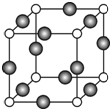
 ˫��ˮ��һ�ֶԻ����Ѻõ���������Ư�����㷺Ӧ���ڻ�����ҽҩ��������������ش��������⣺
˫��ˮ��һ�ֶԻ����Ѻõ���������Ư�����㷺Ӧ���ڻ�����ҽҩ��������������ش��������⣺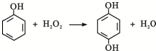 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij��ɫ��Һ�У�NH4+��Na+��Cl-��MnO4- | |
| B�� | ��������ˮ�������c��H+��=1��10-13mol•L-1����Һ�У�Na+��K+��SO32-��CO32- | |
| C�� | ��c��H+��=1��10-13mol•L-1����Һ�У�NH4+��Al3+��SO42-��NO3- | |
| D�� | ��pH=1����Һ�У�K+��Mg2+ SiO32- SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ���ѽ����ҪĿ����������͵������͵IJ�����������ʯ�ʹ��ѻ�����ҪĿ���ǵõ��������ϩ����ϩ����̬������ | |
| B�� | Ŀǰ��ѧ���Ѿ��Ƶõ�ԭ�Ӳ��࣬�����Ǩ�����ǹ��10��������ȡ��������������õľ���� | |
| C�� | ����β����ת��װ�ÿɽ�β���е�NO��CO���к�����ת��ΪN2��CO2����װ���еĴ����ɽ���NO��CO��Ӧ�Ļ�ܣ���������߸÷�Ӧ��ƽ��ת���� | |
| D�� | ���������ǹ��ұ����İ���������ʼ�������֮�ƣ���֪�ò����Ի�ѧҩƷ���У��Ҵ�������������Һ�����Խ������������ﵽ������Ŀ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�14 g C2H4��C3H6�Ļ�������к���̼ԭ�ӵ���ĿΪNA | |
| B�� | �����£�pH=12��Na2CO3��Һ�к��е�OH-������Ϊ0.01NA | |
| C�� | ��״���£�0.56 L�����к��й��ۼ�����ĿΪ0.2 NA | |
| D�� | 7.8 g Na2O2�к��е���������Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��֪ A��B��C��D��ԭ������������������ֶ���������Ԫ�أ�A������������������������Bԭ�ӵļ۵����Ų�Ϊnsnnpn��D�ǵؿ��к�������Ԫ�أ�E�ǵ������ڵ�p��Ԫ���������ֻ��2�ԳɶԵ��ӣ�FԪ�صĻ�̬ԭ�ӵ����ܲ�ֻ��һ�����ӣ������ܲ���ѳ������ӣ�
��֪ A��B��C��D��ԭ������������������ֶ���������Ԫ�أ�A������������������������Bԭ�ӵļ۵����Ų�Ϊnsnnpn��D�ǵؿ��к�������Ԫ�أ�E�ǵ������ڵ�p��Ԫ���������ֻ��2�ԳɶԵ��ӣ�FԪ�صĻ�̬ԭ�ӵ����ܲ�ֻ��һ�����ӣ������ܲ���ѳ������ӣ�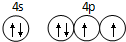 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ������ | ������ |
| A | Ũ�����ڹ�������ɫ��� | Ũ������в��ȶ��� |
| B | Cl2��SO2��Ư���� | Cl2��SO2����ʹ���з�̪��NaOH��Һ��ɫ |
| C | ����������Ũ�����Ӧ | �������۳��ܷ�����Ũ���� |
| D | SiO2�е����� | SiO2�������Ʊ����ά |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ǻ��Ļ�����һ�����ڴ��� | |
| B�� | ���и��������������ǻ����л���һ���Ǵ��� | |
| C�� | ����ʹ��������ͬ�Ĺ����ţ����������ͬ�Ļ�ѧ���� | |
| D�� | �������б������ǻ��Ļ�����һ���Ƿ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com