
����Ŀ�������仯������NH3����Ρ�N2H4��N2O4������ѧ��ѧ��������ҵ������������ռ����Ҫ��λ��
��1�����亽����������(N2H4)��N2O4��ȼ������ȼ������(N2H4)��N2O4�ķ�ӦΪ2N2H4(1)+N2O4(g)=3N2(g)+4H2O(g) ��H = -1077 kJ/mol
��֪��ط�Ӧ�Ļ�ѧ�������������£�
![]()
��ʹ1 mol N2O4(g)�����л�ѧ����ȫ����ʱ��Ҫ���յ�������__________ ��
��2��N2O4��NO2֮����ڷ�ӦN2O4(g)![]() 2NO2(g)����һ������N2O4��������ܱ������У������ƽ��ת����[��(N2O4)]���¶ȵı仯��ͼ��ʾ��
2NO2(g)����һ������N2O4��������ܱ������У������ƽ��ת����[��(N2O4)]���¶ȵı仯��ͼ��ʾ��
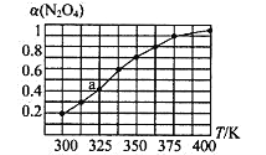
����ͼ�Ʋ�÷�Ӧ��H_______0���>����<����������Ϊ______________ ��
��ͼ��a���Ӧ�¶��£���֪N2O4����ʼѹǿp0Ϊ108 kPa������¶��·�Ӧ��ƽ�ⳣ��Ϊ��Kp=_____________����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������,ȡ��λ��Ч���֣���
����һ�������£��÷�ӦN2O4��NO2����������������ѹǿ����ڹ�ϵ��v(N2O4)=k1p(N2O4)��v(NO2)=k2p2(NO2)������k1��k2���뷴Ӧ�¶��йصij�������Ӧ�����ʣ�ѹǿ��ϵ��ͼ��ʾ��һ���¶��£�k1��k2��ƽ�ⳣ��Kp�Ĺ�ϵ��k1=________������ͼ����ĵ��У��ܱ�ʾ��Ӧ�ﵽƽ��״̬�ĵ�Ϊ______��

��3�����NO2�Ʊ�NH4NO3���乤��ԭ����ͼ��ʾ��
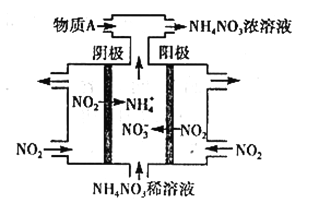
�������ĵ缫��ӦʽΪ_______________________��
��Ϊʹ������ȫ��ת��ΪNH4NO3���貹������A����A�Ļ�ѧʽΪ___________��
���𰸡� 1941 kJ > �¶����ߣ�����N2O4�����ӣ�˵��ƽ�����ơ��÷�ӦΪ���ȷ�Ӧ����H>0 115.2KPa ![]() B����D�� NO2-e-+H2O=NO3-+2H+ NH3
B����D�� NO2-e-+H2O=NO3-+2H+ NH3
����������1�����ݷ�Ӧ���ʱ��H=��Ӧ���ܼ���-�������ܼ��ܼ��㣻
��2���ٸ����¶ȶ�ƽ��״̬��Ӱ����ͼ������ж��ʱ䣻
�ڸ��ݷ�Ӧ����ʽ����ƽ��ʱ��ϵ��N2O4��NO2�ķ�ѹ�����뻯ѧƽ�ⳣ������ʽ�����ѹƽ�ⳣ����
�۵��ﵽ��ѧƽ��ʱ����v��=v�����ݴ����㻯ѧƽ�ⳣ������ʽ��������������2v��N2O4��=v��NO2���жϻ�ѧƽ��ĵ㣻
��3���ٵ�����������������Ӧ������ԭ��ͼ������NO2������ʧȥ����ת��ΪNO3-���ݴ�д�������ĵ缫��Ӧʽ��
�ڸ��ݷ�Ӧʽ�ж�A���ʡ�
��1����H=8E��N-H��+2E��N-N��+E��N2O4��-3E��N��N��-8��O-H��=-1077kJ/mol�����������ݴ��뼴�ɽ��E��N2O4��=1941kJ/mol����ʹ1 mol N2O4(g)�����л�ѧ����ȫ����ʱ��Ҫ���յ�������1941kJ��
��2���ٸ���ͼ������������¶����ߣ�N2O4��ƽ��ת��������˵�������¶������ڷ�Ӧ������У������ʱ��H��0��
��N2O4��NO2֮����ڷ�ӦN2O4(g)![]() 2NO2(g)��a����ʼʱN2O4��ѹǿΪ108kPa��N2O4��ƽ��ת����Ϊ40%����
2NO2(g)��a����ʼʱN2O4��ѹǿΪ108kPa��N2O4��ƽ��ת����Ϊ40%����
N2O4(g)![]() 2NO2(g)
2NO2(g)
��ʼ����mol�� 1 0
ת������mol�� 0.4 0.8
ƽ������mol�� 0.6 0.8
��ƽ��ʱѹǿΪ1.4p0
���Է�Ӧ�ķ�ѹƽ�ⳣ��ΪKp=p2(NO2)/p(N2O4)= ��
��
�۵��ﵽ��ѧƽ��ʱ����v��=v��������������2v��N2O4��=v��NO2��������v��N2O4��=k1p��N2O4����v��NO2��=k2p2��NO2������k1��k2��ƽ�ⳣ��Kp�Ĺ�ϵΪk1=![]() ������2v��N2O4��=v��NO2��������Ա�ʾ��ѧƽ��ĵ�ΪB���D�㣻
������2v��N2O4��=v��NO2��������Ա�ʾ��ѧƽ��ĵ�ΪB���D�㣻
��3���ٵ�����������������Ӧ������ԭ��ͼ������NO2������ʧȥ����ת��ΪNO3-���������ĵ缫��ӦʽΪ��NO2-e-+H2O=NO3-+2H+��
��������ӦʽΪNO2+7e-+8H+��NH4++2H2O�����������H+��ΪʹNO2���ȫ��ת��ΪNH4NO3������Ҫ��Ӧ��H+����NH4+�����Լ����A����ӦΪNH3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��ͬѧΪ̽��H2O2��H2SO3��Br2������ǿ�����������ʵ��(�г���������ȥ��װ�õ��������Ѽ���)��

ʵ���¼���£�

��ش��������⣺
��1��A�з�Ӧ�����ӷ���ʽ��__________________________________________________��
��2��ʵ������������ȿ�����Ŀ����_________________________________________��
��3��װ��C��������____________��C��ʢ�ŵ�ҩƷ��_____________��
��4��ʵ������������Һ��ɺ���ɫ�����Ӧ�����ӷ���ʽ_______________________��
��5��������ʵ��ó��Ľ�����_________________________________________________��
��6��ʵ�鷴˼��
����ͬѧ��Ϊʵ�������������ȿ����������(5)�н��۵ĵó�������Ϊ�Ƿ���ţ�������_____________________________________________________________________��
��ʵ�����������ʼʱ��ɫ�����Ա仯��ԭ����(д��һ������)��____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ָ������������½���ѧ��ת��Ϊ���ܵ�װ�ã��乤��ԭ����ͼ��ʾ�������й������ص�˵���������(����)

A. ����ٽ��˷�Ӧ�е��ӵ�ת��
B. ������Ӧ����CO2����
C. ����ͨ������Ĥ�Ӹ���������������
D. ����ܷ�ӦΪC6H12O6��6O2===6CO2��6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС��ͨ������װ��̽�� MnO2��FeCl3��6H2O�ܷ�Ӧ����Cl2��
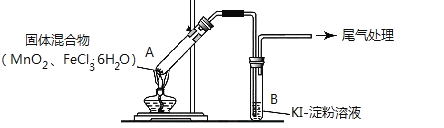
ʵ��������������±���
ʵ���� | ���� | ���� |
ʵ�� 1 | ����ͼ��ʾ����MnO2��FeCl3��6H2O����� | ���Թ�A�в��ֹ����ܽ⣬�Ϸ����ְ��� ���Ժ�����ɫ���壬�ܱڸ��Ż�ɫҺ�� ���Թ�B����Һ���� |
ʵ�� 2 | ��A�еĻ���ﻻΪFeCl3��6H2O��B����Һ��ΪKSCN��Һ�����ȡ� | A�в��ֹ����ܽ⣬���������ͻ�ɫ���壬B��KSCN��Һ��� |
�ش��������⣺
��1��ʵ��1��ʵ��2����������ԭ����___________________________��
��2��ʵ��2˵����ɫ�����к���___________���ѧʽ����ʵ��1�Т۵�����Ҳ�����Ƿ�������һ�����ӷ�Ӧ,�������ӷ���ʽΪ______________________________��
��3��Ϊ��һ��ȷ�ϻ�ɫ�����к���Cl2����ѧϰС���ʵ��1������ָĽ�������
����1����A��B ������ʢ��ij���Լ���ϴ��ƿC�����B����Һ�Ա�Ϊ��ɫ��
����2����B�е���KI��Һ�滻ΪNaBr��Һ�����B����Һ�ʳȺ�ɫ����δ���Fe2+��
��1��C��ʢ�ŵ��Լ���_________________������2�м��� Fe2+���Լ�������____________��ѡ��NaBr��Һ��������__________________��
��4��ʵ��1��ּ��Ⱥ�����Ӧ�б�������δ����������Ԫ������֮��Ϊ1:2����A�з�����Ӧ�Ļ�ѧ����ʽΪ____________________________��
��5����ѧϰС����Ϊʵ��1����Һ���������ܻ�������һ��ԭ����__________���������ʵ�鷽����֤�˲���__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��ȡŨ�Ⱦ�Ϊ0.1mol��L-1�Ĵ�����Һ�Ͱ�ˮ��Һ��20 mL���ֱ���0.1 mol��L-1NaOH��Һ��0.1 mol��L-1��������к͵ζ����ζ�������pH��μ���Һ������仯��ϵ��ͼ��ʾ������˵����ȷ����

A. �������μ���Һ��10 mLʱ��c(CH3COO��)��c(Na��)��c(H��)��c(OH��)
B. �������μ���Һ��20 mLʱ��c(Cl��)��c(NH4��)��c(OH��)��c(H��)
C. �������μ���Һ��10 mLʱ��c(CH3COO��)��c(CH3COOH)��2[c(H��)��c(OH��)]
D. �������μ���Һ��10 mL��20 mL֮�������c(NH4��)��c(Cl��)��c(OH��)��c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ȼҵ���Զ��Ե缫��ⱥ��ʳ��ˮ����ȡ�������������ռ���ȵĺ������ε�ϵ�л�����Ʒ����ͼ�����ӽ���Ĥ�����ʳ��ˮ��ʾ��ͼ��ͼ�е����ӽ���Ĥֻ����������ͨ����
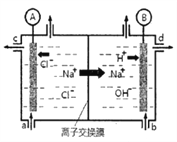
����������:
�����ӽ���Ĥ������Ϊ:____________________��
��д����ⱥ��ʳ��ˮ�����ӷ���ʽ_________��
������������Һ��ͼ��_____λ��������(ѡ��a��b��c��d)
�Ƶ绯ѧ���ճ���������;�㷺��ͼ����þ��������ȼ�ϵ�أ�����ܷ�ӦΪ��Mg��ClO����H2O===Cl����Mg(OH)2����ͼ����Cr2O![]() �Ĺ�ҵ��ˮ�Ĵ���������˵����ȷ������____��
�Ĺ�ҵ��ˮ�Ĵ���������˵����ȷ������____��
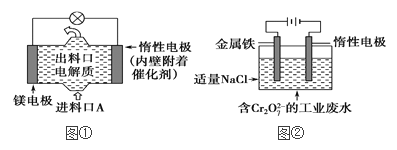
A��ͼ����Cr2O![]() ��������Ե缫�ƶ�����ü�������OH�����ת����Cr(OH)3��ȥ
��������Ե缫�ƶ�����ü�������OH�����ת����Cr(OH)3��ȥ
B��ͼ�ڵĵ����У���0.084 g�������ϲ��뷴Ӧ����������33.6 mL���������
C��ͼ���з����Ļ�ԭ��Ӧ�ǣ�Mg2����ClO����H2O��2e��===Cl����Mg(OH)2
D����ͼ����3.6 gþ�ܽ�����ĵ�������ͼ�ڷ�ˮ���������ۿɲ���10.7 g������������
�ǹ۲�����װ�ã��ش��������⣺
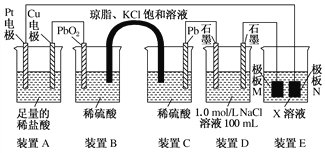
��װ��B��PbO2�Ϸ����ĵ缫��Ӧ����ʽΪ_____________________________________��
��װ��A���ܷ�Ӧ�����ӷ���ʽΪ_____________________________________________��
�۵�װ��A��Cu�缫�����ı�6.4 gʱ��װ��D�в������������Ϊ________ L(��״���£�������������ܽ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������½�������Һ�μӵ�����(N2H4)��ˮ��Һ�У������Һ�е��������ʵ���������(X)��-1g(OH-)�仯�Ĺ�ϵ��ͼ��ʾ�����������������
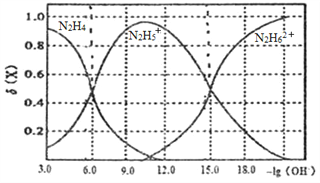
A. ��ӦN2H62++N2H4=2N2H5+��pK=90(��֪pK=-lgK)
B. N2H5Cl��Һ�д���:c(Cl-)+c(OH-)=c(N2H5+)+2c(N2H62+)+c(H+)
C. N2H5Cl��Һ��c(H+)>c(OH-)
D. Kb1(N2H4)=10-6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������X��һ�����ϣ��ɲ�����ϩ��ױ�Ϊ��Ҫԭ�ϣ�������·�ߺϳɣ�

��֪��RX![]() ROH��RCHO��CH3COOR��
ROH��RCHO��CH3COOR��![]() RCH��CHCOOR�� ��ش�
RCH��CHCOOR�� ��ش�
��1�� A�й����ŵ�������______________________��
��2�� D��E�Ļ�ѧ����ʽ________________________________________________��
��3�� X�Ľṹ��ʽ_________________��
��4����F��Ϊͬ���칹��������������������_______�֡�
�������Ȼ�����Һ������ɫ�����ᷢ��������Ӧ ��������������ȡ����
������ͬ���칹���к˴Ź�������������壬��ԭ�����ȷ���1:2:2:2:2:1�ĽṹΪ_____��
��5����������ϳ���Ϣ���Լ���д������ϩΪԭ�ϣ����Լ���ѡ����д���ϳ�CH3CH��CHCOOCH2CH3·�ߡ�_____________________
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com