



 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
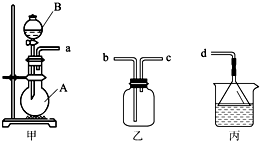 液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液.请回答下列问题:
液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
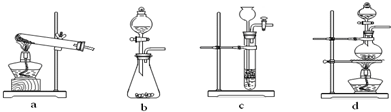
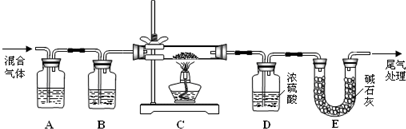
| 实验 编号 |
实验目的 | T/K | 催化剂用量/g | C/mol?l-1 | |
| KMnO4 | H2C2O4 | ||||
| ① | 为以下实验作参考 | 298 | 0.5 | 0.01 | 0.1 |
| ② | 探究KMnO4酸性溶液的浓度对该反应速率的影响 | 298 | 0.5 | 0.001 | 0.1 |
| ③ | 323 | 0.5 | 0.01 | 0.1 | |
| ④ | 探究催化剂对反应速率的影响 | 0.1 | |||
查看答案和解析>>
科目:高中化学 来源:2010-2011学年福建省高三下学期第六次模拟考试(理综)化学部分 题型:实验题
过氧化氢(H2O2)俗称双氧水,不稳定,易分解。溶液的酸碱性对H2O2的稳定性有较大影响,如在碱性溶液中,H2O2分解较快。另外,H2O2见光、遇热、遇到大多数金属氧化物分解也会加快。以下装置可用于探究H2O2相关的性质。

请回答:
(1)实验室用MnO2作催化剂分解H2O2制取氧气,反应的化学方程式为 。
使用图1装置时,H2O2应该盛放在 (填“锥形瓶”或“分液漏斗”)中,读取氧气体积时要注意 。
(2)取等物质的量浓度等体积H2O2溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如下表所示。

①实验1、2研究的是 对H2O2分解速率的影响。
②实验2、3的目的是 。
(3)用 (填“酸式”或“碱式”)滴定管量取25.00mL H2O2溶液于图II的烧瓶中,滴入过量KMnO4酸性溶液反应,最终收集到56mLO2(已折算为标准状况),则该H2O2溶液的物质的量浓度为 。
(已知:2KMnO4+5H2O2+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O)你认为测得的数值比理论值
(填“偏高”、“偏低”或“相等”)
(4)实验表明Na2O2与水反应也可生成O2。某同学猜想是Na2O2先与H2O反应生成H2O2,然后H2O2分解产生O2。为此做探究如下:取Na2O2样品(杂质不参与反应)与过量水充分反应的少量X溶液于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,该反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化氢(H2O2)俗称双氧水,不稳定,易分解。溶液的酸碱性对H2O2的稳定性有较大影响,如在碱性溶液中,H2O2分解较快。另外,H2O2见光、遇热、遇到大多数金属氧化物分解也会加快。以下装置可用于探究H2O2相关的性质。
请回答:
(1)实验室用MnO2作催化剂分解H2O2制取氧气,反应的化学方程式为 。
使用图1装置时,H2O2应该盛放在 (填“锥形瓶”或“分液漏斗”)中,读取氧气体积时要注意 。
(2)取等物质的量浓度等体积H2O2溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如下表所示。
①实验1、2研究的是 对H2O2分解速率的影响。
②实验2、3的目的是 。
(3)用 (填“酸式”或“碱式”)滴定管量取25.00mL H2O2溶液于图II的烧瓶中,滴入过量KMnO4酸性溶液反应,最终收集到56mLO2(已折算为标准状况),则该H2O2溶液的物质的量浓度为 。
(已知:2KMnO4+5H2O2+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O)你认为测得的数值比理论值
(填“偏高”、“偏低”或“相等”)
(4)实验表明Na2O2与水反应也可生成O2。某同学猜想是Na2O2先与H2O反应生成H2O2,然后H2O2分解产生O2。为此做探究如下:取Na2O2样品(杂质不参与反应)与过量水充分反应的少量X溶液于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,该反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源:2011届福建省福州三中高三下学期第六次模拟考试(理综)化学部分 题型:实验题
过氧化氢(H2O2)俗称双氧水,不稳定,易分解。溶液的酸碱性对H2O2的稳定性有较大影响,如在碱性溶液中,H2O2分解较快。另外,H2O2见光、遇热、遇到大多数金属氧化物分解也会加快。以下装置可用于探究H2O2相关的性质。
请回答:
(1)实验室用MnO2作催化剂分解H2O2制取氧气,反应的化学方程式为 。
使用图1装置时,H2O2应该盛放在 (填“锥形瓶”或“分液漏斗”)中,读取氧气体积时要注意 。
(2)取等物质的量浓度等体积H2O2溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如下表所示。
①实验1、2研究的是 对H2O2分解速率的影响。
②实验2、3的目的是 。
(3)用 (填“酸式”或“碱式”)滴定管量取25.00mL H2O2溶液于图II的烧瓶中,滴入过量KMnO4酸性溶液反应,最终收集到56mLO2(已折算为标准状况),则该H2O2溶液的物质的量浓度为 。
(已知:2KMnO4+5H2O2+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O)你认为测得的数值比理论值
(填“偏高”、“偏低”或“相等”)
(4)实验表明Na2O2与水反应也可生成O2。某同学猜想是Na2O2先与H2O反应生成H2O2,然后H2O2分解产生O2。为此做探究如下:取Na2O2样品(杂质不参与反应)与过量水充分反应的少量X溶液于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,该反应的离子方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com