
分析 (1)二氧化氮为红棕色气体的物理性质解答;
(2)一氧化氮和空气中氧气接触方式反应生成红棕色气体二氧化氮;
(3)氨气极易溶于水,和氯化氢发生反应生成固体氯化铵;
(4)实验室制备氨气是利用氯化铵和氢氧化钙加热反应生成氨气.
解答 解:(1)二氧化氮是一种红棕色的气体,故选C,
故答案为:C;
(2)常温下在空气中很容易发生颜色改变的是NO,一氧化氮和空气中氧气接触方式反应生成红棕色气体二氧化氮,2NO+O2=2NO2,
故答案为:A;
(3)氨气极易溶于水,和氯化氢发生反应生成固体氯化铵,可用做“喷泉实验”,且遇到HCl会产生白烟的是氨气,
故答案为:B;
(4)实验室制备氨气是利用氯化铵和氢氧化钙加热反应生成氨气,选D,
故答案为:D.
点评 本题考查了物质性质、物质性质的应用、注意积累化学知识,掌握基础是解题关键,题目难度不大.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 在4mL0.1mol•L-1的K2Cr2O7溶液中滴加数滴1mol•L-1的NaOH溶液,溶液颜色从橙色变成黄色 | |
| B. | 配制0.1 mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释 | |
| C. | 用干燥且洁净的玻璃棒蘸取NaClO溶液,滴到放在表面皿上的pH试纸上测pH值 | |
| D. | 在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用,迅速混合后测出初始温度,用环形玻璃搅拌棒进行搅拌使酸和碱充分反应、准确读取实验时温度计最高温度、并且取2-3 次的实验平均值等措施,以达到良好的实验效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有①③ | C. | 只有①②③ | D. | 只有①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油经分馏后得到的汽油是纯净物 | |
| B. | 煤的干馏是复杂的物理化学变化,石油分馏是物理变化 | |
| C. | 从海水中得到无水MgCl2,电解熔融MgCl2制取金属镁 | |
| D. | 天然油脂是混合物,所以天然油脂没有固定的熔点和沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z 为 0.3 mol/L | B. | Y2为 0.4 mol/L | C. | X2为 0.2 mol/L | D. | Z 为 0.4 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
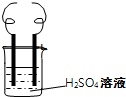 用电极a(铁丝)、电极b(铜丝)和H2SO4溶液可以构成原电池或电解池,如图所示.
用电极a(铁丝)、电极b(铜丝)和H2SO4溶液可以构成原电池或电解池,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | “除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+.发生的主要反应的离子方程式为2Fe2++H2O2+4NH3•H2O═2Fe(OH)3↓+4NH4+ | |
| B. | 配制硫酸铝溶液时,需用硫酸酸化的目的是抑制Al3+水解 | |
| C. | “结晶”这步操作中,母液需要蒸干后才能获得铵明矾晶体(含结晶水) | |
| D. | “分离”操作的名称是过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com