
| A. | 一定条件下,2mol SO2与足量O2反应可得到2mol SO3 | |
| B. | 含4mol HCl 的浓盐酸与足量的MnO2加热反应可制备1mol Cl2 | |
| C. | 10ml 18.0 mol/L H2SO4与足量铜加热反应可制备0.09 mol SO2 | |
| D. | 一定条件下,1mol N2与3 mol H2反应可制备1.0 mol NH3 |
分析 A、二氧化硫与氧气反应生成三氧化硫不可能完全转化;
B、实际上当反应进行到一定程度浓盐酸变稀,反应会停止,所以氯化氢不能全部反应;
C、金属铜可以和浓硫酸之间反应,但是和稀硫酸之间不反应;
D、1mol N2与3mol H2反应的产物氨气的量会小于2mol.
解答 解:A、一定条件下,2molSO2与足量O2反应得到SO3的量会小于2mol,故A错误;
B、含4mol HCl的浓盐酸与足量的MnO2加热反应,随着反应的进行,盐酸变稀,二氧化锰只能和浓盐酸反应,和稀盐酸之间不会发生反应,反应可制备Cl2的物质的量小于1mol,故B错误;
C、10mL 18.0mol/L H2SO4与足量铜加热反应,随着反应的进行,硫酸变稀,Cu和稀硫酸之间不反应,可制备SO2的物质的量小于0.09mol,故C错误;
D、一定条件下,1mol N2与3mol H2反应不能进行彻底,产生氨气的量会小于2mol,可以获得1.0mol NH3,故D正确.
故选D.
点评 本题涉及物质的性质以及化学反应的可逆性等方面的知识,注意知识的归纳和整理是关键,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①② | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物 | |
| B. | 碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子之间的作用力 | |
| C. | 烧碱固体溶于水的过程中,共价键被破坏 | |
| D. | 有机化合物CH3CH2NO2与H2N-CH2-COOH是同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 春蚕到死丝方尽,蜡炬成灰泪始干 | B. | 粉身碎骨浑不怕,要留清白在人间 | ||
| C. | 爆竹声中一岁除,春风送暖入屠苏 | D. | 野火烧不尽,春风吹又生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60g丙醇中存在的共价键总数为10NA | |
| B. | 1L 0.1mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA | |
| C. | 钠在空气中燃烧可生成多种氧化物.23g钠充分燃烧时转移电子数为1NA | |
| D. | 常温下,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
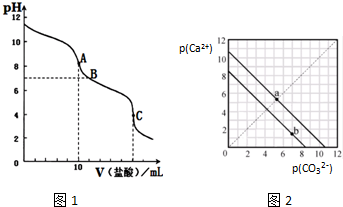
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无法比较 | B. | V(B)=0.6 mol/(L•min) | ||
| C. | V(AB3)=0.5 mol/(L•min) | D. | V(A)=0.4mol/(L•min) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com