
【题目】某化学兴趣小组的同学在实验室中用含有铝、铁、铜的废弃合金为主要原料制取硫酸铝溶液、硝酸铜晶体和无水氯化铁,其实验流程如下图所示。

已知:Fe3+沉淀的pH范围为1.9~3.2;Cu2+沉淀的pH范围为4.7~6.7。
请回答下列问题:
(1)写出向合金中加入KOH溶液后所发生反应的离子方程式:__________________,若在该反应中转移0.6NA的电子,则获得标准状况下的气体体积为________L。
(2)下列物质中可作为试剂Z的是_______(填序号)。
A.铜粉 B.氨水 C.氧化铜
加入Z后,调节溶液的pH范围应为________________。
(3)实验操作Ⅰ的顺序依次为____________(填序号)。
A.蒸发浓缩 B.过滤 C.冷却结晶
(4)写出滤渣E与W反应的化学方程式______________________。
【答案】(1)2Al+2OH-+2H2O=2AlO2-+3H2↑(3分)6.72
(2)C;3.2≤pH<4.7(或3.2<pH<4.7)
(3)ACB(4)Fe(OH)3+3HCl=FeCl3+3H2O(3分)
【解析】
试题分析:(1)合金中铝与氢氧化钠溶液反应,发生反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑;若在该反应中转移0.6NA的电子,则生成0.3mol氢气,标准状况下的气体体积为6.72L。
(2)试剂Z是调节溶液的pH,由于制备硝酸铜晶体不能引入新杂质,则c只能选择氧化铜,答案选C;调节pH的目的是沉淀铁离子,而不能沉淀铜离子,所以加入Z后,调节溶液的pH范围应为3.2≤pH<4.7。
(3)实验操作Ⅰ的顺序依次为蒸发浓缩、冷却结晶和过滤,答案选ACB;
(4)由于得到氯化铁溶液,所以滤渣E与W反应的化学方程式为Fe(OH)3+3HCl=FeCl3+3H2O。


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 干燥氯气能使pH试纸先变红后褪色
B. SO2能使溴水褪色,体现了SO2的漂白性
C. 硅酸钠的溶液中通入二氧化碳会产生沉淀
D. 固体Na2CO3比固体NaHCO3稳定,相同条件下在水中NaHCO3比Na2CO3溶解度更大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】
(1)元素的第一电离能:Al________Si(填“>”或“<”)。
(2)基态Mn2+的核外电子排布式为____________。
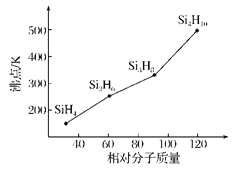
(3)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是________________________。
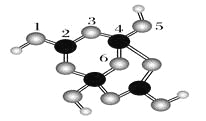
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:
①在Xm-中,硼原子轨道的杂化类型有________;配位键存在于________原子之间(填原子的数字标号);m=________(填数字)。
②硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有________ (填序号)。
A离子键 B共价键 C金属键 D范德华力 E氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅的说法不正确的是( )
A.硅是非金属元素,它的单质是灰黑色有金属光泽的固体
B.硅的导电性能介于导体和绝缘体之间,是良好的半导体材料
C.硅的化学性质不活泼,常温下不与任何物质发生反应
D.加热到一定温度时,硅能与氯气、氧气等非金属反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.直径介于1nm~100nm之间的微粒称为胶体
B.电泳现象可证明胶体带电
C.渗析法可用于含有氯化钠的淀粉溶液的提纯
D.用含1molFeCl3的溶液可制得6.02×1023个Fe(OH)3胶体粒子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com