
【题目】下列叙述中不正确的是
A. 以铁作阳极,铂作阴极,电解饱和食盐水,可以制备烧碱
B. 25℃下,在NH3·H2O稀溶液中加水稀释,![]() 的值不变
的值不变
C. 工业生产硫酸时,接触室催化氧化S02时使用热交换器可以充分利用热量,降低生产成本
D. 反应![]() 室温下不能自发进行,则△H>0
室温下不能自发进行,则△H>0
科目:高中化学 来源: 题型:
【题目】下列反应中,氯元素全部被氧化的是( )
A. 2P+3Cl2![]() 2PCl3
2PCl3
B. 2NaCl(熔融)![]() 2Na+Cl2↑
2Na+Cl2↑
C. NaOH+HClNaCl+H2O
D. 2Cl2+2Ca(OH)2CaCl2+Ca(ClO)2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.2 L由NaCl溶液、MgCl2溶液、CuCl2溶液组成的混合溶液中,部分离子的浓度如图所示。
(1)混合液中,NaCl的物质的量为_______mol,MgCl2的质量为_______g。
(2)该混合溶液中CuCl2的物质的量浓度为_____molL﹣1,将该混合溶液加水稀释至体积为1 L,稀释后溶液中Cu2+的物质的量浓度为_______molL﹣1。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种瑞香素的衍生物的结构简式如图,下列有关该有机物性质的说法正确的是

A. 能与FeCl3溶液发生显色反应
B. 1 mol该有机物最多可与3 mol H2加成
C. 1 mol该有机物最多可与含4 molNaOH溶液反应
D. 1 mol该有机物与足量NaHCO3溶液反应可放出3 mol CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质A有如图所示的转化关系(部分产物已略去),已知H能使溴的CCl4溶液褪色。
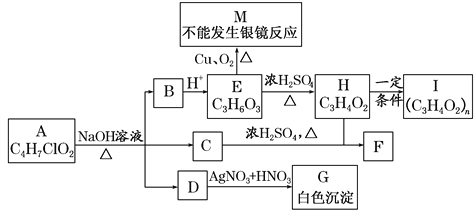
回答下列问题:
(1)A的结构简式为________。
(2)1 mol E与足量NaOH溶液反应时,消耗NaOH的物质的量为________mol。
(3)M的某些同分异构体能发生银镜反应,写出其中任意一种结构简式:________________。
(4)写出化学方程式H―→I:__________________________________。
(5)E通常可由丙烯、NaOH溶液、H2、O2、Br2等为原料合成,请按“A―→B―→C―→…”的形式写出反应流程,并在“―→”上注明反应类型但不需要注明试剂及反应条件________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过量的锌粉与一定量的稀盐酸反应,为了减慢反应速率,但是又不影响生成的氢气总量,可以采取的措施是
A.升高温度B.加入适量的水C.加入少量CuSO4溶液D.加入浓度较大的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化苄(C6H5CH2Cl)是一种重要的有机化工原料。工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄。
(1)写出甲苯与干燥氯气在光照条件下反应合成氯化苄的化学方程式________________。
(2)用下列方法分析氯化苄粗产品的纯度:
步骤I:称取2.555 g样品于烧瓶中,加入100.00 mL 4mol/L氢氧化钠溶液共热,冷却至室温。加入100.00 mL4mol/L硝酸,一段时间后,将烧瓶中的溶液全部转移至250.00 mL的容量瓶中,加水定容。
步骤II:从容量瓶中各取50.00 mL溶液于三只锥形瓶中,各加入25.00 mL0.2000mol/L硝酸银溶液。
步骤m:用硫酸铁铵作指示剂,用0.2000 mol/LNH4SCN溶液分别滴定剩余的硝酸银,所得滴定数据如下表。
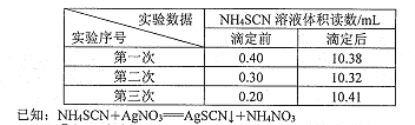
①加入硝酸的目的是____________。
②在步骤III操作中,判断达到滴定终点的现象是____。
③该样品中氯化苄的质量分数(写出计算过程)____。
④上述测定结果通常高于氯化苄中氯元素的理论含量,原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G为七种短周期主族元素,原子序数依次增大。已知:A、F的最外层电子数分别等于各自的电子层数,其中A的单质在常温下为气体。C与B、G在元素周期表中处于相邻位置,这三种元素原子的最外层电子数之和为17,质子数之和为31。D与F同周期,且在该周期中D元素的原子半径最大。下列说法不正确的是( )
A. C、D、G三种元素形成的盐,水溶液可能呈碱性
B. A与B能形成离子化合物A5B,且既含有离子键又含有共价键
C. B、C、G的简单氢化物中C的氢化物稳定性最强
D. D、E、F、G形成的简单离子半径逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验题
Ⅰ.课本实验
(1)苯甲酸的重结晶实验操作步骤是_________、__________、__________、分离晶体,粗苯甲酸溶解后还要加点水的目的是________________。
(2)为了验证溴乙烷中含有溴元素,有以下操作:①加硝酸银溶液 ②加NaOH溶液 ③加热 ④加蒸馏水 ⑤加硝酸至溶液显酸性,合理的顺序是(______)
A、②①③⑤ B、②④⑤③ C、②③⑤① D、②①⑤③
(3)在溴乙烷与NaOH乙醇溶液的消去反应中可以观察到有气体生成。有人设计了实验方案来检验生成的气体是否为乙烯,如图所示。

①Ⅰ中水的作用____________。
②Ⅱ中还可用________________,若用此物质,此时______(填“有”或“无”)必要将气体先通入水中。
Ⅱ.拓展实验
1,2一二溴乙烷可作抗爆剂的添加剂。下图为实验室制备1,2一二溴乙烷的装置图,图中分液漏斗和烧瓶a中分别装有浓H2SO4和无水乙醇,试管d中装有液溴。
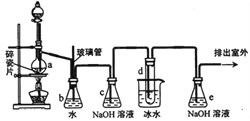
已知:
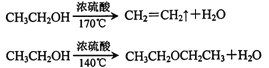
相关数据列表如下:
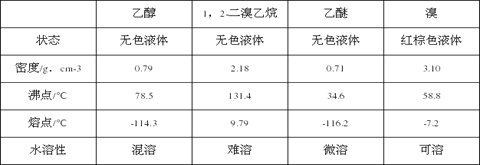
(1)实验中应迅速将温度升高到170℃左右的原因是__________________。
(2)安全瓶b在实验中有多重作用。其一可以检查实验进行中导管d是否发生堵塞,请写出发生堵塞时瓶b中的现象__________________;如果实验中导管d堵塞,你认为可能的原因是__________________;安全瓶b还可以起到的作用是___________________________;
(3)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是_______________;
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多,如果装置的气密性没有问题,试分析可能的原因___________________________;
(5)除去产物中少量未反应的Br2后,还含有的主要杂质为_______,要进一步提纯,下列操作中必须的是__________________(填入正确选项前的字母)。
A. 重结晶 B.过滤 C.萃取 D.蒸馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com