
将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g,则下列有关叙述中正确的是
A.加入合金的质量可能为9.6g
B.沉淀完全时消耗NaOH溶液体积为150mL
C.参加反应的硝酸的物质的量为0.4mol
D.溶解合金时产生NO气体体积0.224L(以标准状况)
【知识点】守恒法用于氧化还原反应计算 C2 C3 B3
【答案解析】C 解析:生成沉淀的质量比原合金的质量增加5.1g,说明OH—质量为5.1g,即0.3mol,金属结合氢氧根离子的物质的量与反应转化的电子的物质的量相等,所以反应转化的电子为0.3mol,生成的NO为0.1mol,根据氮原子守恒计算参加反应的硝酸的物质的量为0.4mol,故C正确;消耗NaOH溶液体积应为100mL,B错误;产生NO气体体积标况下应为2.24L,D错误;根据电荷守恒,镁、铜合金共0.15 mol,用极端假设法,如果全部是铜,质量为9.6g,所以合金质量应比9.6g小,A错误。
故答案选C
【思路点拨】本题考查了守恒法用于氧化还原反应计算,解题的关键是利用生成沉淀的质量比原合金的质量增加5.1g,即0.3mol,得到反应转化的电子为0.3mol。


科目:高中化学 来源: 题型:
(1)25。C时,0.1mol/L的HA溶液中c(H+)/c(OH-)=1010.请回答下列问题:
①HA是__________(填“强电解质”或“弱电解质”)。
②在加水稀释HA溶液的过程中,随着水量的增加而增大的是_________(填字母)。
A. c(H+)/c(HA) B. c(HA) /( A-)
C. c(H+)与c(OH-)的乘积 D.c(OH-)
(2)已知:CH4+H2O=CO(g)+3H2(g) 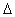 H=+206.2kJ·mol-1
H=+206.2kJ·mol-1
CH4+CO 2=2CO(g)+2H2(g) 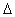 H=-247.4kJ·mol-1
H=-247.4kJ·mol-1
CH4(g)与H2O(g)反应生成CO 2(g)和H2(g)的热化学方程式为__________.
(3)下图是利用甲烷燃料电池电解50 mL 2mol/L的氯化铜溶液的装置示意图:
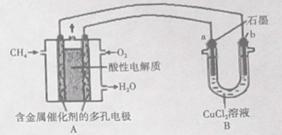
请回答:
①甲烷燃料电池的负极反应式为_______________.
②当线路中有0.6mol电子通过时,B中阳极产物的质量为___________g.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是
A、生铁中含有碳,抗腐蚀能力比纯铁弱 B、用锡焊接的铁质器件,焊接处易生锈
C、在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 D、铁管上镶嵌锌块,铁管不易被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
下表各选项中,不能利用置换反应通过Y得到W的一组化合物是( )
| 选项化合物 | A | B | C | D |
| Y | CO2 | Fe2O3 | SiO2 | FeCl3 |
| W | MgO | Al2O3 | CO | CuCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
右图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是 ( )

A.NH4Al(SO4)2 B.KAl(SO4)2
C.Al2(SO4)3 D.NaAlO2
查看答案和解析>>
科目:高中化学 来源: 题型:
在隔绝空气的条件下,某同学将一块部分被氧化的钠块用一张已除去氧化膜、并用针刺一些小孔的铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待钠块反应完全后,在容器中仅收集到1.12 L氢气(标准状况),此时测得铝箔质量比反应前减少了0.27 g,水槽和容器内溶液的总体积为2.0 L,溶液中NaOH的浓度为0.050 mol·L-1(忽略溶液中离子的水解和溶解的氢气的量)。
(1)写出该实验中发生反应的化学方程式:
;
(2)试通过计算确定该钠块中钠元素的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝溶液,并用于烟气脱硫。
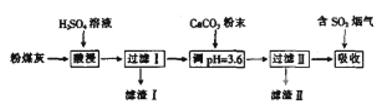
(1) (“能”或“不能”)用NaOH溶液代替H2SO4溶液。
(2)酸浸时反应的离子方程式为
(3)加CaCO3调节溶液的pH至3.6,其目的是 。Al2(SO4)x(OH)6-2x______(填“易”或“难”)于水。
(4)已知粉煤灰中Al2O3的质量分数为40.8%,制得的碱式硫酸铝【Al2(SO4)x(OH) 6-2x】中x=1.5.某实验小组取80.0g粉煤灰进行上述实验,假设在整个过程中铝的损耗率为10%,则可制得碱式硫酸铝的质量为__________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com